中国农业大学动科学院刘国世教授团队发现肝脏褪黑素信号的缺失会增加由代谢紊乱引发的2型糖尿病的发病风险
文章导读
肝脏褪黑素信号缺失竟会直接引发2型糖尿病?中国农业大学刘国世教授团队通过跨物种实验揭开代谢紊乱背后的关键机制。研究首次证实褪黑素受体缺陷会导致血糖升高、脂肪堆积,甚至引发胰岛素抵抗。更令人振奋的是,团队通过基因编辑培育出高产褪黑素绵羊,为糖尿病防治开辟全新路径。这项突破性发现将如何改变慢性病预防策略?
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,我校动物科学技术学院刘国世教授团队在国际知名学术期刊Cell Communication and Signaling上发表研究论文Loss of melatonin signaling increases the risk of T2DM caused by metabolic disorders。该研究通过人类群体遗传学分析、基因敲除小鼠模型及过表达褪黑素合成酶羊验证,系统阐明了褪黑素信号(褪黑素及受体)系统的缺陷是导致2型糖尿病(T2DM)及相关代谢综合征的重要风险因素 。

2型糖尿病(T2DM)是全球范围内的重大公共卫生挑战,其特征为胰岛素敏感性下降及糖脂代谢紊乱 。尽管全基因组关联分析(GWAS)已发现褪黑素受体MT1/MT2基因变异与T2DM易感性相关,但其具体生物学功能和分子机制一直未得到充分解析 。
刘国世教授团队通过多物种、多层面的深入研究,取得了以下突破性进展:研究发现,携带MT1受体(rs2119882)突变的人群具有更高的空腹血糖水平和身体质量指数(BMI)。代谢组学分析显示,该变异导致血浆中棕榈酸(饱和脂肪酸)水平升高,而油酸(不饱和脂肪酸)水平降低 。在细胞层面,抑制MT1和MT2受体会导致人肝细胞中葡萄糖转运蛋白(GLUT-4)和胰岛素受体(INSR)水平显著下降,进而抑制糖原合成 。利用CRISPR/Cas9技术构建的MT1/MT2基因敲除小鼠表现出明显的肥胖、脂肪肝、胰岛素抵抗和雄激素水平下降。在配合高脂饮食(HFD)挑战时,这种糖尿病表型被进一步放大 。团队通过体细胞核移植技术培育了内源性高产褪黑素(AANAT过表达)过表达褪黑素合成酶羊。实验证明,增强褪黑素信号(褪黑素及受体)能显著改善动物的糖耐量并提升胰岛素水平,这为T2DM的预防和治疗提供了新的策略依据 。
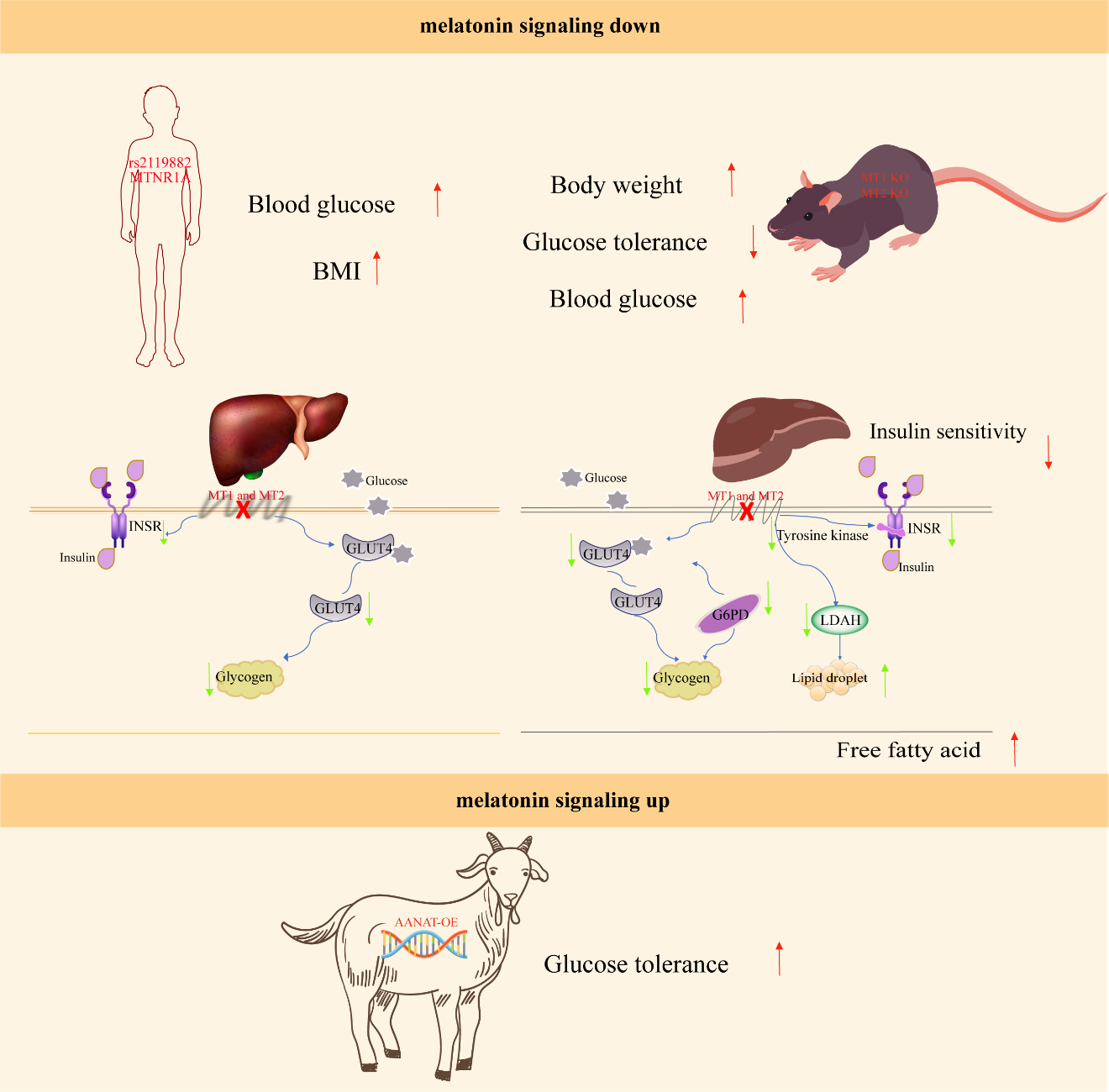
该研究通过“人-鼠-羊”跨物种研究模式,构建了完整的褪黑素信号(褪黑素及受体)调控糖脂代谢网络,明确了褪黑素受体缺失导致肝脏脂质沉积及全身性代谢紊乱的分子路径 。研究结果强调了保持完整褪黑素信号(褪黑素及受体)通路对于维持机体代谢平衡、降低2型糖尿病风险的重要性 。
中国农业大学动物科学技术学院博士研究生阎来庆、已毕业博士吕东颖和中国农业大学张鲁副教授为该论文的共同第一作者,中国农业大学动物科学技术学院刘国世教授为通讯作者 。中国农业大学动物科学技术学院郜宇博士后、西班牙奥维耶多大学Ana Coto-Montes教授、德国哥廷根大学Rüdiger Hardeland教授参与了本项研究并给予大力支持。研究得到了国家自然科学基金委面上项目(32172733)、重点项目(32430101)和青年项目(32202673)等项目的资助 。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。














说实话,我一直以为褪黑素只和睡眠有关,没想到它居然还能左右血糖和体重,真是开了眼界。
我在实验室玩过MT1敲除小鼠,真的发现代谢紊乱,和文里描述差不多。
哈哈,这研究太科幻了😂
褪黑素缺失居然跟肥胖挂钩?
哎,我最近也血糖偏高。
这事儿听起来挺吓人的。