我国学者在亚细胞定位邻近标记脂质组学技术方面取得新进展
文章导读
你是否知道,细胞器间的脂质转运竟藏着疾病发生的秘密?我国科学家朱正江与陈以昀团队在《自然・化学》发表突破性成果,首创亚细胞定位邻近标记脂质组学技术,无需分离细胞器即可精准捕捉线粒体、细胞核、溶酶体等内部的脂质分布。更通过“邻近标记+13C同位素”双标记策略,首次定量揭示PE脂质在不同细胞器中来源各异——线粒体依赖PSD途径,而细胞核与溶酶体则靠CDP-Etn途径。mTOR激活还能特异性提升溶酶体脂质含量,却不改变全细胞水平,这一发现为理解脂质代谢调控提供了全新视角与强大工具。
— 内容由好学术AI分析文章内容生成,仅供参考。
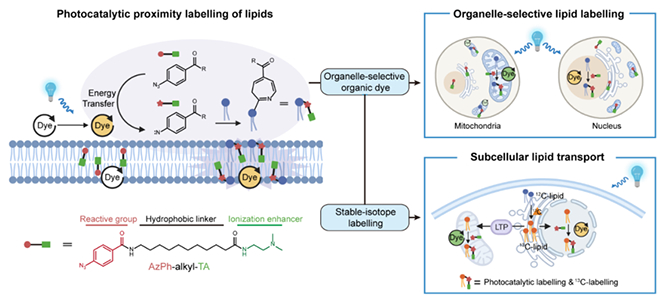
图 亚细胞定位邻近标记脂质组学技术
在国家自然科学基金项目(批准号:22425404,92357308,22337005)等资助下,中国科学院上海有机化学研究所朱正江团队与陈以昀团队合作在亚细胞定位邻近标记脂质组学技术方面取得进展,相关成果以“亚细胞定位邻近标记脂质组学技术及细胞器间脂质转运研究(Quantitative profiling of lipid transport between organelles enabled by subcellular photocatalytic labelling)”为题,于2025年8月6日在线发表于《自然・化学》(Nature Chemistry)期刊,论文链接:https://doi.org/10.1038/s41557-025-01886-w。
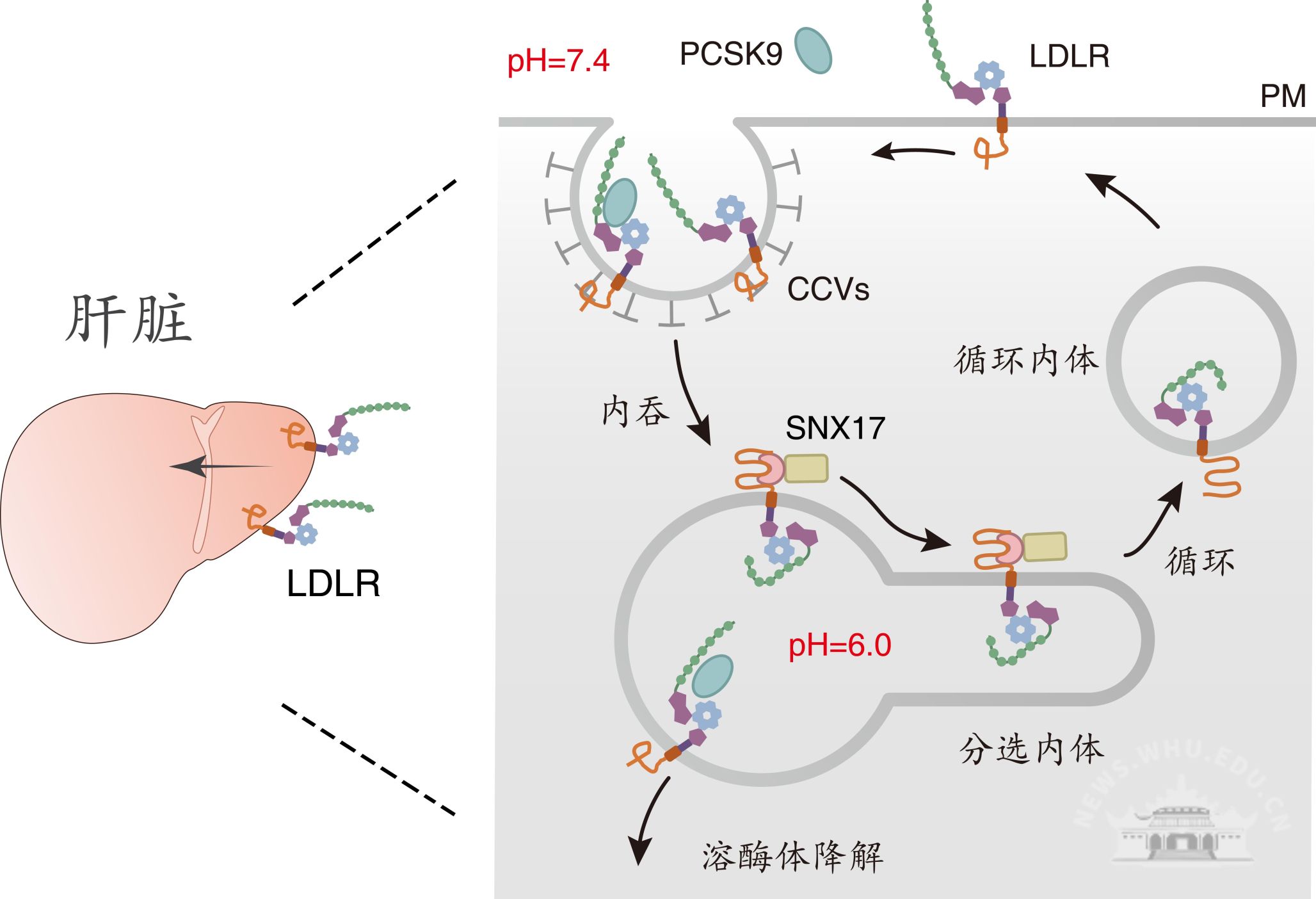
脂质是参与信号传导和能量储存等生命活动、构成细胞膜的核心物质,其功能与其在细胞内的空间分布密切相关。细胞内不同亚细胞结构通过独特的脂质组成,支持特定生化反应与功能需求,细胞器间脂质转运失调能导致多种人类重大疾病的发生。如何在生理状态下对亚细胞脂质的分布特征、转运路径及代谢规律进行精准化学测量,已成为当前生命科学领域亟待突破的重要课题。
针对该问题,上述研究团队开发了亚细胞定位邻近标记脂质组学技术,设计并合成了适用于脂质邻近标记的小分子探针,并以具有细胞器特异性定位的小分子荧光染料作为光催化剂,在光照射下激活并催化标记探针,使其与特定细胞器中的脂质分子反应,得到光催化标记脂质。结合高分辨质谱分析,该技术无需分离细胞器即可实现亚细胞定位脂质组的精准分析,在线粒体、细胞核与溶酶体中分别鉴定出 60~80 种脂质。研究团队进一步将亚细胞定位邻近标记脂质组学技术与稳定同位素示踪标记技术结合,发展出“邻近标记 + 13C-同位素”双标记示踪测量策略,系统定量表征了脂质分子从内质网到线粒体、溶酶体、细胞核等亚细胞器的转运规律,并分析了各种脂质合成途径和运输途径对特定细胞器内脂质组成的贡献比例。研究结果表明,线粒体中磷脂酰乙醇胺(PE)类脂质主要来源于磷脂酰丝氨酸脱羧酶合成途径(the PSD pathway),而细胞核与溶酶体中 PE 脂质主要来源于CDP-ethanolamine合成途径(the CDP-Etn pathway)。同时,研究也揭示mTOR 激活可特异性提高溶酶体中胆固醇、磷脂酰乙醇胺和磷脂酰丝氨酸的含量,而不影响整个细胞内脂质含量,为细胞器介导的脂质代谢调控研究提供了有力技术支撑。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...