中山大学张辉杨念生团队研究揭示巨噬细胞来源的VISTA在肠炎发病机制中的作用与机制
文章导读
肠道炎症为何反复难愈?中山大学张辉、杨念生团队重磅发现:巨噬细胞中的VISTA分子竟是关键"幕后推手"!研究首次揭示,在肠炎患者及小鼠模型中,VISTA异常激活后,竟通过LRIG1"锁死"肠道干细胞再生通路——它直接掐断脂肪酸氧化能量供应,导致肠黏膜修复瘫痪。更颠覆认知的是,阻断VISTA可快速缓解病变,且效果独立于传统免疫调节!这项发表于《细胞与分子免疫学》的突破,不仅破解了肠炎顽固复发的深层机制,更为百万患者点亮新希望:靶向VISTA-LRIG1轴或成治愈肠炎的黄金钥匙。立即解锁再生医学的革命性路径!
— 内容由好学术AI分析文章内容生成,仅供参考。
(通讯员康峻鸣)近日,附属第一医院张辉研究员、杨念生教授团队研究发现,在炎症性肠病(IBD)患者及结肠炎小鼠模型中,VISTA在促炎的单核/巨噬细胞中的表达显著上调,敲除或阻断VISTA可显著减轻结肠炎小鼠的肠道病变,但不影响肠道炎症与肠道微生态,该保护作用在清除巨噬细胞后消失。机制上,巨噬细胞来源的VISTA通过与肠道干细胞上的LRIG1分子结合,抑制ErbB2-mTOR-4EBP1信号通路而下调PPARα信号,抑制脂肪酸氧化(FAO)水平,引起肠道类器官生长和上皮再生障碍。相关研究发表于国际知名期刊《细胞与分子免疫学》(Cellular & Molecular Immunology)。
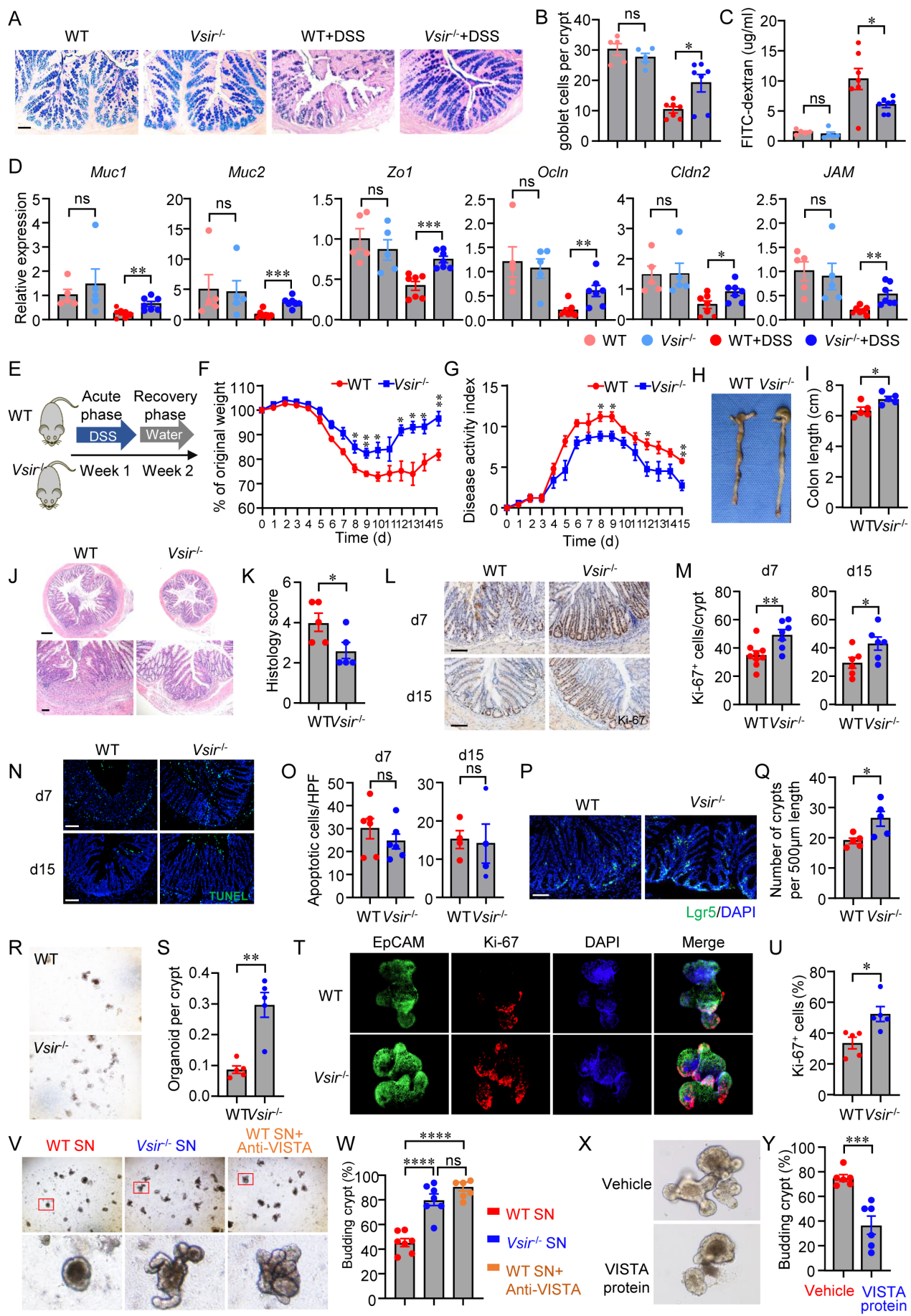
本研究首次阐明了巨噬细胞来源的VISTA-LRIG1轴在肠道屏障修复中的关键调控作用,揭示了其独立于传统免疫调节的致病机制,提示靶向VISTA-LRIG1轴可为肠炎患者提供新的策略。
附属第一医院风湿免疫科/精准医学研究院张辉研究员为该论文最后通讯作者,风湿免疫科杨念生教授是共同通讯作者,风湿免疫科李梦圆博士后、陈斌锋医师、胃肠外科王志雄副教授、风湿免疫科硕士研究生郭瑞祥为共同第一作者。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...