中国农业大学营养与健康系任发政院士团队揭示不合理膳食导致肝脏代谢紊乱新机制 为食源性干预提供精准靶点
文章导读
你是否知道,不合理的饮食会悄悄“关闭”肝脏的自我清洁功能?中国农业大学任发政院士团队最新研究发现,高脂高胆固醇饮食会显著降低肝脏中G3BP1蛋白水平,导致自噬受阻、脂质堆积,进而引发脂肪肝和代谢紊乱。这项发表于《Nature Communications》的成果首次揭示了G3BP1通过调控TFE3影响脂质代谢的分子机制,为精准营养干预提供了关键靶点。颠覆传统认知,从源头破解脂肪肝成因,这项研究或将改变我们对抗代谢性肝病的方式。
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,中国农业大学营养与健康系任发政院士团队张昊与刘蓉教授在Nature Communications期刊在线发表研究论文Dysregulation of GTPase-activating protein-binding protein1 in the pathogenesis of metabolic dysfunction-associated steatotic liver disease。

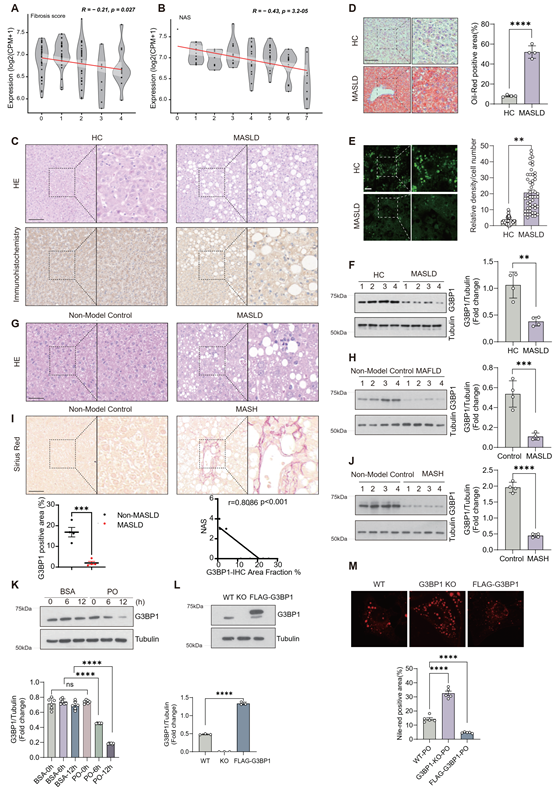
随着现代饮食结构的变迁,代谢功能障碍相关脂肪性肝病(MASLD)已发展成为影响全球数亿人健康的重大公共卫生挑战。长期摄入高脂(HFD)或高脂高胆固醇(HFHC)等不合理膳食,显著增加了肝脏脂质异常堆积、炎症反应及系统性代谢紊乱的风险。在这一背景下,深入探索MASLD发生的分子机制并确立有效的营养干预策略,成为当前研究的热点。
近日,研究团队在代谢功能障碍相关脂肪性肝病的发病机制研究中取得重要突破。研究发现,长期摄入高脂(HFD)和高脂高胆固醇(HFHC)饮食的动物模型肝脏中G3BP1蛋白水平显著下降,并伴随严重的肝脂肪变性、炎症浸润及代谢功能失调。这一重要发现揭示了G3BP1与饮食诱导的肝代谢紊乱之间存在密切关联。
进一步的研究表明,G3BP1在调控肝脏脂质稳态中发挥着核心作用。它通过维持自噬流的正常运行、影响转录因子TFE3的核质定位,精密调节脂质的降解与合成。尤其重要的是,G3BP1的功能缺失会导致自噬过程受阻,脂滴清除效率下降,从而加剧肝内脂质沉积。本研究从分子层面阐释了不良饮食模式导致代谢功能障碍相关脂肪性肝病的具体机制,为“精准营养”干预提供了新思路。
中国农业大学任发政院士、张昊教授、刘蓉教授为共同通讯作者。中国农业大学博士后欧阳芹芹,苏黎世联邦理工学院博士后苏佳琪,中国农业大学副教授李依璇为共同第一作者。该研究得到国家自然科学基金、国家重点研发计划项目(32361163613,92354302-1, 3240801,2024YFF1106001)的资助。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...