文章导读
你拼命运动、节食,体重却纹丝不动?大多数人以为减肥靠的是热量缺口,却忽略了身体里一个被长期忽视的“产热开关”。清华团队最新研究发现,肌肉分泌的肌泌降糖素(Feimin)在寒冷刺激下能潜入脂肪细胞,激活一条全新的产热通路——这个机制一旦被破解,或许意味着未来不用挨饿也能高效燃脂。但问题来了:为什么肥胖人群的这个通路会失灵?答案可能比你想象的更残酷。
— 内容由好学术AI分析文章内容生成,仅供参考。
肥胖及相关代谢性疾病已成为全球性的健康挑战。适应性产热作为机体抵御肥胖的重要防御机制,通过能量消耗维持代谢稳态,然而,其中能量感知与转录控制相耦合的分子机制,科学界仍不完全清楚。
5月5日,清华大学生命学院王一国教授团队与中南大学湘雅二医院张晶晶教授团队合作,在《美国国家科学院院刊》(Proceedings of the National Academy of Sciences of the United States of America, PNAS)发表题为“胞内肌泌降糖素促进寒冷诱导的产热”(Cellular Feimin promotes cold-induced thermogenesis)的研究论文。研究揭示了肌肉分泌因子肌泌降糖素(Feimin)在脂肪组织中调控寒冷诱导产热的关键作用及其分子机制。此前,该团队已发现肌泌降糖素在进食后由肌肉分泌,调节血糖稳态;在运动后入核,抑制肌肉产热并提高运动耐力。该研究中,团队聚焦脂肪组织,首次阐明了肌泌降糖素在寒冷刺激下介导适应性产热的新功能。
研究显示,在高脂诱导的肥胖小鼠和肥胖人群的脂肪组织中,肌泌降糖素的磷酸化水平与核定位均显著降低;而在寒冷暴露下,两者均显著升高。这提示肌泌降糖素可能在调控脂肪产热、抵抗肥胖中发挥重要作用。为进一步验证,研究人员构建了脂肪组织特异性肌泌降糖素敲除小鼠(Feimin AKO)。结果发现,在寒冷刺激下,Feimin AKO小鼠体温显著下降,耗氧量和能量消耗均降低。在高脂饮食诱导的肥胖模型中,该小鼠体重增长更快,脂肪堆积更严重,并表现出更明显的糖耐量异常和胰岛素抵抗,表明肌泌降糖素缺失会加剧饮食诱导的肥胖及相关代谢紊乱。
基于前期研究,AMPK能够磷酸化胞内肌泌降糖素(cFeimin)并促进其入核。在冷刺激过程中,伴随AMPK的激活,胞内肌泌降糖素的磷酸化水平及核内信号显著增强。通过对AMPK脂肪特异性敲除小鼠的表型分析发现,敲除AMPK显著抑制了冷刺激诱导的肌泌降糖素磷酸化及其核转位。为进一步明确胞内肌泌降糖素入核后如何调控产热,研究人员利用蛋白质组学筛选,发现胞内肌泌降糖素能够与转录共激活因子PGC1α结合。免疫共沉淀等实验进一步证实,入核后的Feimin正是通过与PGC1α相互作用,促进脂肪组织产热。
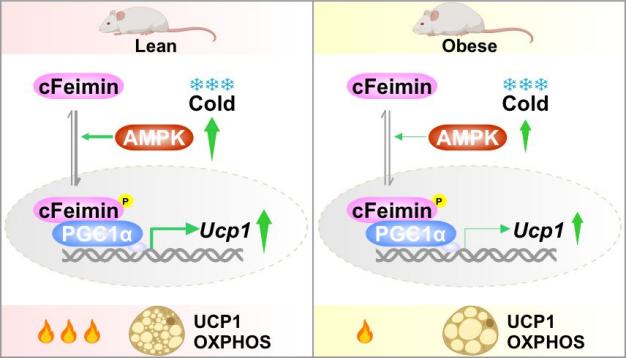
寒冷条件下胞内肌泌降糖素入核并与PGC1α相互作用,增强脂肪组织产热
综上所述,研究明确了“AMPK-cFeimin-PGC1α信号轴”在调控寒冷诱导产热中的关键作用。结合研究团队此前在饮食与运动背景下对肌泌降糖素功能的探索,相关研究共同描绘了肌泌降糖素在多种代谢应激条件下(如进食、运动和寒冷刺激)通过不同作用形式与机制灵活调节能量代谢的全景图,为肥胖及相关代谢性疾病的治疗策略开发提供了重要的新靶点。
清华大学生命学院教授王一国与中南大学湘雅二医院教授张晶晶为论文共同通讯作者。清华大学生命学院已出站博士后彭颖、石晓柳,2023级博士生王亚卓为论文共同第一作者。王一国实验室2023届博士毕业生贾良杰、博士后李甜甜,张晶晶实验室博士后蔡梓歆、2025级博士生李豪亦为研究作出重要贡献。
研究得到国家自然科学基金委、科技部、清华大学“笃实计划”、清华-北大生命科学联合中心、清华大学钱塘生命科学发展基金等的支持。
论文链接:
https://www.pnas.org/doi/epdf/10.1073/pnas.2534599123
供稿:生命学院
编辑:李华山
审核:郭玲
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。

















清华又出成果了,支持一下👍