文章导读
面对癌症转移,你是否以为只要切除原发灶就能高枕无忧?绝大多数患者和家属都忽略了那个在肿瘤扩散前就已悄然形成的“隐形陷阱”。南京大学团队最新发现,癌细胞竟能提前操控肺部代谢,分泌棕榈酸破坏血管屏障,为致命转移铺平道路。这解释了为何许多治疗看似成功却最终复发。更惊人的是,研究已找到阻断这一链条的钥匙,不仅能降低转移负荷,还能重塑免疫环境。这个被长期忽视的“脂质信号”究竟如何成为生死攸关的转折点?
— 内容由好学术AI分析文章内容生成,仅供参考。
肿瘤远处转移是导致癌症患者死亡的主要原因,而肿瘤细胞为何“选择性”定植于特定器官,仍是国际肿瘤学界亟待破解的重大科学难题。围绕这一关键问题,研究团队聚焦“转移前生态位”(Pre-metastatic niche)的形成机制,深入解析肺部微环境中代谢重编程与免疫调控之间的交互网络。
研究首次发现三阴性乳腺癌在远端转移发生前,即可通过系统性信号重塑肺部脂质代谢,诱导肺血管内皮细胞大量分泌棕榈酸(Palmitic acid),在肺组织中构建一个富含脂质的促转移微环境;该脂质信号通过激活中性粒细胞中的TLR4–NF-κB通路,促使其释放关键炎症因子LCN2(Lipocalin-2),破坏肺微血管内皮的紧密连接结构,为循环肿瘤细胞的外渗和肺部定植打开通道。
更重要的是,研究团队通过靶向干预肺内皮细胞的脂肪酸合成途径,成功阻断了这一级联反应,不仅显著降低肺转移负荷,还同步改善了肺部的抗肿瘤免疫微环境。该工作不仅阐明了代谢-免疫互作驱动器官特异性转移的新机制,也为临床干预肿瘤转移提供了全新的理论支撑与潜在治疗策略。
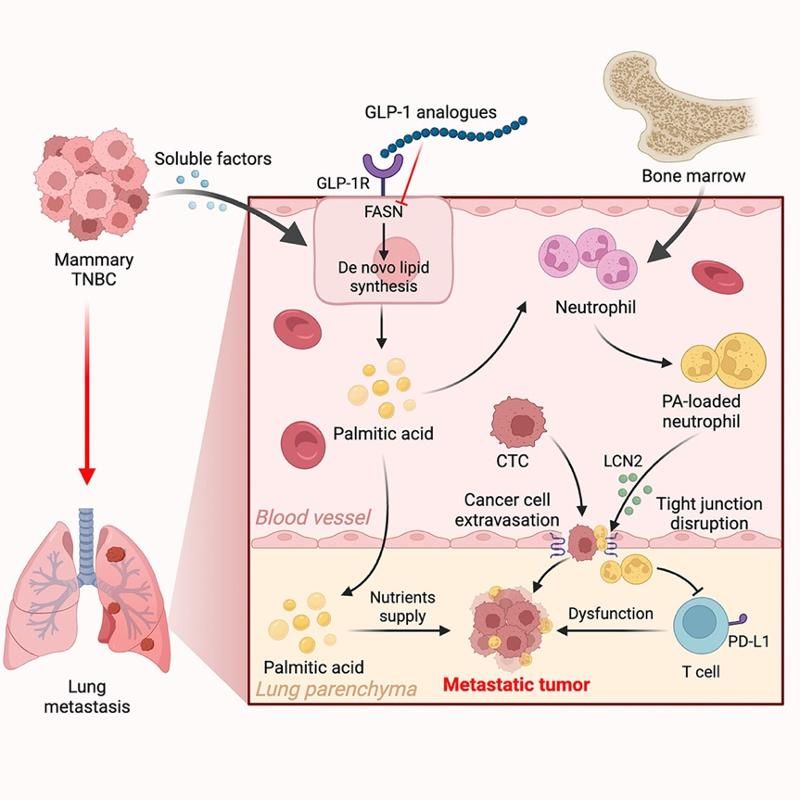
本研究提出了“脂质–免疫–血管屏障”时空协同促进肿瘤器官倾向性转移的新理论,成果于2026年4月24日,在线发表于Cell子刊《Immunity》杂志。南京大学医学院博士毕业生钱鹏、博士研究生李玉鑫和韩毅峰为论文共同第一作者;南京大学医学院附属鼓楼医院邹征云教授为共同通讯作者;鼓楼医院病理科许纯博士为本研究提供了病理学支持。
原文链接:https://www.sciencedirect.com/science/article/pii/S1074761326001378
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。















南大这波操作太牛了,终于能治转移了!