文章导读
你以为物种进化只是单向的“优胜劣汰”?要么获得功能,要么彻底丢失?清华最新研究直接颠覆了这一认知:在同一裂殖酵母群体中,竟同时上演着截然相反的进化剧本。一部分菌株通过基因沉默或丢失主动“自废武功”,另一部分却靠水平基因转移疯狂“扩容”出超强代谢力。这种双向并行的进化机制,不仅解释了微生物如何极致适应环境,更暴露了传统演化模型中最大的盲区。当“退化”与“增强”成为同一物种的生存双策略,我们过去对生命适应性的理解是否从一开始就错了方向?
— 内容由好学术AI分析文章内容生成,仅供参考。
传统观点认为,进化对于某一特定性状而言是“单行道”:一个物种要么丢失,要么获得某种功能。然而,清华大学生物医学交叉研究院杜立林实验室发现,同一物种可以同时沿两个相反方向进化:有些裂殖酵母菌株通过基因丢失或沉默丧失半乳糖利用能力,另一些则通过水平基因转移与基因扩增获得更强的代谢能力。这一“双向进化”范式为理解真核微生物代谢性状的进化提供了新视角。
微生物代谢能力的变异是决定其环境适应性进化的关键。芽殖酵母(Saccharomyces cerevisiae)的半乳糖代谢途径(Leloir 途径)是研究代谢性状进化的经典模型,该途径依赖三种酶的协同作用,其编码基因在真菌中往往成簇存在。裂殖酵母(S. pombe)作为遗传学和进化生物学研究的重要对象,与芽殖酵母亲缘关系较远,二者约在五亿年前分化。此前,科学界针对裂殖酵母半乳糖代谢途径的研究较少,对于自然界中裂殖酵母个体在半乳糖利用能力上的多样性亦不清楚。
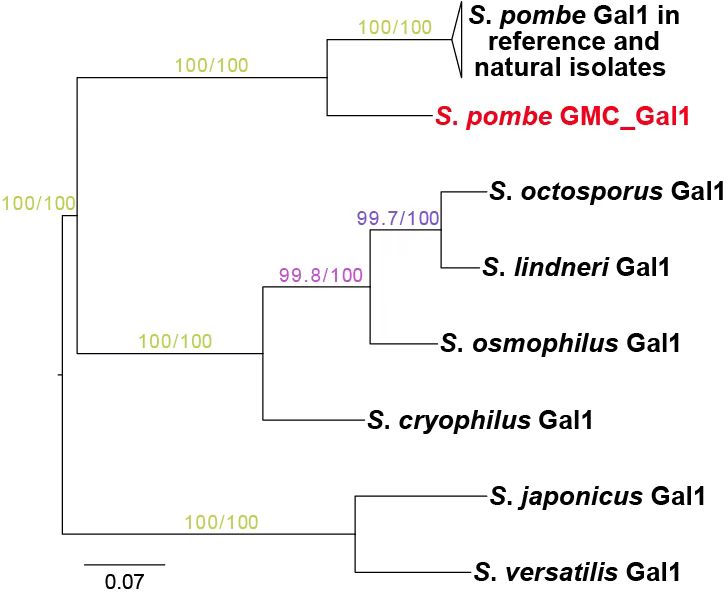
GMC_Gal1及其同源物在裂殖酵母中的最大似然法系统发育树
研究人员系统分析了覆盖裂殖酵母已知遗传多样性的58个自然分离株,发现它们在半乳糖利用能力上存在异乎寻常的表型多样性:从完全不能利用半乳糖(Gal−)到在半乳糖培养基上异常快速生长(GalF),呈现出从功能丧失到功能增强的广泛跨度。
不能利用半乳糖的Gal−表型源于两类机制:一是基因丢失,7个菌株通过3种不同途径(转座子介导的重组、微同源介导的缺失以及DUF999家族基因间的重组)完全或部分缺失了gal基因簇;二是表达沉默,另外10个菌株虽保留完整的gal基因簇,但其表达受到MAPK信号通路和转录抑制蛋白Ssn6的抑制,导致表达水平不足。
与Gal−表型相反,GalF菌株的超强半乳糖利用能力源于参考基因组中不存在的多拷贝基因簇:gal-melcluster(GMC)。该基因簇以4至8个串联拷贝形式存在,每个拷贝含9个基因,除编码半乳糖代谢酶外,还包含一个水解蜜二糖(melibiose)的蜜二糖酶的基因。进一步实验表明,高拷贝数带来的基因剂量效应导致了GalF表型。GMC不仅增强了半乳糖利用能力,还赋予了菌株利用蜜二糖的能力(Mel⁺)。Mel⁺表型几乎完全与GMC关联,仅有一个例外的Mel⁺菌株携带了一个独立的蜜二糖酶基因。系统发育分析表明,这些增强代谢能力的基因源于水平基因转移。
综上所述,该工作揭示了真核微生物代谢性状可塑性的新范式:相反方向的进化力量可在一个物种内协同作用,共同塑造代谢多样性。
研究成果以“基因丢失、抑制、扩增和水平获取形成了裂变酵母的半乳糖/二糖代谢”(Gene loss, repression, amplification, and horizontal acquisition shape galactose/melibiose metabolism in fission yeast)为题,于4月24日发表于《美国国家科学院院刊》(Proceedings of the National Academy of Sciences of the United States of America, PNAS)。
清华大学生物医学交叉研究院杜立林实验室的杜晓敏博士为论文第一作者,杜立林教授为论文通讯作者。其他作者还包括杜立林实验室的生物信息员索芳。该研究在北京生命科学研究所完成。
论文链接:
https://doi.org/10.1073/pnas.2532532123
供稿:生物医学交叉研究院
编辑:李华山
审核:郭玲
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。













清华这实验室又搞大事了,双向进化听着就牛。