文章导读
当你在实验室盯着细胞应激反应的数据一筹莫展时,是否想过,决定生死的可能不是某个明星蛋白,而是核糖体上一段曾被当作“冗余垃圾”的rRNA扩展片段?我们一直以为真核细胞调控翻译靠的是复杂因子网络,但北大郭强团队用冷冻电镜拍下的原位图像显示:动物细胞在压力下会直接让核糖体“手拉手”休眠。更震撼的是,这个过程不靠外源因子,而是由ES31b、ES30a等扩展片段自主介导——这些长期被忽视的序列,竟然是细胞存亡的关键开关。如果未来药物能精准干预这一机制,你现在的研究方向会不会一夜过时?
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,北京大学生命科学学院郭强研究员课题组在Nucleic Acids Research在线发表了题为“rRNA expansion segments mediate ribosome dimerization as a conserved stress response”的研究论文。该研究利用冷冻电子断层扫描成像(cryo-ET)技术,在细胞原位解析了核糖体的翻译活性与空间分布形式,揭示了动物细胞中核糖体通过rRNA扩展片段形成二聚体的分子机制,并阐明该过程是一种保守的应激响应,参与翻译调控。
核糖体是由蛋白质和核糖体RNA(rRNA)构成的大型分子机器,承担着细胞内全部蛋白质合成的核心功能。蛋白质合成是细胞中能量消耗最高的过程之一,因此在受到外界胁迫时,细胞往往会迅速降低整体翻译水平。在细菌中,除了对单个核糖体翻译活性的调控外,细胞还可在环境应激条件下依赖休眠因子促使核糖体形成二聚体,从而实现更高层次的翻译调控[1]。这种休眠状态有利于核糖体的储存和保护,维持核糖体群体的稳定性,并在应激解除后促进翻译的快速恢复[2]。然而,真核细胞中是否存在类似的、通过调控核糖体空间拓扑组织来调节翻译活性的机制,长期以来尚不清楚。
在本研究中,利用cryo-ET对大鼠神经元进行原位观察,并结合课题组此前开发的邻近分子拓扑分析方法NEMO-TOC[3],发现应激诱导条件下核糖体会形成两种无活性的二聚体结构(如图)。值得注意的是,这两种二聚体中的核糖体相互作用分别由rRNA扩展片段ES31b,以及ES30a和ES20a介导,并通过“kissing-loop”方式实现二聚化;这一机制随后又在生化实验中得到了进一步验证(图E)。rRNA扩展片段是真核核糖体特有的rRNA序列,其在进化过程中具有显著的序列差异,因此长期以来常被视为核糖体中的“结构性冗余”区域,相关功能研究相对有限[4]。本研究首次表明,特定的rRNA扩展片段可在应激条件下直接介导核糖体二聚化。此外,研究还发现,这种核糖体二聚化现象在嘌呤霉素处理、氨基酸缺乏以及内质网应激等多种条件下均可发生,并在应激解除后迅速消失,显示出明显的动态可逆性。
值得一提的是,在本研究审稿期间,Science杂志发表了题为“Ribosomal RNA expansion segments mediate the oligomerization of inactive animal ribosomes”的相关研究[5]。该工作进一步证明,核糖体二聚体对维持细胞在应激状态下的存活具有重要作用。与Science论文仅报道由ES31b介导的一种二聚体结构相比,本研究还进一步发现了另一种由ES30a和ES20a介导的核糖体二聚体。结合课题组此前在U2OS细胞中发现的由ES27L介导的核糖体二聚体[6],这些结果共同提示:rRNA扩展片段的不同区域可能通过介导休眠核糖体二聚体的形成,广泛参与真核细胞的翻译调控。
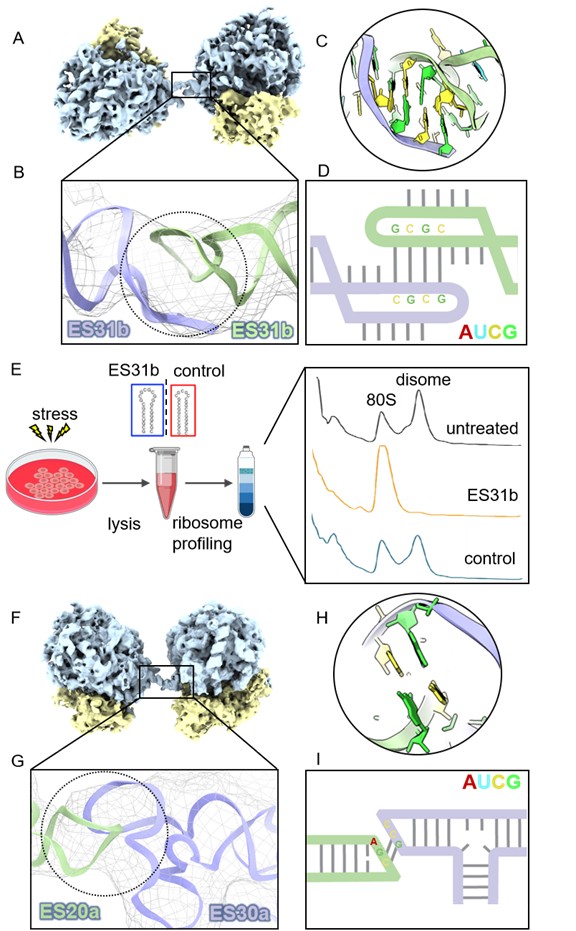
rRNA扩展片段介导的核糖体二聚化机制。A—D. 核糖体rRNA扩展片段ES31b介导二聚体的形成;E. RNA竞争实验验证二聚体相互作用界面;F—I. 核糖体rRNA扩展片段ES30a和ES20a介导的另一类二聚体形成
综上,本研究确立了rRNA扩展片段在应激诱导核糖体休眠二聚化过程中的核心作用,拓展了对翻译调控机制的认识。不同于原核细胞依赖休眠因子实现核糖体失活与储存的方式,真核细胞可直接利用核糖体自身的rRNA元件,实现快速且可逆的应激响应,为理解翻译调控的空间组织原则提供了新的视角。
郭强、凯斯西储大学Derek J Taylor教授、Maria Hatzoglou教授为本论文共同通讯作者,郭强实验室江文宏博士(现为湖北工业大学副教授),博士研究生陈晨、王星为共同第一作者。本工作得到科技部重点研发计划、国家自然科学基金、北京市杰出青年基金等的支持。
参考文献:
[1] Matzov, D. et al. The cryo-EM structure of hibernating 100S ribosome dimer from pathogenic Staphylococcus aureus. Nature Communications 8, 723, (2017).
[2] Feaga Heather, A., Kopylov, M., Kim Jenny, K., Jovanovic, M. & Dworkin, J. Ribosome Dimerization Protects the Small Subunit. Journal of Bacteriology 202, 10.1128/jb.00009—00020, (2020).
[3] Jiang, W. et al. A transformation clustering algorithm and its application in polyribosomes structural profiling. Nucleic Acids Research 50, 9001—9011, (2022).
[4] Hariharan, N., Ghosh, S. & Palakodeti, D. The story of rRNA expansion segments: Finding functionality amidst diversity. WIREs RNA 14, e1732, (2023).
[5] Schwarz, A. et al. Ribosomal RNA expansion segments mediate the oligomerization of inactive animal ribosomes. Science 391, eadr4287, (2026)
[6] Wu, Y. et al. Translation landscape of stress granules. Science Advances 11, eady6859, (2025).
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。














那平时没应激的时候这些ES片段干嘛去了?
以前一直觉得ES那段就是冗余垃圾,这下打脸了。
这标题看着就头大,直接滑到底了。