文章导读
过去十几年,我们一直以为抑癌基因p53是细胞重编程的“绊脚石”,为了追求逆转细胞命运的高效率,只能强行抑制这个防癌守门人,代价却是让产物极易突变致癌。但邓宏魁团队最新发表在《细胞》的研究彻底颠覆了这一铁律:在化学重编程中,p53竟是不可或缺的“守护者”,抑制它反而会让效率暴跌。这套化学小分子组合究竟如何巧妙化解“防癌”与“增殖”的死结,甚至自动清除突变细胞?读懂这个底层机制的翻转,你才会明白未来真正安全的干细胞治疗离我们有多近。
— 内容由好学术AI分析文章内容生成,仅供参考。
2026年4月17日,北京大学博雅讲席教授、昌平实验室领衔科学家、生命科学学院邓宏魁课题组在国际学术期刊《细胞》(Cell)上发表了题为“p53 safeguards chemical reprogramming of human somatic cells toward pluripotency”的研究论文。该研究发现,关键肿瘤抑制因子p53在化学重编程中发挥核心保护作用,打破了“p53阻碍细胞重编程”的传统认知。化学重编程的这一特性,揭示了其与转录因子重编程在机理上的根本区别和独特优势,为安全、可控地制备人多能干细胞和细胞重编程研究提供了新理论和新策略。

论文截图
细胞重编程可通过调控细胞命运,诱导获得适用于临床治疗的目标细胞类型,开辟了再生医学新的路径。2006年,日本科学家山中伸弥(Shinya Yamanaka)借助病毒载体将Oct4、Sox2、Klf4和c-Myc四个转录因子(OSKM,即“山中因子”)导入成体细胞,将其重编程为诱导多能干细胞(iPS细胞),是生命科学研究里程碑式的突破。
然而,iPS技术在抑癌因子p53调控层面却存在一个生物学悖论。早在2008年,邓宏魁团队发现p53是细胞重编程的关键障碍:抑制p53可以显著提高山中因子介导的重编程效率(Cell Stem Cell, 2008)。2009年,《自然》(Nature)杂志同期刊发的五项独立研究进一步证实了这一结果。p53因能抑制细胞异常增殖和肿瘤发生而广为熟知,但成体细胞却需借助山中因子中的原癌基因来增强细胞可塑性和增殖能力,进而实现高效重编程。山中因子所包含的原癌基因与p53抑癌通路之间相互拮抗,抑制p53虽能促进重编程,却会同时降低对基因组稳定性的保护。
原癌基因与抑癌基因之间的博弈,体现了通过转录因子强制驱动的细胞重编程技术存在潜在的肿瘤发生风险。随着部分重编程(partial reprogramming)等技术的兴起,这一长期悬而未决的难题受到了更为广泛的关注。因此,精准调控p53活性,使其既能在重编程过程中发挥基因组保护作用,又不影响重编程效率,是细胞重编程技术应用的关键。
与转录因子强制驱动的细胞重编程不同,自然界中的一些动物组织再生过程巧妙地解决了“p53的抑癌功能”与“细胞增殖和重编程”之间的矛盾。p53不仅是肿瘤防控的“守门人”,还在蝾螈断肢再生、鹿角再生等剧烈生理重塑过程中,通过时空和下游功能的动态调控,确保细胞增殖和去分化有序可控。这些自然再生过程提示,“p53的抑癌活性”与“细胞重编程”不一定是相悖和矛盾的。
2013年,邓宏魁团队首次建立了完全利用化学小分子将体细胞重编程为多能干细胞(CiPS细胞)的化学重编程技术(Science, 2013),并在2022年实现了诱导人CiPS细胞(Nature, 2022)。化学重编程通过小分子组合的精确调控,以类似低等动物组织再生的过程使细胞有序产生去分化状态,并借助具有可塑性的中间态细胞完成多能性的构建(Nature, 2022;Cell Rep ., 2023;Cell Stem Cell, 2024)。
在该项最新研究成果中,邓宏魁团队发现p53是化学重编程的“守护者”而非“障碍”。实验结果显示,抑制p53会大幅降低CiPS细胞诱导效率(如图1),与OSKM重编程体系中“抑制p53提高重编程效率”的经典结论截然相反。这种依赖p53活性的重编程路径为化学重编程带来了重要的安全保障:平行对比实验显示,OSKM重编程更容易在iPS细胞中富集p53缺陷,而化学重编程则能有效清除p53缺陷的异常细胞,确保CiPS细胞的基因组稳定性。
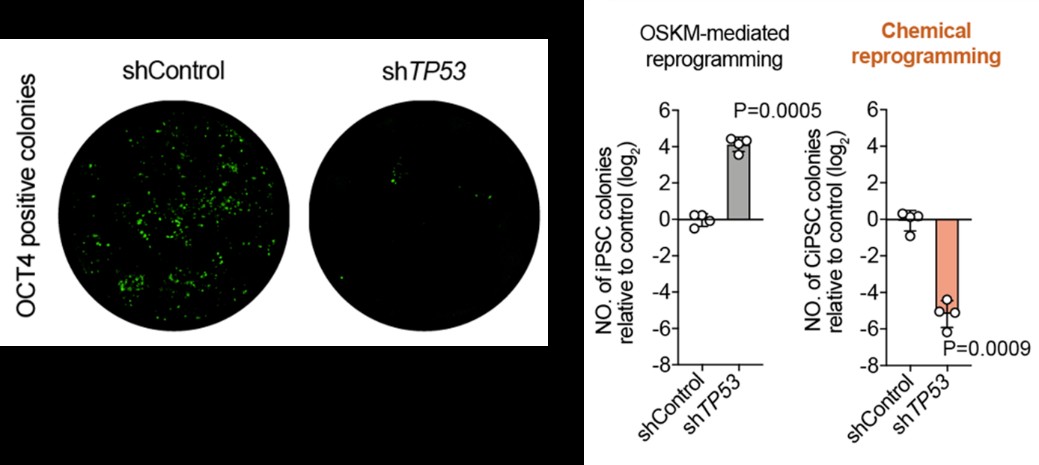
图1. 抑制p53活性大幅降低CiPS细胞诱导效率
该研究还揭示了化学重编程如何兼顾p53活性和细胞增殖的分子机制。结果显示,化学小分子组合可以实现p53不同下游功能的选择性激活,巧妙解决了“p53激活”与“细胞增殖抑制”之间的矛盾:一方面,化学小分子调控视黄酸受体通路激活是上调p53及其下游BTG2基因表达的关键,抑制重编程过程中细胞过度间质化;另一方面,化学小分子抑制TGF-β通路并下调了p53下游的细胞周期抑制因子p21,实现了在维持p53活性的同时保障细胞增殖能力(如图2)。
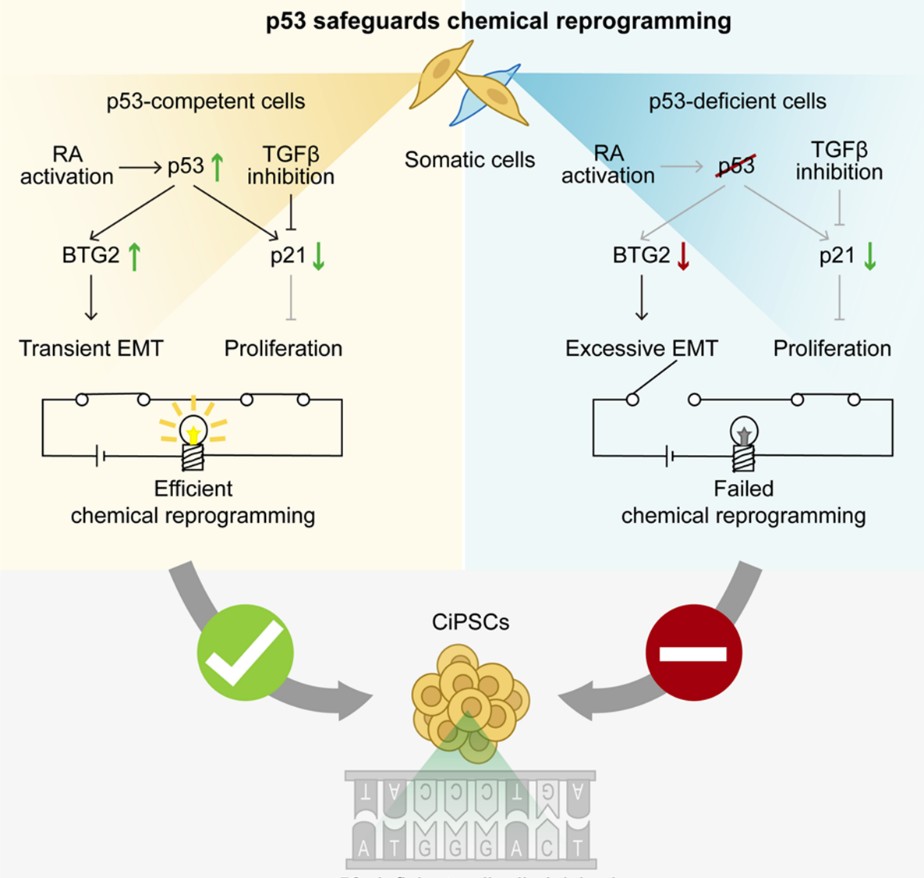
图2. 化学重编程中p53发挥关键保护作用
该研究实现了p53在肿瘤抑制与高效细胞重编程之间的平衡。在化学重编程过程中,p53作为质量控制因子,可有效清除重编程产物中p53缺陷及携带突变的细胞,从底层机制上确保了重编程来源的多能干细胞的安全性。
化学重编程在多个方面与转录因子重编程存在本质区别:1)化学重编程具备有序分阶段、动态可控的优势,以类似动物组织再生的机制逐步提升细胞可塑性;2)可精准调控p53网络,形成天然的安全保障;3)化学小分子以简便可控的方式灵活操纵细胞命运,易于干细胞的大规模制备与标准化生产。化学重编程技术在效率和普适性上得到了显著提高(Cell Stem Cell, 2023;Nat. Chem. Biol. , 2025),并成功应用于人外周血细胞(Cell Stem Cell, 2025)。2024年,基于化学重编程的人胰岛移植治疗实现了1型糖尿病的功能性治愈,患者恢复自主胰岛素分泌与血糖调控功能,摆脱胰岛素注射治疗(Cell, 2024),体现了该技术的临床应用前景。
综上,p53依赖的化学重编程策略,为安全、可控地调控细胞命运提供了全新路径。该研究是细胞命运调控理论的重要发现,有望推动再生医学的突破性发展,在细胞治疗、体内再生与延缓衰老等研究领域具有广阔应用前景。
北京大学成林、王杨璐、杨芷涵、曹靖宵、彭芳琪为该研究的共同第一作者。邓宏魁、北京大学孙仕成副研究员和成林博士是这一研究成果的共同通讯作者。北京大学关景洋研究员和李程教授为本研究提供了重要帮助。本工作获得了国家自然科学基金、国家重点研发计划、北京市自然科学基金、中国博士后科学基金等支持。
主要参考文献:
Guan et al. (2022). Chemical reprogramming of human somatic cells to pluripotent stem cells. Nature 605, 325—331.
Hou et al. (2013). Pluripotent stem cells induced from mouse somatic cells by small-molecule compounds. Science 341, 651—654.
Liuyang et al. (2023). Highly efficient and rapid generation of human pluripotent stem cells by chemical reprogramming. Cell Stem Cell 30, 450—459.
Peng et al. (2025). Chemical reprogramming of human blood cells to pluripotent stem cells. Cell Stem Cell 32, 1192—1199.
Wang et al. (2023). Chemical-induced epigenome resetting for regeneration program activation in human cells. Cell Reports 42, 112547.
Wang et al. (2024). Transplantation of chemically induced pluripotent stem-cell-derived islets under abdominal anterior rectus sheath in a type 1 diabetes patient. Cell 187, 6152—6164.
Wang et al. (2025). A rapid chemical reprogramming system to generate human pluripotent stem cells. Nature Chemical Biology 21, 1030—1038.
Zhao et al. (2008). Two supporting factors greatly improve the efficiency of human iPSC generation. Cell Stem Cell 3, 475—479.
Zhu et al. (2024). Generation of human expandable limb-bud-like progenitors via chemically induced dedifferentiation. Cell Stem Cell 31, 1732—1740.
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。














化学重编程和转录因子重编程区别这么大的吗?
这个发现确实颠覆了传统认知。
有点东西啊,之前一直以为p53就是阻碍没想到还能是保护。