文章导读
微生物细胞工厂明明初期产量惊人,传代几次后却莫名“罢工”?这并非操作失误,而是高产细胞在群体竞争中因代谢负担过重,被低产细胞“逆向淘汰”的必然结果。清华大学李春课题组给出的解法极为巧妙:利用生物传感器构建“生产依赖”型回路,让细胞不产即死。这一策略不仅让产量暴涨,更揭露了细胞群体内竟存在类似社会分工的协作机制,彻底颠覆了传统认知。
— 内容由好学术AI分析文章内容生成,仅供参考。
微生物细胞工厂为植物天然产物的绿色制造提供了重要途径,在医药、食品和精细化工等领域展现出巨大应用潜力。然而,在实际生产和长期培养过程中,工程菌株往往会出现“菌株退化”或“生产丢失”的问题。这是由于合成目标产物通常会增加细胞的代谢负担,高产细胞在群体竞争中反而处于劣势,最终被低产甚至不产的细胞取代,导致整体生产能力逐渐下降。这一问题长期制约着微生物细胞工厂在工业化生产中的稳定性与可靠性,因此,如何在细胞群体层面保持稳定并维持高产表型,成为合成生物学和代谢工程领域的重要挑战。
针对这一问题,清华大学化工系李春教授课题组合作提出了一种生物传感器驱动的生长-合成耦合策略,通过将产物合成与细胞生长优势相连接,使高产细胞能够在群体竞争中持续被富集,从而实现高产表型的稳定维持。
研究人员首先利用转录组分析比较了能够合成目标三萜产物甘草次酸(glycyrrhetinic acid, GA)的酿酒酵母工程菌株与对照菌株之间的转录响应差异,从中筛选出对GA具有显著响应的启动子元件PDR5。通过系统的启动子工程优化使该生物传感器的动态响应范围显著提升,从而开发了一个高灵敏度的GA生物传感系统。在此基础上,研究人员构建了一个“生产依赖”型调控回路,将GA生物传感器与酵母必需基因的表达相耦合,使细胞的生长能力依赖于目标产物的合成水平。通过这一策略,只有能够持续合成GA的细胞才能获得生长优势,而低产或不产的细胞则逐渐在群体竞争中被淘汰。经过定向进化后,该系统不仅显著提高了工程菌株的产量,还有效抑制了长期培养过程中常见的产量衰减现象,实现了细胞工厂生产表型的稳定化。
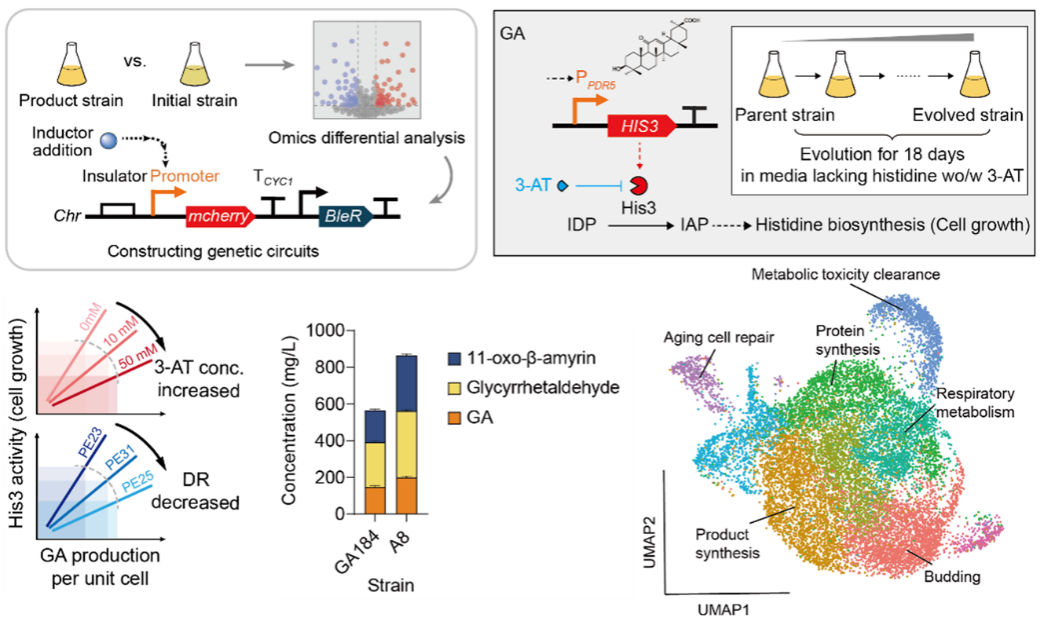
基于生物传感器构建“生产依赖”型调控回路,揭示酵母细胞工厂进化机制
为了进一步理解这一系统在细胞群体中的作用机制,研究人员利用单细胞RNA测序技术对生产能力进化与退化的菌株进行了深入解析。结果表明,在生长-合成耦合系统下,细胞群体并未趋于完全均一,而是形成了具有不同功能特征的细胞亚群。其中部分细胞主要承担快速增殖、抗逆功能,而另一部分细胞则高度表达三萜合成通路相关基因,成为主要的产物合成群体。这种类似“分工合作”的群体结构,使得细胞工厂能够在保持整体生长能力的同时维持较高的代谢生产效率。进一步结合单细胞转录组数据,研究人员还识别出若干在非生产细胞中高表达的“生产拮抗”基因,并通过基因工程改造进一步提升了GA等三萜化合物的合成水平。
该研究构建了一种从生物传感器挖掘、代谢耦合调控到单细胞解析优化的系统化策略,不仅为解决细胞工厂生产稳定性问题提供了新的技术路径,也揭示了工程微生物群体在高效代谢生产过程中的潜在分工机制。相关成果为未来通过群体工程与单细胞组学手段进一步优化微生物制造体系提供了重要理论基础和技术框架,对推动天然产物的可持续生物制造具有重要意义。
研究成果以“设计生物传感器依赖的耦合系统稳定细胞工厂的高合成表型”(Design of the biosensor-dependent coupling system stabilizes the high-synthesis phenotype of cell factory)为题,于4月13日发表于《自然·通讯》(Nature Communications)。
清华大学化工系教授李春与北京理工大学化学与化工学院副教授吕波为论文共同通讯作者,清华大学化工系助理研究员秦磊、天津大学2023届博士毕业生杨博、北京理工大学2023级博士生黄睿为论文共同第一作者。研究得到国家重点研发计划、中国自然科学基金的支持。
论文链接:
https://doi.org/10.1038/s41467-026-71801-5
供稿:化工系
编辑:李华山
审核:郭玲
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。



















清华这招让高产细胞必须干活才能活,有点意思啊。