研究提出结核肉芽肿胆固醇累积损伤免疫互作新机制
文章导读
你以为结核病难治只是因为细菌太狡猾?最新研究揭示了一个被长期忽略的"帮凶"——肉芽肿里堆积如山的胆固醇。中科院团队用空间转录组技术绘制了病灶的"活地图",发现一个惊人事实:结核杆菌竟能劫持巨噬细胞的溶酶体,让胆固醇把抗原呈递的"信号灯"MHC-II活活锁死在细胞内,直接切断CD4+ T细胞的免疫应答通道。更关键的是,小鼠实验证实只要恢复胆固醇稳态,抗结核能力就能显著增强。
— 内容由好学术AI分析文章内容生成,仅供参考。
以结核分枝杆菌感染所致结核病为代表的慢性肺部感染,其致病核心在于肺部区域免疫防御功能受损,为病原体长期存留创造了条件。结核分枝杆菌侵入肺部后,可诱导免疫细胞聚集形成肉芽肿。这类组织结构与肿瘤微环境具有相似特征,在决定感染转归中发挥关键作用。目前,针对结核肉芽肿的免疫特征及其内部免疫失稳的精细调控机制,仍有待系统阐明。
近日,中国科学院微生物研究所等研究团队绘制了结核肉芽肿的时空动态转录图谱,揭示了胆固醇累积介导肺部固有-适应性免疫互作界面受损的新机制。
研究团队采用空间转录组等前沿技术手段,系统绘制了结核肉芽肿中关键固有免疫细胞(巨噬细胞)与适应性免疫细胞(T细胞)的空间分布、转录特征及互作图谱,发现了其免疫异质性受组织病理类型(坏死性或非坏死性肉芽肿)、细胞空间定位(肉芽肿核心区或外周区)、特殊结构毗邻(多核巨细胞或三级淋巴结构)、病原持留状态(有或无结核分枝杆菌感染)及动态感染阶段等多重因素协同调控。
通过与肺部肿瘤微环境的对比分析,研究团队进一步鉴定出结核肉芽肿中MHC-II–CD4–TCR免疫信号轴受损的独特表型,并证实该表型与肉芽肿内脂质异常累积密切相关。机制研究表明,结核分枝杆菌可通过分枝菌酸等特定组分,诱导巨噬细胞溶酶体发生胆固醇累积,使MHC-II被滞留于溶酶体而无法定位至细胞膜表面呈递抗原,进而削弱CD4+ T细胞应答,最终导致肺部保护性免疫功能受损。小鼠实验证实,恢复肺部胆固醇稳态可显著增强宿主抗结核分枝杆菌能力。
该研究揭示了溶酶体胆固醇累积损伤固有-适应性免疫信号轴的关键机制,提出了靶向调控胆固醇代谢干预慢性感染的新策略,为结核病治疗与疫苗优化提供了新思路。
相关研究成果发表在《自然-微生物》(Nature Microbiology)上。研究得到国家卫生健康委员会等的支持。
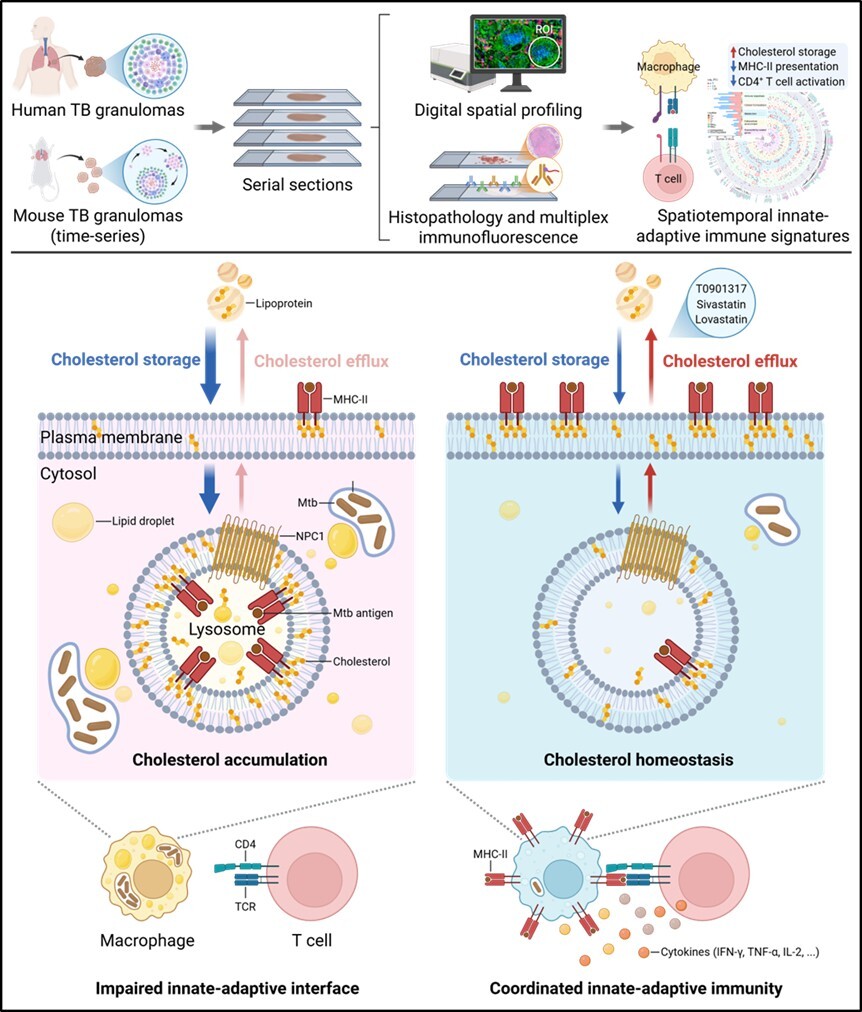
结核分枝杆菌诱导溶酶体胆固醇累积进而损害巨噬细胞与CD4+ T细胞相互作用的机制示意图
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。



















胆固醇这玩意儿居然能搞坏免疫?涨姿势了,以前只知道吃多了不好。