文章导读
你还在以为CAR-T是细胞治疗的唯一方向?当整个行业挤破头做体外基因改造时,一场静悄悄的革命已经转向体内——北大李湘盈团队最新研究发现,红细胞不只是氧气搬运工,还能当核酸快递员,精准把mRNA送进脾脏。我们扒完全文才意识到,传统脂质颗粒总卡在肝脏出不来,而这个新系统竟能绕开障碍,在脾脏原位生成CAR-髓系细胞,1/10剂量就实现更强抑瘤效果。更关键的是,这些细胞不是孤立作战,而是激活整个免疫军团协同攻击肿瘤。如果你以为这又是另一个递送优化,那你就错了——它真正颠覆的,是细胞治疗必须“体外回输”的铁律。这种模式,会不会成为下一代免疫疗法的胜负手?
— 内容由好学术AI分析文章内容生成,仅供参考。
2026年3月25日,北京大学生命科学学院李湘盈团队联合西湖大学高晓飞团队在Science Translational Medicine发表研究论文“In vivo Generation of CAR-Myeloid Cells through Erythrocyte-Mediated mRNA Delivery for Cancer Immunotherapy”,并入选当期封面(图1)。该研究提出了一种以红细胞为基础的mRNA递送新策略,能够将核酸精准输送至脾脏免疫细胞,并在体内直接诱导生成具备抗肿瘤活性的CAR-髓系细胞,为细胞治疗提供了一种不同于传统体外改造的实现路径。
图1 本文入选当期期刊封面图
当前主流的脂质纳米颗粒(LNP)递送体系在体内往往优先聚集于肝脏,这在一定程度上限制了其在免疫系统中的应用。针对这一瓶颈,研究团队将目光转向红细胞这一天然循环载体。红细胞具有良好的生物相容性和极低的免疫原性,同时在生命周期中与脾脏免疫系统存在持续互动。当红细胞发生衰老或结构变化时,会被脾脏中的吞噬细胞清除,这一过程为其进入免疫微环境提供了天然通道1,2。该研究利用这一特性,将mRNA包裹的纳米颗粒稳定固定在红细胞表面,构建了一种新型复合递送体系。体内分布结果显示,与传统LNP主要富集于肝脏不同³,mRNA-LNP-Ery优先在脾脏富集,并被髓系免疫细胞高效摄取,而在非靶组织中的分布明显降低,表现出良好的免疫器官选择性(图2)。
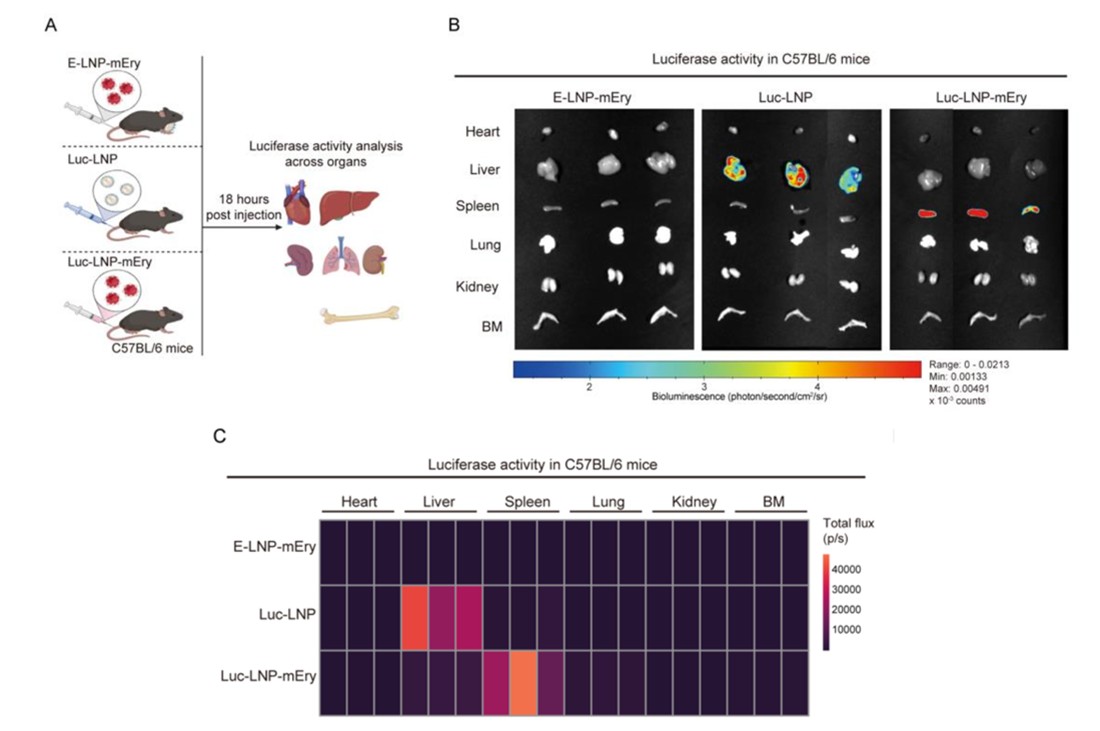
图2 mRNA-LNP-Ery高效靶向脾脏,实现mRNA递送
在细胞层面,该递送方式还带来了不同于传统路径的运输机制。常规LNP多通过内吞作用进入细胞,随后大量滞留在内体结构中,导致核酸难以释放进入胞质4。而红细胞介导的递送体系则更多依赖吞噬过程进入细胞,其胞内转运路径发生改变。成像分析表明,一部分mRNA可以在吞噬体成熟过程中提前释放,从而显著提升其进入胞质并参与蛋白翻译的效率。这一差异为提高核酸药物的表达效率提供了新思路。
在功能验证方面,研究团队进一步递送编码嵌合抗原受体(CAR)的mRNA,实现对体内髓系细胞的原位编程。在多种肿瘤模型中,包括免疫抑制程度较高的实体瘤模型,该策略均展现出明显的抑瘤效果,并显著延长动物生存时间。值得注意的是,与传统LNP递送相比,该方法在约1/10剂量下即可达到更优的治疗效果,同时系统性毒性较低,显示出较好的安全性。进一步研究发现,这一治疗效果高度依赖脾脏:在脾脏被移除或免疫系统受损的条件下,抗肿瘤作用明显减弱。转录组分析显示,体内生成的CAR-髓系细胞呈现免疫激活相关特征,并能够促进效应T细胞和NK细胞进入肿瘤组织,从而形成更强的免疫协同反应。
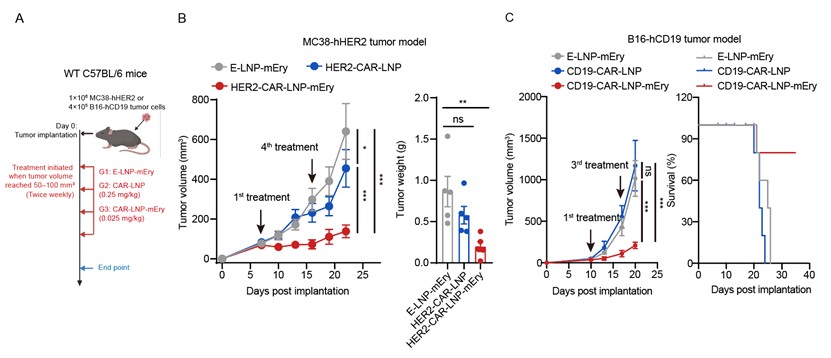
图3 CAR-LNP-Ery在体内生成CAR-髓系细胞并产生抗肿瘤作用。(A)CAR-LNP-Ery抗肿瘤实验流程示意图(B)在MC38-hHER2小鼠模型中,比较不同处理组的肿瘤生长曲线及肿瘤重量,评估抗肿瘤效果(C)在B16-hCD19小鼠模型中,比较不同处理组的肿瘤生长及生存情况
总体来看,该研究建立了一种利用红细胞实现核酸定向递送的新策略,并首次实现了在体内直接构建功能性CAR-髓系细胞。通过将递送系统与免疫细胞编程相结合,该工作拓展了细胞治疗的实现方式,为未来开发更高效、更安全的肿瘤免疫治疗手段提供了新的思路。与此同时,这一成果也进一步丰富了红细胞在生物医学领域中的应用潜力,从传统的运输功能拓展至精准递送与免疫调控平台。
李湘盈与高晓飞为本文共同通讯作者。西湖大学聂小千博士、刘悦华博士、姚星云及西湖生物宋玉婷博士为本文共同第一作者。该研究得到科技部、浙江省自然科学基金等的资助,并得到了细胞增殖与分化教育部重点实验室、北大–清华生命科学联合中心的支持。
参考文献:
1. Pivkin, I. V. et al. Biomechanics of red blood cells in human spleen and consequences for physiology and disease. Proc Natl Acad Sci U S A 113, 7804—7809 (2016). https://doi.org/10.1073/pnas.1606751113
2. Dao, M., MacDonald, I. & Asaro, R. J. Erythrocyte flow through the interendothelial slits of the splenic venous sinus. Biomech Model Mechanobiol 20, 2227—2245 (2021). https://doi.org/10.1007/s10237-021-01503-y
3. Rohner, E., Yang, R., Foo, K. S., Goedel, A. & Chien, K. R. Unlocking the promise of mRNA therapeutics. Nature Biotechnology 40, 1586—1600 (2022). https://doi.org/10.1038/s41587-022-01491-z
4. Gilleron, J. et al. Image-based analysis of lipid nanoparticle–mediated siRNA delivery, intracellular trafficking and endosomal escape. Nature Biotechnology 31, 638—646 (2013). https://doi.org/10.1038/nbt.2612
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。


















又是CAR又是髓系的,听着就复杂,真能上临床吗?
我之前做mRNA递送被肝富集坑惨了,这方法要是能推广就好了
刚看完实验数据,1/10剂量就起效,毒性还低,靠谱!
红细胞当快递员?有点意思,不过脾脏切除的人咋办🤔
这递送效率提升也太关键了吧,之前LNP卡在内体里根本出不来