文章导读
骨科植入物最大的隐患,往往不是材料不够硬,而是身体把它当成了“入侵者”。你或许以为 PEEK 材料力学优异就能一劳永逸,却不知它的“生物惰性”正导致无数患者术后遭遇炎症包裹与骨整合失败。当传统涂层还在试图强行粘合时,西安交大二附院团队发现了一个被忽视的真相:骨修复需要的不是单一刺激,而是一场精准的“免疫 - 成骨”时序接力。他们构建的双药递送系统,竟能像指挥家一样,先平息早期炎症风暴,再在后期精准激活成骨通路。这种让惰性材料“学会”与人体对话的仿生逻辑,究竟是如何在大段骨缺损修复中实现逆转的?
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,西安交大二附院骨科中心关节与足踝病区杨佩教授/马瑞副研究员团队与西安交通大学材料科学与工程学院李成新教授合作,在国际权威期刊《化学工程杂志》(《Chemical Engineering Journal》发表题为《仿生免疫-成骨时序调控:基于磺化聚醚醚酮表面PDA涂层双药递送系统的构建及其促进骨缺损修复的研究》(Biomimetic sequential immuno-osteogenic regulation via a dual-drug delivery system with PDA coating on sulfonated PEEK promotes bone defect repair)的创新研究成果。论文第一作者为西安交大二附院博士生吴紫萱和郭晓宇及医工交叉博士后马凯,通讯作者为西安交大二附院杨佩教授、马瑞副研究员及西安交通大学材料学院李成新教授。
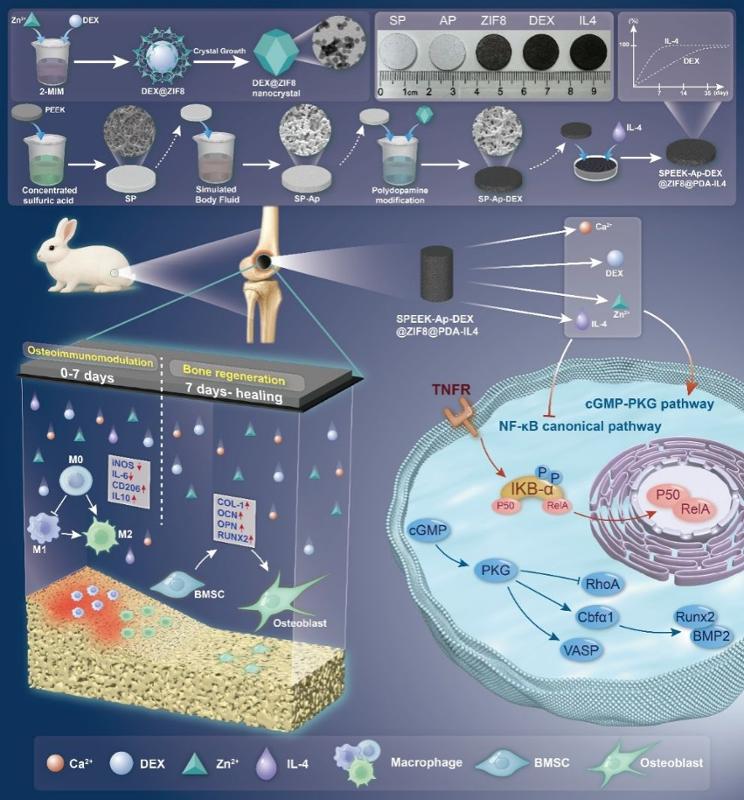
如何让PEEK材料从“生物惰性”变为“生物活性”?这是团队一直在攻克的难题。PEEK虽然力学性能优异,但它本身不具备促进骨再生的能力,植入后容易引发炎症反应,导致纤维包裹,最终影响植入物的长期稳定性。针对这一临床痛点,团队与材料学院李成新教授合作,提出了一种新的解决思路:通过表面涂层设计,让植入材料能够按照骨修复的生理节奏,分阶段发挥不同作用。
在磺化处理后的PEEK表面构建仿生磷灰石层,再利用聚多巴胺将搭载地塞米松的金属有机框架物ZIF-8纳米颗粒固定在材料上,同时吸附白细胞介素-4。这样就形成了一种具有时序释放功能的复合涂层,这种涂层的工作机制很简单:植入早期,白细胞介素-4快速释放,发挥免疫调节作用,促进巨噬细胞向抗炎表型转化,为后续骨再生创造有利的微环境。植入中后期,地塞米松和锌离子缓慢释放,持续促进成骨细胞分化,加速新骨形成。体外实验和兔股骨缺损模型证实,这种时序调控策略有效抑制了早期炎症反应,抑制NF-κB炎症通路、激活cGMP-PKG成骨通路,最终显著促进了新骨形成和骨整合。
临床医生从临床发现并提出问题,与工科专家发起医工交叉合作开发创新器械,最后再应用于临床,是外科临床医生做科研的方向之一。正是这种跨学科的碰撞与融合,让团队一步一个脚印,将生物惰性的PEEK逐步转化为具有免疫调控功能的活性植入平台。
该系列研究获得了国家自然科学基金、中央高校基本科研业务费及陕西省重点研发计划等项目的持续支持。目前,团队正聚焦于大动物模型验证和临床转化研究,为大段骨缺损、重度骨质疏松等复杂临床场景下的骨修复难题提供医工交叉解决方案。
论文链接:https://doi.org/10.1016/j.cej.2026.175076
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。



















这个涂层设计有点意思,早期抗炎后期成骨,思路挺巧妙的。
看不懂,太专业了😂