文章导读
面对“冷肿瘤”这块难啃的骨头,传统的免疫治疗往往束手无策,因为肿瘤内部的T细胞早已陷入“耗竭”休眠。清华团队这次没有走老路去外部“搬救兵”,而是设计了一种名为BiDT的分子“桥”,直接在肿瘤微环境内部重建了免疫突触。这种“原地激活”的策略不仅逆转了T细胞的死亡命运,更意外地发现了与PD-L1阻断剂的协同增效机制。当大家都以为免疫治疗已入瓶颈,这项研究是如何打破僵局,让那些“装睡”的T细胞重新杀敌的?
— 内容由好学术AI分析文章内容生成,仅供参考。
肿瘤免疫治疗的疗效很大程度上取决于肿瘤微环境内功能性T细胞的存在与活性。传统免疫学观点认为,T细胞的活化启动主要依赖于引流淋巴结中树突状细胞(DC细胞)的抗原呈递。然而,在肿瘤进展过程中,肿瘤浸润T细胞常呈现功能耗竭状态。目前,一个关键的科学问题尚未得到充分阐释:能否通过肿瘤微环境内DC细胞与耗竭T细胞之间功能性互作再次激活肿瘤内耗竭T细胞?这一问题的阐明对于开发靶向肿瘤微环境、逆转免疫抑制的新策略至关重要。
3月17日,清华大学基础医学院傅阳心教授和王文彦副研究员团队与重庆医科大学张旭浩副教授合作在《自然·通讯》(Nature Communications)发表题为“新型DC-T细胞衔接器BiDT重激活肿瘤浸润耗竭T细胞功能”(Reactivating exhausted tumor-infiltrating T cells by a bispecific DC-T cell engager in mice)的研究论文。研究创新性地设计了一种DC-T细胞的衔接器分子BiDT,成功实现了在肿瘤微环境内部直接重新激活耗竭的DC细胞和T细胞,为克服肿瘤免疫逃逸提供了全新策略。
该研究设计的双特异性分子可同时靶向耗竭CD8⁺ T细胞表面的抑制性受体TIM3与DC表面的I型干扰素受体。该分子在肿瘤微环境中发挥“分子桥”功能,一方面阻断T细胞的抑制性信号,另一方面向DC递送IFNα激活信号。这种物理性桥接在肿瘤局部重建了功能性的免疫突触,其核心机制在于:IFNα信号驱动DC活化并上调共刺激分子表达,进而为与其桥接的耗竭T细胞提供关键的活化信号。该信号轴可有效逆转T细胞凋亡,并恢复其IL-2响应与IFN-γ分泌等效应功能。
进一步的转化研究揭示了该策略与现有免疫检查点阻断疗法的协同潜力。研究发现,该疗法在激活DC的同时可诱导其上调PD-L1,而联合使用PD-L1阻断抗体可打破由此形成的代偿性免疫抑制反馈。在B16F10黑色素冷肿瘤模型中,联合治疗展现出显著的协同效应,为临床上治疗T细胞浸润匮乏的“冷肿瘤”提供了新的联合策略。
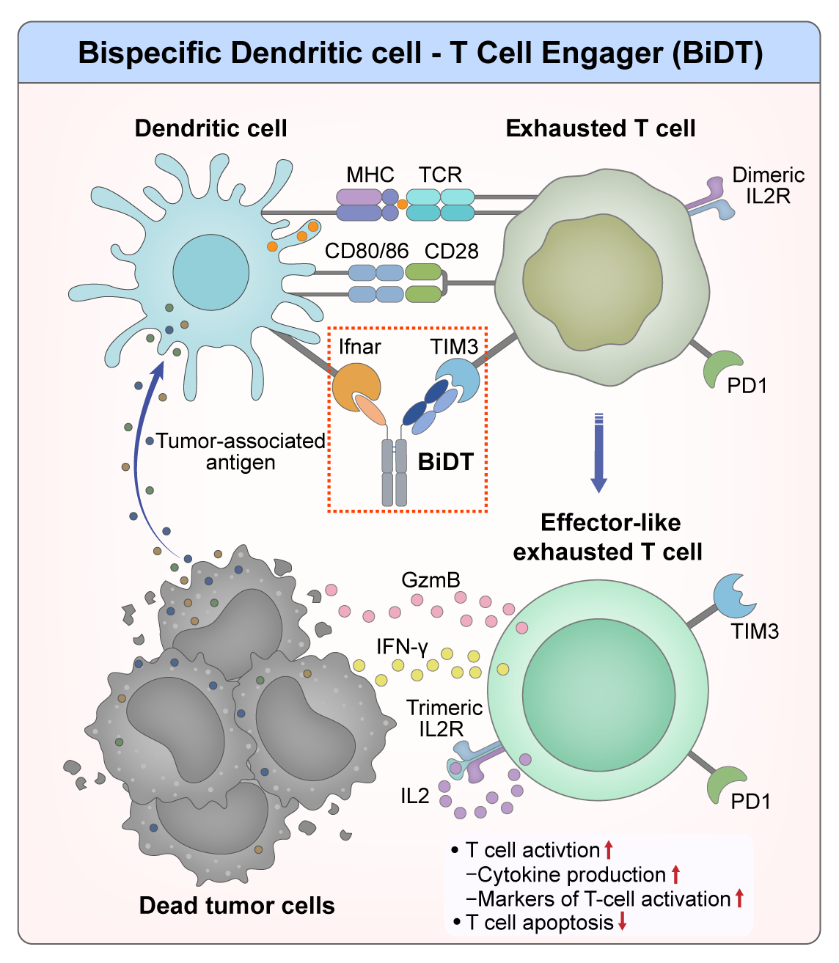
新型DC-T衔接器BiDT作用机制示意图
为克服IFNα系统给药的外周毒性,研究团队进一步开发了其肿瘤微环境激活的前体药物(Pro-BiDT)。该前药通过肿瘤富集的金属蛋白酶特异性切割释放活性,在临床前模型中实现了在维持抗肿瘤活性的同时显著降低全身毒性,从而提高了治疗指数。
综上所述,该研究不仅开发了一种能够精准干预肿瘤免疫微环境的新型衔接器分子,而且从机制上阐明了一条不依赖于外周淋巴细胞补充、直接发生于肿瘤内部的T细胞再活化新路径,为克服“冷肿瘤”的免疫治疗耐药性提供了新的思路与潜在的治疗策略。
重庆医科大学副教授张旭浩(清华大学基础医学院已出站博士后),清华大学基础医学院博士后高宇、2024级博士生胡文波为论文共同第一作者。清华大学基础医学院教授傅阳心、副研究员王文彦和张旭浩为论文通讯作者。研究得到中国科学院微生物所研究员朱明昭、广州国家实验室研究员彭华等的合作支持,并得到国家自然科学基金等的资助。
论文链接:
https://doi.org/10.1038/s41467-026-70876-4
供稿:基础医学院
编辑:李华山
审核:郭玲
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。


















冷肿瘤终于有招了?以前听说这种很难搞,要是能联合PD-L1效果稳住就神了。
小白求问,这个前药Pro-BiDT大概还要多久能上临床啊?
清华基础医学院这波可以啊,发了NC还搞了个前药设计,思路挺顺。
BiDT这玩意儿要是能避开全身毒性,那确实比传统放化疗香多了。
这名字起得挺玄乎,看描述好像是直接在肿瘤内部把T细胞“叫醒”?