脊灰疫苗研发取得进展
文章导读
你或许以为脊灰疫苗研发已经停滞不前,但中科院的这项突破正在颠覆传统疫苗的生产逻辑。当大多数疫苗还在依赖活病毒培养时,这项研究用酵母系统直接制备出热稳定型病毒样颗粒,不仅完全避开了活病毒的安全隐患,更实现了惊人的高产量和低成本。更关键的是,这种新型疫苗在小鼠实验中仅需1微克就能诱导高滴度中和抗体,而其背后的冷冻电镜结构解析揭示了抗原稳定性的核心机制。但真正决定这种疫苗能否替代传统方案的关键,在于那个被精准定量检测的D-抗原——这个隐藏在产品质量控制环节的细节,究竟会成为新一代疫苗的制胜法宝还是潜在瓶颈?
— 内容由好学术AI分析文章内容生成,仅供参考。
脊髓灰质炎是由脊髓灰质炎病毒(PV)引发的急性传染病。当前,亟待研发不使用活病毒的新一代脊灰疫苗。
近日,中国科学院分子细胞科学卓越创新中心团队等,利用酵母重组表达系统,制备了1型脊髓灰质炎病毒(PV1)热稳定型病毒样颗粒(VLP)候选疫苗,通过冷冻电镜系统,解析了其组装机制及D—抗原性的结构基础。
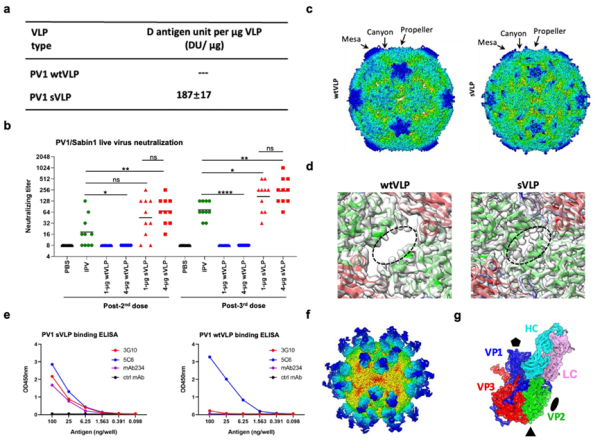
在毕赤酵母中,研究团队制备出PV1野生型病毒样颗粒(wtVLP),以及基于热稳定突变毒株SC7的稳定型颗粒(sVLP)。实验显示,其D—抗原含量较高、热稳定性优异。小鼠免疫实验中,1微克sVLP可诱导高滴度中和抗体。该酵母表达系统产量高,成本优势与产业化前景显著。
团队运用冷冻电镜技术,解析了野生型与稳定型颗粒的高分辨率三维结构。结果显示:野生型VLP呈扩张构象,二重轴通道开放,缺乏D—抗原性;含7个热稳定性突变的sVLP呈紧密构象,二重轴通道封闭,关键抗原结构稳定有序。结构比对显示,sVLP与已报道的SC6b D—抗原颗粒一致,在原子水平揭示了热稳定突变锁定D—抗原构象的机制,为设计高稳定性脊灰VLP疫苗提供了依据。
团队在免疫小鼠中筛选出特异性识别D—抗原的中和性单克隆抗体3G10。结构分析显示,其结合于病毒表面“峡谷”区,与VP1的BC/GH环及VP2 EF环形成氢键和盐桥网络。在D—抗原向C—抗原构象转变过程中,该表位结构松散化破坏了抗体结合界面,使其具备高度特异性。3G10结合表位与病毒受体PVR结合位点高度重叠,通过空间位阻阻断病毒—受体结合,实现中和作用。团队以此建立了以3G10为核心的双抗体夹心检测法,实现了D—抗原的精准定量,为疫苗质量控制提供了工具。
该研究阐明了酵母表达脊髓灰质炎病毒样颗粒的组装机制及D—抗原性的结构基础,构建了兼具高产量、高稳定性和强免疫原性的候选疫苗以及配套的抗原检测体系,为新一代脊灰疫苗开发奠定了基础。
相关研究成果在线发表在NPJ Vaccines上。研究工作得到国家自然科学基金委员会、科学技术部、中国科学院等的支持。
脊灰疫苗研发取得进展
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。














D—抗原构象这玩意儿终于搞明白了,看来离无活毒疫苗不远了🤔
又是冷冻电镜又是单抗检测……技术堆得挺满,但啥时候能用上?
之前带娃打脊灰疫苗还担心副作用,希望这个新方案快点落地。
小鼠实验才1微克就有高滴度抗体?人用剂量会不会差很多?
热稳定突变锁定构象……听着就靠谱,比以前那些容易失效的强多了。
酵母表达系统产量高?那成本能降多少啊,求具体数据。
这疫苗要是真不用活病毒就太好了,小时候打针可遭罪了。