文章导读
你体内的肿瘤细胞,可能正等着被“点燃”——不是用化疗,而是用一场精准控制的免疫风暴。大多数癌症免疫疗法还在被动唤醒T细胞时,北大团队已经找到了主动制造“自体疫苗”的钥匙:通过纳米佐剂精准触发肿瘤细胞焦亡,让死亡细胞自己变成抗原库。我们发现,这种原位生成的焦亡囊泡,不仅能同时释放肿瘤抗原和免疫信号,还能在微环境中形成持续激活树突状细胞的“热点”。小鼠实验中甚至实现了转移灶完全消退与长期免疫记忆。但问题来了——既然人体也有早期内吞体,为什么现有疗法没能复制这一效果?答案藏在一个连多数实验室都忽略的时空窗口里。
— 内容由好学术AI分析文章内容生成,仅供参考。
2026年3月3日,药学院天然药物及仿生药物全国重点实验室汪贻广教授、张强院士、陈斌龙副研究员团队在《自然·材料学》(Nature Materials)上发表了题为“In situ-generated vaccine-like pyroptosome for personalized cancer immunotherapy”的研究工作。

论文截图
原位肿瘤疫苗通过直接在肿瘤内激活免疫反应,将患者自身肿瘤转化为“个性化疫苗”,为精准免疫治疗提供了新策略。然而,其疗效仍受到癌症–免疫循环(CIC)各环节协同效率不足的限制。肿瘤细胞的死亡方式及其免疫原性,是决定免疫应答强度的核心因素。与相对“免疫沉默”的细胞凋亡不同,焦亡等裂解型程序性细胞死亡能够大量释放肿瘤抗原和炎性信号,从而显著增强抗肿瘤免疫反应。但现有焦亡诱导策略缺乏精准的时空调控,易引发炎症失控和脱靶损伤,成为制约其临床转化的重要挑战。
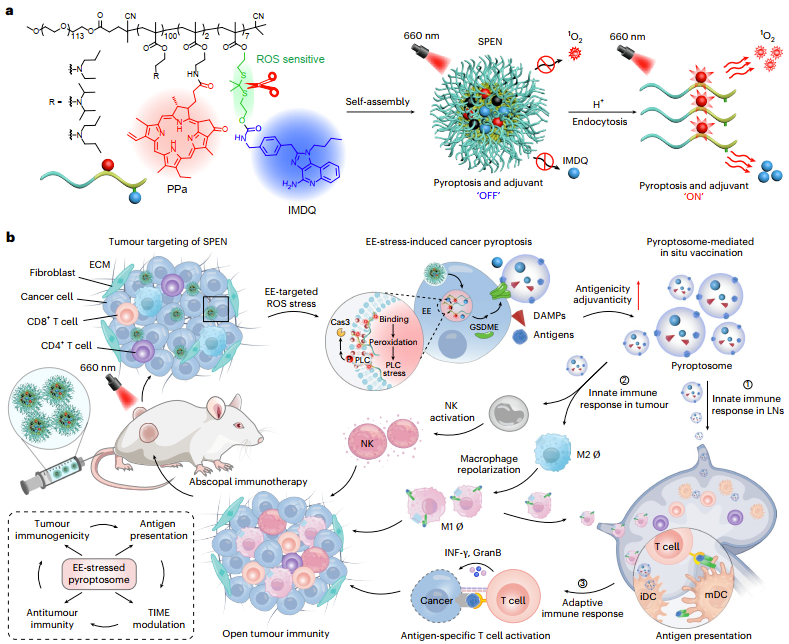
在前期研究中,该研究团队在国际上率先建立了内吞细胞器精准靶向递送技术,创新性发现了细胞内吞转运过程时空操控纳米药物的生物学效应和抗肿瘤疗效,并系统阐明了早期内吞体靶向的纳米药物能特异性诱导高免疫原性肿瘤细胞焦亡(Nat. Nanotechnol.,2022,17,788—798)。在此基础上,研究团队基于内吞细胞器精准靶向递送技术进一步构建了焦亡激活型纳米佐剂(SPEN),能够精准作用于肿瘤细胞早期内吞体膜,高效诱导肿瘤细胞焦亡,并原位释放TLR7/8免疫激动剂,在“正确的时间”和“正确的位置”建立强效的免疫激活微环境。
研究发现,通过靶向早期内吞体膜诱导焦亡,可以产生富含肿瘤抗原和免疫激动信号的焦亡囊泡(pyroptosome),这些囊泡如同“原位生成的自体疫苗”,能够高效激活树突状细胞和T细胞反应,放大抗肿瘤免疫。在自发乳腺癌等多种小鼠肿瘤模型中,该策略实现了原发肿瘤与转移灶的完全消退,并建立了持久的免疫记忆,在再次肿瘤挑战时表现出显著保护效果。这一研究不仅揭示了焦亡囊泡介导免疫启动的分子机制,也为构建可精准调控的个性化免疫治疗提供了理论框架和工程化设计思路。
小鼠肿瘤模型示意图
本研究的第一完成单位是北京大学药学院天然药物及仿生药物全国重点实验室。汪贻广、张强和陈斌龙为该论文的通讯作者。陈斌龙和万方劼博士为论文的共同第一作者。天然药物及仿生药物全国重点实验室仪器平台和北京大学医学部医药卫生分析中心的各位老师为该研究提供了重要帮助。该工作得到国家自然科学基金、教育部基础学科和交叉学科突破计划以及北京市自然科学基金等项目资助。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。















这个SPEN到底是怎么精准定位到内吞体的?想了解细节
好像又要掀起一波免疫治疗的热潮
焦亡的副作用会不会影响正常细胞?
之前实验室里也玩过类似的纳米递送,超麻烦
我觉得如果能控制炎症,那真的能救命
这技术听起来有点科幻😂