文章导读
你以为胚胎发育的关键在于基因组激活,但清华与浙大的最新研究告诉你,真正决定生命起跑线的其实是受精后第一次DNA复制。当90%的研究聚焦在表观遗传时,这个团队发现了被长期忽略的母源因子THAP1——它像精准的节拍器,通过调控dNTP合成来控制胚胎第一个细胞周期。缺失这个因子的胚胎会卡在1-2细胞阶段,就像发条突然停摆。更惊人的是,只需在合子中补充一个下游基因,就能让濒临停滞的胚胎恢复发育节奏。这个发现不仅改写了发育生物学教科书,更揭示了那些不明原因的不孕症背后可能藏着的真相——你是否想过,生命的第一次分裂失败,可能源于最基础的核苷酸供给不足?
— 内容由好学术AI分析文章内容生成,仅供参考。
在哺乳动物早期发育中,卵母细胞在成熟前会积累大量母源蛋白质与RNA,为受精后“母源-合子转变”(Maternal-to-Zygotic Transition, MZT)及随后发生的合子基因组激活(Zygotic genome activation, ZGA)提供基础。母源效应基因(Maternal Effect Genes, MEGs)在卵子中表达和积累,但在卵子成熟阶段不一定具有功能,而在受精后胚胎发育过程中则发挥关键作用。之前发现的母源效应基因多与表观遗传调控或RNA代谢相关。早期胚胎的第一次DNA复制通常发生在基因组激活之前,因此母源因子对于胚胎第一次DNA复制至关重要。
2月23日,清华大学生命学院颉伟教授团队与浙江大学医学院(医学遗传与发育研究院)嵇姝妍教授团队合作,以“母源效应因子THAP1通过Rrm1调节小鼠早期胚胎的第一个细胞周期”(THAP1 is a maternal effect factor required for the first cell cycle via Rrm1 in early mouse embryos)为题,在《欧洲分子生物学组织报告》(EMBO Reports)上发表研究论文。研究发现,转录因子THAP1在卵母细胞中表达并激活包括Rrm1在内的少数但关键的基因。RRM1参与dNTP合成,其在卵子中的积累保证了早期胚胎在受精后第一次DNA复制的正常进行。当母源THAP1缺失时,胚胎1细胞DNA复制进程显著延迟并出现1–2细胞期延缓和阻滞,同时伴随ZGA缺陷,最终导致雌鼠生育力严重下降。
THAP1属于Thanatos相关蛋白家族,是含THAP结构域的转录因子。在人类中,THAP1基因突变会引发一种神经系统运动障碍疾病肌张力障碍6型(DYT6)。相较于分化的组织,THAP1蛋白在卵子和着床前胚胎中表达很高,但其在早期胚胎发育中的具体功能仍不清楚。围绕这一问题,研究团队构建了卵母细胞特异性Thap1母源敲除模型。结果显示,母源Thap1缺失对卵母细胞发育和成熟并无显著影响,但受精后胚胎从1细胞向2细胞的发育进程明显延迟,许多胚胎停滞于1–2细胞阶段,并伴随ZGA缺陷,最终造成雌鼠生育力显著下降。
为解析其分子基础,研究团队结合转录组分析发现,Thap1缺失会导致卵母细胞中一小部分基因表达下调,其中包括编码核糖核苷酸还原酶亚基的Rrm1。RRM1参与dNTP合成,是DNA复制所必需的关键环节。为证明Thap1敲除对dNTP有影响,研究团队采用优化的无标记HPLC-MS策略,绘制了覆盖卵母细胞生长到受精后早期合子的代谢动态图谱。在母源Thap1缺失背景下,早期阶段dNTP供给受到影响,进而导致1细胞期胚胎S期退出延迟、DNA损伤增加以及细胞周期检查点持续激活,最终引起1细胞向2细胞的发育异常。为进一步证明Rrm1与dNTP直接影响胚胎发育,研究团队通过在合子中过表达Rrm1,能够显著改善母源Thap1缺失胚胎的发育进程,使2细胞进程与ZGA几乎得到完全恢复;补充Rrm1催化产物(dNDPs)亦可对相关缺陷产生一定程度缓解。上述结果共同支持“Thap1–Rrm1-dNTP供给”在受精后第一个细胞周期中的关键作用。
综上,研究将转录因子THAP1确立为小鼠早期发育过程中的母源效应因子之一,揭示其通过调控核苷酸代谢相关基因表达保障生命中第一次DNA复制。
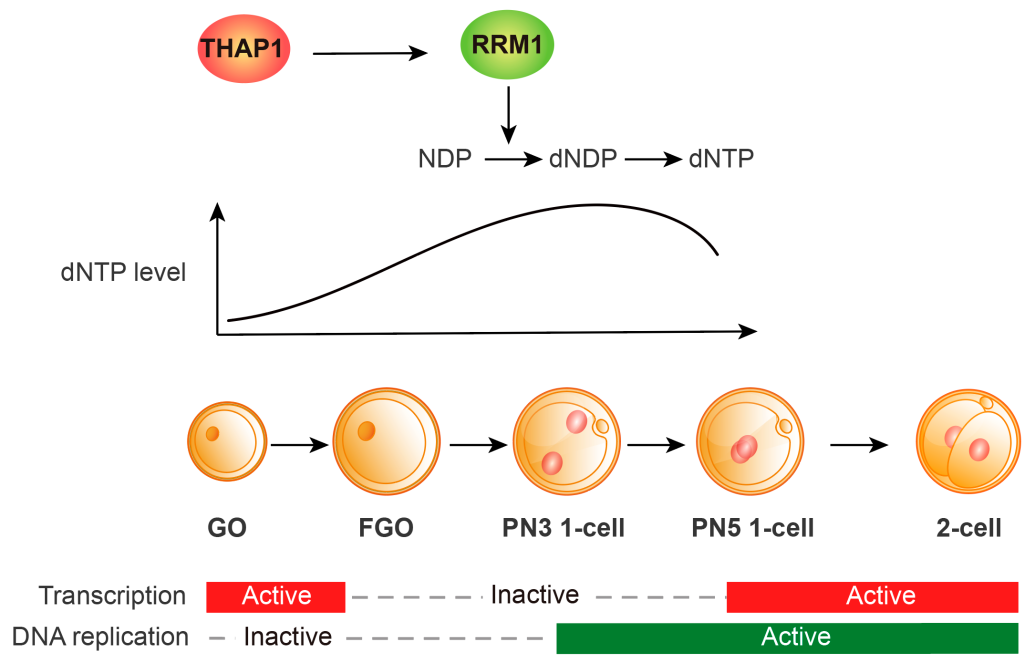
THAP1通过调控下游基因Rrm1转录,保障受精后第一个细胞周期所需dNTP供应,支持1细胞向2细胞转变及合子基因组激活(ZGA)
清华大学生命学院教授颉伟与浙江大学医学院(医学遗传与发育研究院)教授嵇姝妍(原颉伟组博士后)为论文通讯作者;清华大学生命学院2024届博士生毕业生范强、北京大学PTN项目2020级博士生吴希、清华-北大生命科学联合中心博士后党燕娜为论文共同第一作者。研究得到新基石基金、清华大学实验动物中心和清华大学生物计算中心的支持,并得到科技部重点研发计划、国家自然科学基金委、清华-北大生命科学联合中心等的经费支持。
论文链接:
https://doi.org/10.1038/s44319-026-00712-9
供稿:生命学院
编辑:李华山
审核:郭玲
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。














论文说“少数但关键基因”,结果就揪出Rrm1一个?有点悬啊。
又是HPLC-MS测代谢,现在发育生物学都卷到这程度了?
合子还没激活就得靠卵子里存的蛋白,压力全给母源了。
之前做胚胎实验时也遇到过1细胞阻滞,说不定就是类似机制。
THAP1在人里突变导致肌张力障碍,小鼠模型这结果有点意思🤔
dNTP不够直接拖垮第一次复制,难怪生育力暴跌。
Rrm1过表达能救回来?这通路挺关键啊。
母源THAP1缺失居然卡在1-2细胞,这瓶颈太致命了。