高通量核酸适体筛选与动力学分析平台成功开发
文章导读
你是否还在为找不到疾病的精准治疗靶点而困扰?中国科学院杭州医学研究所成功开发全球首个集高通量筛选与动力学分析于一体的SPARK-seq平台,突破性地实现“靶点发现”与“分子配对”同步完成。通过CRISPR编辑、单细胞测序与智能算法的三重结合,该技术如同布下一张“智能渔网”,能在海量分子中精准捕获特异性结合的核酸适体,为三阴性乳腺癌等缺乏明确靶点的肿瘤治疗带来全新希望。这不仅是方法的升级,更是一场从“大海捞针”到“智能制钥”的范式革命。
— 内容由好学术AI分析文章内容生成,仅供参考。
2026年1月1日,中国科学院杭州医学研究所构建了全球首个融合单细胞分辨率与高通量测序的核酸适体筛选与动力学分析平台——SPARK-seq,为精准分子识别、靶标发现及药物递送等领域提供了全新的研究工具与思路。
三阴性乳腺癌因其细胞表面缺乏类似HER2那样明确的药物作用靶点,导致许多特效药“无的放矢”,使临床治疗面临巨大挑战。
研究人员需要在根本上实现“双突破”——既要为这类疾病快速找到关键靶点,又要定制精准的治疗方案。传统寻找新药物靶点(“目标”)和对应治疗分子(“钥匙”)的方法效率低下,如同“大海捞针”。
SPARK-seq相当于布下了一张“智能渔网”,其工作流程分为三步。第一步,利用CRISPR基因编辑技术,对大量癌细胞进行“微创手术”,使其表面不同的膜蛋白功能逐一缺失;同时引入包含海量候选分子的核酸适体库。第二步,借助单细胞测序技术,为每个细胞拍摄“高清全景照”,同步捕获关键信息。第三步,通过开发新的算法和大数据分析,在海量数据中直接找出那些只牢牢结合在有癌变特征“目标”上的“钥匙”,并量化其结合的牢固程度。
这意味着,研究人员能在闭环系统中,同步发现新的疾病关键靶点,并获得能精准作用于该靶点的潜在治疗工具——核酸适配体,实现了“既发现锁,又配好钥匙”的一体化突破。SPARK-seq的研发,使得高效、规模化地发现与优化靶向分子成为可能,为生物医学领域建立了快速研发平台。
这一研究为三阴性乳腺癌等肿瘤带来了新的治疗希望,开创了强大的原创研发模式。未来或许能够像查询字典一样,快速锁定目标,并定制专属的“特效钥匙”。
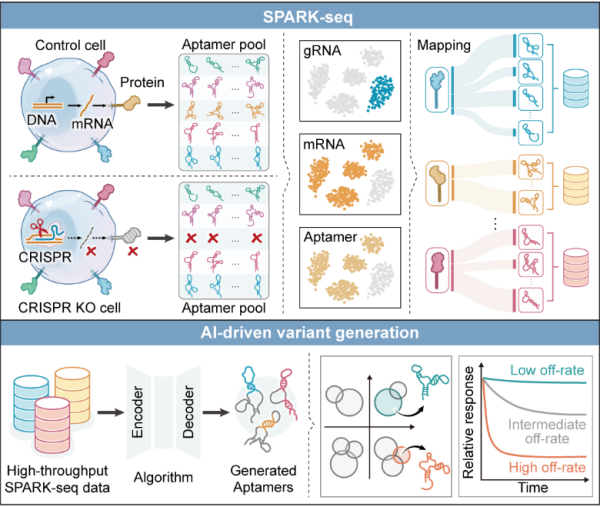
SPARK-seq平台用于核酸适体发现和变体设计
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。


















这步“微创手术”具体怎么控制脱靶率的,求细节!
查字典式找药?要是真这么容易就好了…hhh
又是标题党吧?说白了不还是测序套壳,有啥本质突破?
前几天刚读到适体库建库的坑,这里居然一步到位了,羡慕。
我搞生物信息的,想问下他们用的什么比对算法,BWA还是自研的?
单细胞+高通量双杀,这算法怕不是得跑断服务器?
之前看靶点筛选都得耗几个月,这效率直接起飞了吧?
感觉像给细胞做CT,还能顺便配钥匙,绝了 👍
这平台听着挺神的,真能搞定三阴性乳腺癌?