中山大学颜光美梁剑开团队鉴定G蛋白偶联受体TPRA1作为溶瘤病毒M1新型受体
文章导读
溶瘤病毒M1为何能精准“锁定”癌细胞?中山大学颜光美、梁剑开团队揭晓关键答案:首次发现G蛋白偶联受体TPRA1是M1病毒的新型功能受体!研究团队通过CRISPR-Cas9筛选技术,揭示TPRA1不仅介导病毒入侵,其表达水平还与治疗效果显著相关,有望成为指导临床精准用药的生物标志物。这一突破为破解肿瘤“试错式治疗”困局提供新路径,相关成果已发表于《Advanced Science》。
— 内容由好学术AI分析文章内容生成,仅供参考。
(通讯员张玉琦) 溶瘤病毒作为一种新兴的肿瘤治疗策略,能够选择性感染并杀伤肿瘤细胞,同时激活机体的抗肿瘤免疫反应,展现出广阔的临床应用前景。在这一过程中,病毒受体作为介导病毒入侵的关键分子,不仅决定病毒的组织嗜性和感染效率,也深刻影响溶瘤病毒疗法的靶向性与总体抗肿瘤效应。
近日,中山大学中山医学院颜光美梁剑开团队在该领域取得重要突破。研究通过膜蛋白CRISPR-Cas9筛选系统,首次鉴定G蛋白偶联受体TPRA1为溶瘤病毒M1的新型受体及疗效预测生物标志物。相关成果发布于期刊《Advanced Science》(《先进科学》)。
恶性肿瘤以其高度异质性和有限的治疗时间窗,长期被视为精准医疗领域最具挑战性的疾病类型之一。然而,目前多数抗肿瘤治疗方案仍停留在“试错式治疗”阶段,疗效差异显著且难以预测。要实现从“试错”到“精准”的范式转变,关键在于找到能够准确预测药物疗效的生物标志物。
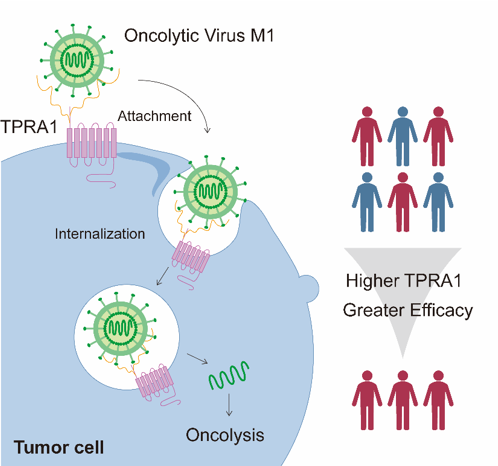
研究表明,TPRA1通过其胞外域的糖基化结构结合M1病毒颗粒,并借助胞内域介导的细胞膜-内体穿梭功能促进病毒内吞,从而显著提升M1病毒的感染效率和抗肿瘤效应。在肿瘤细胞系、动物模型及临床样本中,TPRA1的表达水平与M1病毒的抗肿瘤效应均呈现显著正相关。该研究不仅阐明了TPRA1作为M1病毒新受体及其分子机制,同时为M1病毒的临床精准应用提供了关键的功能性生物标志物。
中山医学院博士后胡琳翊为论文第一作者,中山医学院梁剑开副教授与蔡静副教授为共同通讯作者。该研究获得了国家自然科学基金、广东省自然科学基金等项目的资助。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...