文章导读
为何结直肠癌免疫疗法对多数患者效果有限?武汉大学江从庆、张金方与哈佛医学院魏文毅团队重磅揭秘:肿瘤细胞竟通过高表达ChREBP蛋白,疯狂掠夺胆碱并分泌趋化因子,将免疫卫士巨噬细胞"策反"为免疫抑制帮凶!研究发现,这种胆碱争夺战直接掐断巨噬细胞的cGAS-STING防御通路,导致癌细胞成功逃避免疫攻击。更关键的是,靶向抑制ChREBP有望打破免疫逃逸魔咒,为微卫星稳定型结直肠癌患者点燃新希望——这项发表于《癌症研究》的突破,或将彻底改写免疫治疗困局。
— 内容由好学术AI分析文章内容生成,仅供参考。
(通讯员仲南)9月5日,肿瘤学研究领域国际权威杂志《癌症研究》(Cancer Research, IF: 16.6)在线发表了由武汉大学中南医院结直肠肛门外科江从庆教授团队、武汉大学医学研究院张金方教授课题组、哈佛医学院魏文毅教授最新研究论文,题为“ChREBP-Mediated Choline Deprivation and Chemokine Secretion Shape Tumor-Associated Macrophages to Promote Immune Evasion”。中南医院结直肠肛门外科博士后赵健宏、陈保祥、博士研究生邓艳容与武汉大学中南医院樊利芳医生为论文共同第一作者,江从庆教授、张金方教授、魏文毅教授和解萧宇副研究员为论文的共同通讯作者,武汉大学中南医院为第一通讯单位。
癌症免疫疗法的显著成功为肿瘤治疗开辟了新途径。然而,仅有少数患者能够从中显著获益并实现长期临床应答。大部分的结直肠癌患者表现为微卫星稳定型,免疫检查点阻断(ICB)的临床疗效较为有限。
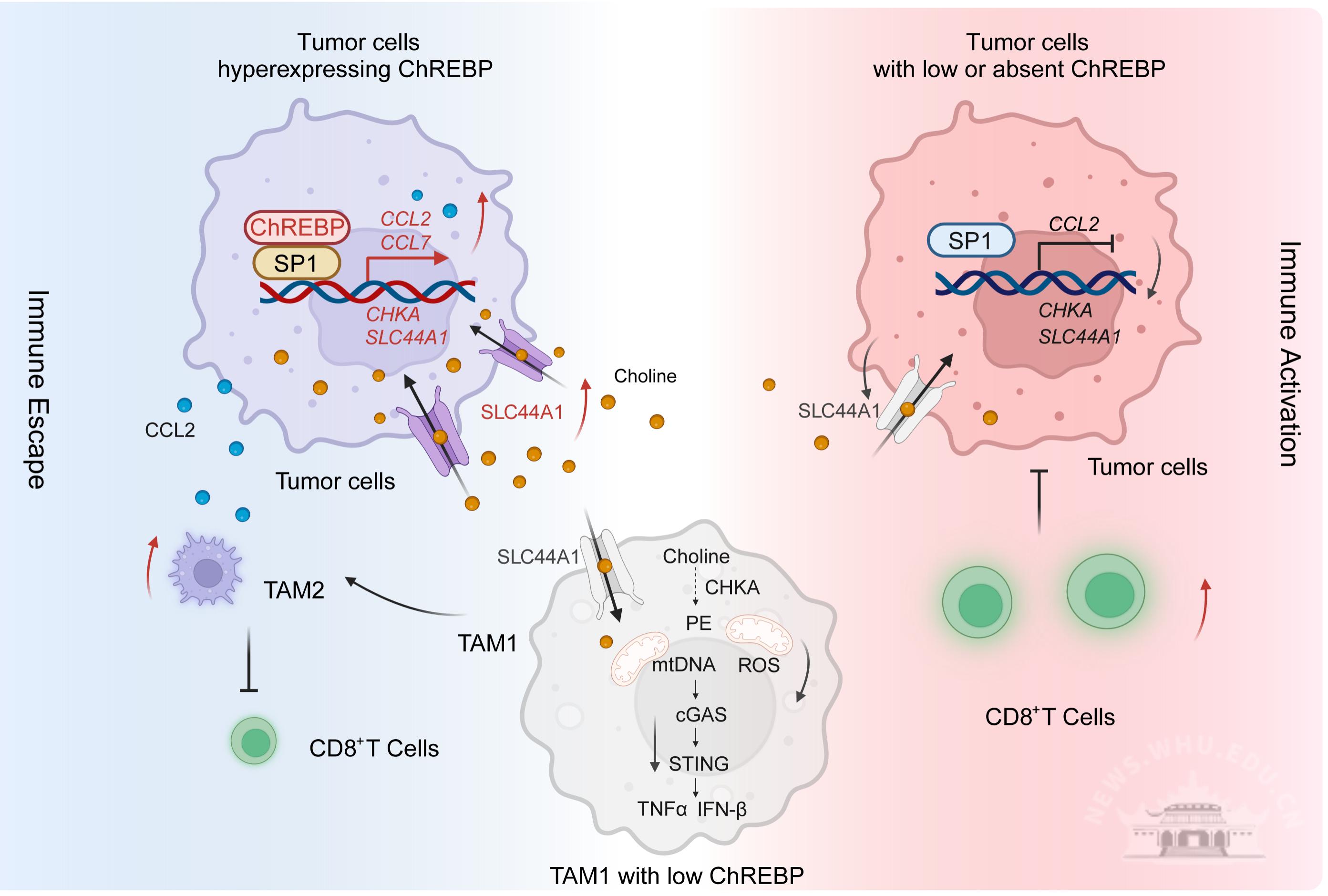
研究发现,碳水化合物反应元件结合蛋白(ChREBP)介导的胆碱剥夺可诱导肿瘤相关巨噬细胞(TAMs)重编程,并维持免疫抑制性肿瘤微环境(TME)。肿瘤细胞高表达ChREBP促进趋化因子CCL2、CCL7及胆碱转运蛋白SLC44A1的表达,诱导了TAMs肿瘤浸润。此外,高表达SLC44A1的肿瘤细胞在与TAM1的胆碱竞争中获胜,抑制了后者cGAS-STING通路激活,促使其重编程为M2样免疫抑制表型并诱导结直肠癌免疫逃逸。
该项研究发现了ChREBP介导的胆碱剥夺与趋化因子分泌重塑TAMs促进结直肠癌免疫逃逸的新机制,提示靶向抑制ChREBP可能成为提高ICB疗效的一种潜在治疗策略。
原文链接:https://doi.org/10.1158/0008-5472.CAN-25-0235
(编辑:肖珊)
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...