研究揭示具核梭杆菌黏附宿主细胞动态调控机制
文章导读
你是否想过,细菌竟能像“分子魔术贴”一样精准黏附癌细胞?具核梭杆菌正是通过这种神秘机制,在结直肠癌患者肠道中大肆定植,并抑制免疫反应。中国科学院微生物研究所联合仁济医院,首次在原子层面揭开这一过程的动态调控之谜:其黏附素CbpF以三聚体形式与癌细胞表面CEACAM1/5受体结合,形成类似“毛面与钩面”的可调节“粘扣”结构,既能在外力下稳固吸附,又能灵活脱离。这项发表于PNAS的研究不仅揭示了病原菌促癌的关键一步,更为抗癌与抗菌双效药物开发提供了全新靶点。
— 内容由好学术AI分析文章内容生成,仅供参考。
病原菌表面粘附素通过特异性分子,识别介导病原体与宿主的紧密接触,并在感染过程中呈现动态调控特征。然而,关于细菌-宿主界面粘附强度的动态调控机制尚不明确。
具核梭杆菌是在结直肠癌患者肠道中显著富集的厌氧菌,可通过黏附素CbpF特异性结合癌细胞表面的高表达的CEACAM1和CEACAM5,其中CEACAM1激活后,还会导致免疫细胞活性受抑制。因此,阐明CbpF与CEACAM1和CEACAM5相互作用的机制,对开发针对细菌促进肿瘤发生的靶向疗法具有重要意义。
中国科学院微生物研究所与上海交通大学医学院附属仁济医院合作,从原子层面解析了具核梭杆菌CbpF与受体CEACAM1和CEACAM5结合的关键机制。
研究团队运用冷冻电镜技术,解析了CbpF分别与受体CEACAM1和CEACAM5结合的高分辨率结构。在复合物结构中,CbpF以三聚体形式组装,形成对称的3:3结合模式。同时,研究还观察到两个CbpF三聚体与一个处于二聚体状态的受体分子相结合的复合物颗粒。
基于这一发现,科研团队提出了“粘扣”模型,即高度灵活的CbpF蛋白充当“毛面”,通过多结合位点与宿主受体“钩面”相互作用,从而建立起紧密黏附。该机制可能使细菌能够在机械应力作用下灵活调节黏附强度,在需要时牢牢黏附,在必要时轻松脱离来适应复杂的生理环境。
上述研究深化了对具核梭杆菌在肿瘤组织中定植以及免疫抑制机制的理解,为开发新型抗肿瘤和抗菌药物提供了关键靶点。
相关研究成果发表在《美国国家科学院院刊》(PNAS)上。
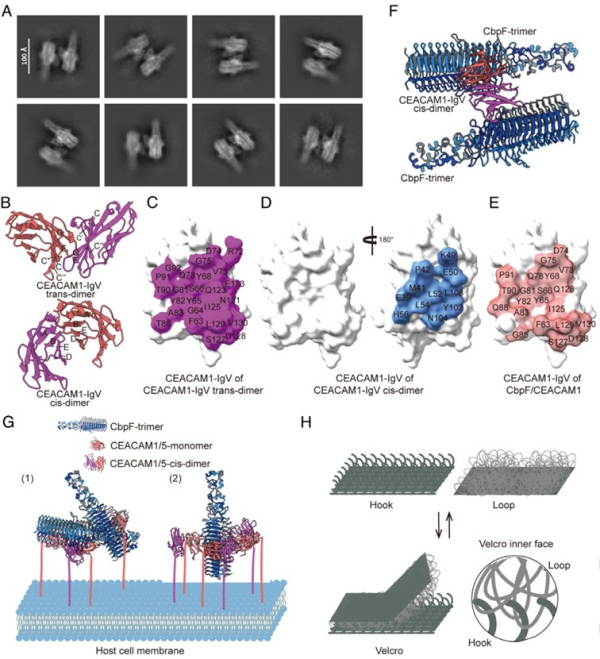
CbpF与受体CEACAM1和CEACAM5结合的“粘扣”模型
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...