文章导读
胺类分子本是药物合成的基石,却为何难以变身C-C键构建高手?南京大学陆红健团队颠覆传统认知,首创无金属参与的脱胺Giese反应!仅用市售DPPH试剂,10分钟内将廉价伯胺“一键转化”为烷基自由基,实现C-N到C-C键的华丽转身。突破性在于:无需昂贵金属催化剂,兼容桥环分子、氨基酸甚至完整药物分子(如Donepezil),药物末端编辑效率飙升。更整合多维分子编辑平台,为新药研发提供“无痕”修饰利器。这项《Nature Chemistry》重磅成果,正悄然改写有机合成规则——点击解锁药物化学的全新可能!
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,南京大学化学化工学院陆红健教授团队首创性地将氮原子删除策略(N-atom deletion)引入经典aza-Michael反应体系中,实现了一种全新的无金属参与的脱胺Giese反应。
伯胺是最常见且最廉价的有机砌块之一,广泛存在于天然产物、药物和生物探针分子中,尤其在医药化学中具有不可替代的重要性。虽然胺基广泛用于亲核反应,如aza-Michael加成,但其作为“烷基源”构建(sp³)C−C(sp³)键却面临挑战(图1a)。在此基础上,该团队提出“脱胺Giese反应”新思路(图1b):在aza-Michael反应体系中引入O-二苯基磷酰基羟胺(DPPH),利用其高效的氮删除能力,抑制传统C−N加成路径,从而引导反应走向C−C键构建。其价值体现在以下几个方面:(1)方法学上扭转传统氮杂Michael加成反应体系。无需购买任何新原材料即可获得替代产品,实现构建C−N键到构建C−C键的转化;(2)使用市售试剂O-二苯基膦基羟胺(DPPH)作为脱氮剂,仅需10分钟即可完成转化,具备优异的官能团兼容性与广泛的底物适应性;(3)该方法统一了Giese反应和氮杂Michael加成的反应前体池,为药物发现提供了高效的分子修饰工具。
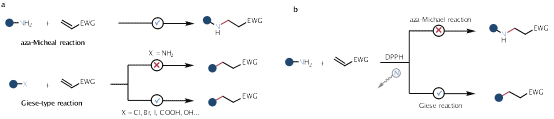
Fig. 1 | Background and Our strategy to access direct deaminative Giese-type reaction. a, Introduction of the aza-Michael and Giese-type reactions. b, This work: DPPH-mediated N-atom deletion in aza-Michael reactions redirects classical C-N bond formation toward Giese-type C-C coupling.
更为突出的是,该反应展现出前所未有的底物普适性和官能团兼容性。作者系统评估了多种胺类底物,涵盖从1°、2°到3°烷基胺,以及具有桥环结构的刚性分子如bicyclo[1.1.1]pentane、2-azabicyclo[2.1.1]hexane和bicyclo[2.2.2]octane等。此外,多种药物片段、天然产物、甚至氨基酸和肽类分子均成功参与反应,体现其优异的适应性。
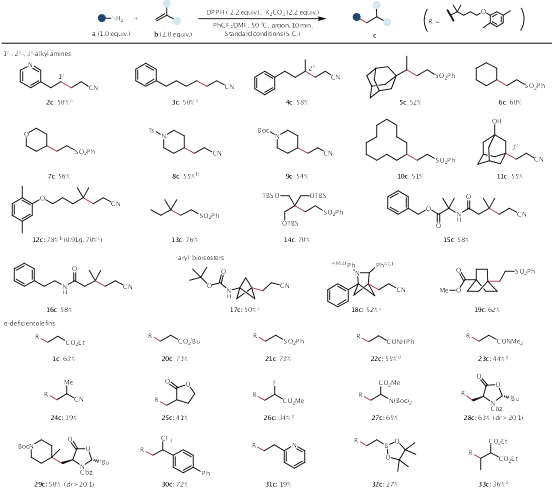
Table 2 | Substrate scope of deaminative Giese-type reaction.
与此同时,该策略也被应用于药物末端编辑中。如Fluvoxamine、Alogliptin、Linagliptin等上市药物通过该方法实现结构转化,保留核心结构同时拓展结构空间。团队还以Donepezil为例,从商品胺出发,三步完成药物合成,展示了该方法在快速构建药物候选分子方面的潜力。
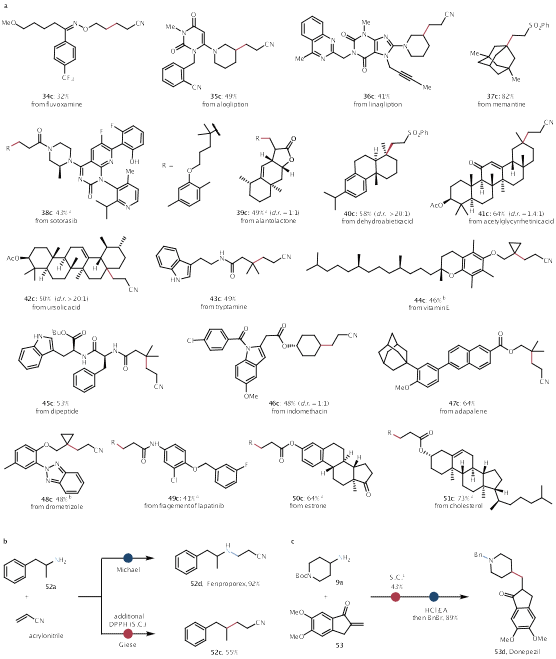
Fig. 2 | Late-stage modification and synthesis of bioactive molecules. a, N-atom deletion of structurally diverse bioactive molecules. b, Synthesis of Fenproporex and its N-atom deleted product. c, Synthesis of Donepezil.
更进一步,研究团队将该脱胺方法与胺导向的C−H功能化策略整合,发展出包括1,1-双官能团化、1,3/1,4-烷基芳基化、氘代反应、三官能团化在内的系列多维分子编辑手段,形成一套基于氮的“无痕”导向官能团化平台,为复杂骨架构建与同位素标记提供解决方案。
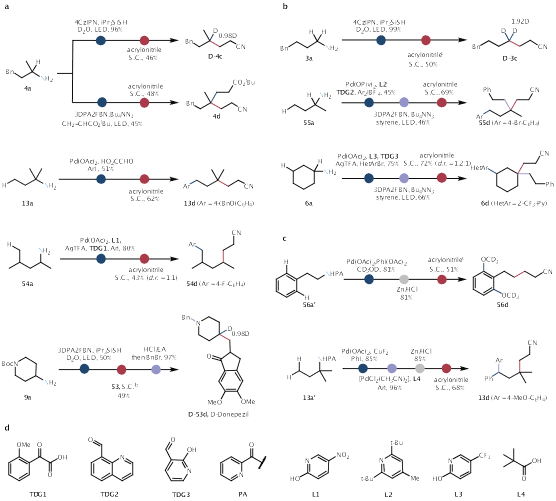
Fig. 3 | Multiple functionalization using N-atom as a traceless directing group. a, Difunctionalization strategies shown include 1,1-dialkylation, 1,1-deturoalkylation, 1,3-alkylarylation, 1,4-alkylarylation, and the synthesis of D-Donepezil. b, Trifunctionalization reactions include 1,1,1-dideturoalkylation and 1,1,3-dialkylarylation. c, 1,4,4-Alkyldialkoxylation and 1,3,3-alkyldiarylation of protected amines. d, Structures of transient directing groups (TDGs), picolinamide (PA) and ligands (L).
作者通过自由基捕获实验(TEMPO、EPR)及自由基钟验证,清晰揭示了反应历程中关键的三氮鎓中间体、异二氮烯及烷基自由基的形成与反应路径,并提出了详细的自由基链式传递机制,为后续反应拓展和设计提供理论基础。
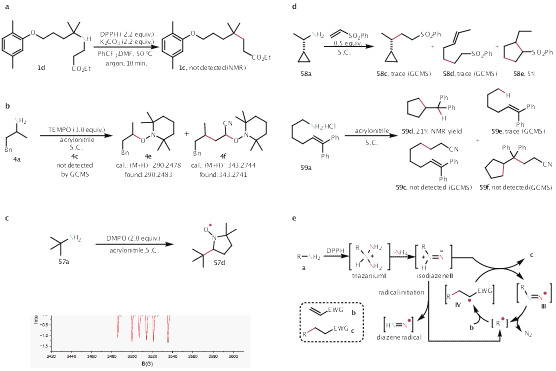
Fig. 4 | Mechanistic studies. a, Detection of key intermediate. b, Radical trapping reaction. c, EPR spectroscopy. d, Radical clock experiments. e, Proposed mechanism.
本研究成功开发了一种脱胺Giese-type反应的新方法。该方法具有温和的反应条件、快速的反应时间和广泛的底物适用性,在生物活性分子的后期功能化中表现出色,为药物化学和天然产物合成提供了新的工具。该研究成果以“Deaminative Giese-Type Reaction”在线发表于《Nature Chemistry》。
该工作通讯单位为南京大学配位化学全国重点实验室、化学化工学院。本文由化学化工学院2021级博士研究生马盼盼(第一作者)、2022级硕士生崔张凯(第二作者)和陆红健教授(通讯作者)共同完成。研究获得国家自然科学基金(22071100、22271148)和江苏省自然科学基金(BK20231400)的资助。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...