科研人员提出“孤儿受体”结构解析新策略
文章导读
面对与焦虑、抑郁密切相关的“孤儿受体”,药物研发往往因缺乏配体而陷入死局,仿佛在黑暗中摸索。中科院团队最近打破僵局,绕过传统依赖配体的老路,利用一种全新策略直接锁定了GPR151的高分辨率结构。这一发现不仅揭示了其“反常规”的分子开关和“内置闸门”机制,更颠覆了我们对GPCR经典激活模式的认知。这套无需纯化蛋白的筛选方法,究竟是如何让“不可成药”的靶点现出原形的?答案藏在那些微小的构象变化里。
— 内容由好学术AI分析文章内容生成,仅供参考。
G蛋白偶联受体(GPCR)是人体内规模最大、分布最广泛的膜蛋白超家族之一。其中,超过140种GPCR因缺乏明确的内源性配体而被称为“孤儿受体”。它们广泛存在于中枢神经系统,与焦虑、抑郁及神经退行性疾病相关,却因“无配体、无效应蛋白”的双重缺失,难以解析其结构与功能。
近期,中国科学院分子细胞科学卓越创新中心等,针对“孤儿受体”结构解析难题提出了全新策略,并解析了“孤儿受体”GPR151(高度集中表达在与负性情绪密切相关的大脑缰核区域)的高分辨率冷冻电镜结构,为该类重要药物靶点的系统性研究打开了突破口。
研究团队利用纳米抗体Nb6构建“分子支架”,通过工程化改造使孤儿受体能够被稳定“锁定”在特定构象。团队进一步发展出无需配体、无需纯化蛋白的热稳定性突变筛选策略NELiS。该方法突破传统依赖配体或纯化体系的限制,仅通过细胞粗提物即可快速筛选稳定突变,降低实验门槛并提升效率。借助NELiS,研究人员在GPR151中识别出4个关键热稳定突变,获得稳定的受体复合物,并解析了GPR151的非激活态冷冻电镜结构。
同时,研究揭示了GPR151“反常规”的分子特征:其经典激活开关W6.48呈异常“向上翻转”构象,并被多重极性相互作用锁定;关键结构基序由疏水环境转变为更亲水配置;Na+结合位点及离子锁结构也发生系统性重塑。这些改变提高了受体激活的能垒,使GPR151稳定维持在非激活状态。
研究发现,GPR151的N端如同“内置闸门”,直接插入配体结合口袋上方,物理性阻断潜在配体进入;移除这一结构后,受体呈现出更接近肽类GPCR的开放构象,并表现出激活趋势。这提示,GPR151可能依赖一种区别于经典GPCR的全新调控机制。
研究结合其在脑内缰核—脚间核通路中的突触前定位提出,GPR151可能不依赖“配体—受体—效应蛋白”模式,而采用更特殊的信号调控方式。这拓展了人们对GPCR作用机制的认知,也为理解神经精神疾病提供了新的分子视角。
这项研究发展了可推广的孤儿GPCR结构解析新范式,揭示了GPR151结构基础,为后续功能研究及药物开发奠定了基础。
相关研究成果在线发表在《美国国家科学院院刊》(PNAS)上。研究工作得到国家自然科学基金、国家重点研发计划、中国科学院战略性先导科技专项等的支持。
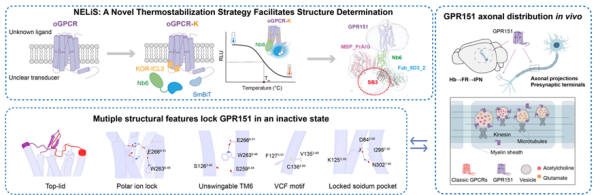
NELiS助力孤儿受体GPR151结构解析
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
















又是PNAS,国内科研现在真卷啊😂
纳米抗体做支架这招有点意思,之前搞过类似实验,稳定构象确实难搞。
这技术听着挺牛的,但具体咋应用到药物开发上啊?