文章导读
病毒不停变异,每次出新款毒株你就赶着去打加强针,以为这叫与时俱进?北大团队用DynaVac数学模型戳破了一个反直觉真相:盲目追新打针,你极可能掉进“免疫陷阱区”——旧记忆死死压制新应答,反而防不住新毒株。更颠覆常识的是,初免剂量越高陷阱越深;而拉长接种间隔、甚至降低剂量,才是跳出陷阱的关键。这套把疫苗设计从盲猜变成精准预测的三分区框架,究竟会如何颠覆你下一次的接种决策?
— 内容由好学术AI分析文章内容生成,仅供参考。
2026年4月16日,北京大学生命科学学院、核糖核酸北京研究中心陆剑研究组与云南大学张子杰研究组合作,在《细胞报告》(Cell Reports)上发表题为“Mapping immune imprinting zones enables predictive vaccination optimization”的研究论文。针对病毒持续变异背景下疫苗更新的核心难题——免疫印记,研究团队构建了可定量预测抗体应答的动力学模型DynaVac,并提出了“保护区-陷阱区-突破区”三分区框架,为变异株疫苗的更新策略与加强免疫方案提供了预测性理论工具。
RNA病毒因复制速度快、突变率高、演化迅速,导致SARS-CoV-2等病毒在流行过程中不断产生能够逃逸既往免疫的新变异株。在此背景下,既往感染或疫苗接种所形成的免疫记忆,在机体再次暴露于新抗原时会被优先唤起,进而影响针对新变异株的抗体应答,这一现象被称为免疫印记。免疫印记既能保留对既往毒株的保护,也可能抑制针对新变异株的从头应答,从而成为变异株疫苗优化的关键障碍。由于免疫史、疫苗平台和变异株之间的组合复杂多变,仅凭经验难以判断何种接种方案能有效更新免疫记忆、建立对新变异株的防护。
陆剑团队长期专注于RNA病毒进化与疫苗优化研究,前期已率先提出SARS-CoV-2的S/L双谱系划分并构建分层次谱系系统,揭示了病毒演化与传播的基本轨迹(Tang et al.,National Science Review,2020);从密码子演化角度提出了mRNA疫苗序列优化策略(Wu et al.,Advanced Science,2023);并建立了SIRSVIDE模型以刻画病毒传播、免疫逃逸与演化动态(Jin et al.,hLife)。在此基础上,本研究进一步构建了基于常微分方程的动力学模型DynaVac。该模型能够从机制层面同时刻画抗原、初始B细胞、记忆B细胞和抗体之间的动态关系,实现了对复杂序贯接种条件下体液免疫反应的定量模拟。
模型构建过程中,本研究首先将体液免疫反应划分为初次免疫和加强免疫两个阶段。初次免疫阶段,模型描述抗原产生、初始B细胞活化与成熟、记忆B细胞形成以及抗体分泌等关键过程;加强免疫阶段则进一步引入不同变异株之间的交叉中和关系,以及既有记忆B细胞与初始B细胞对新抗原的竞争(图1)。相较于传统高复杂度的单细胞水平模拟,DynaVac采用群体层面的平均化建模策略,在保留主要免疫学机制的同时大幅降低计算量,因而能够支持大规模参数拟合和多种接种方案的前瞻性模拟。
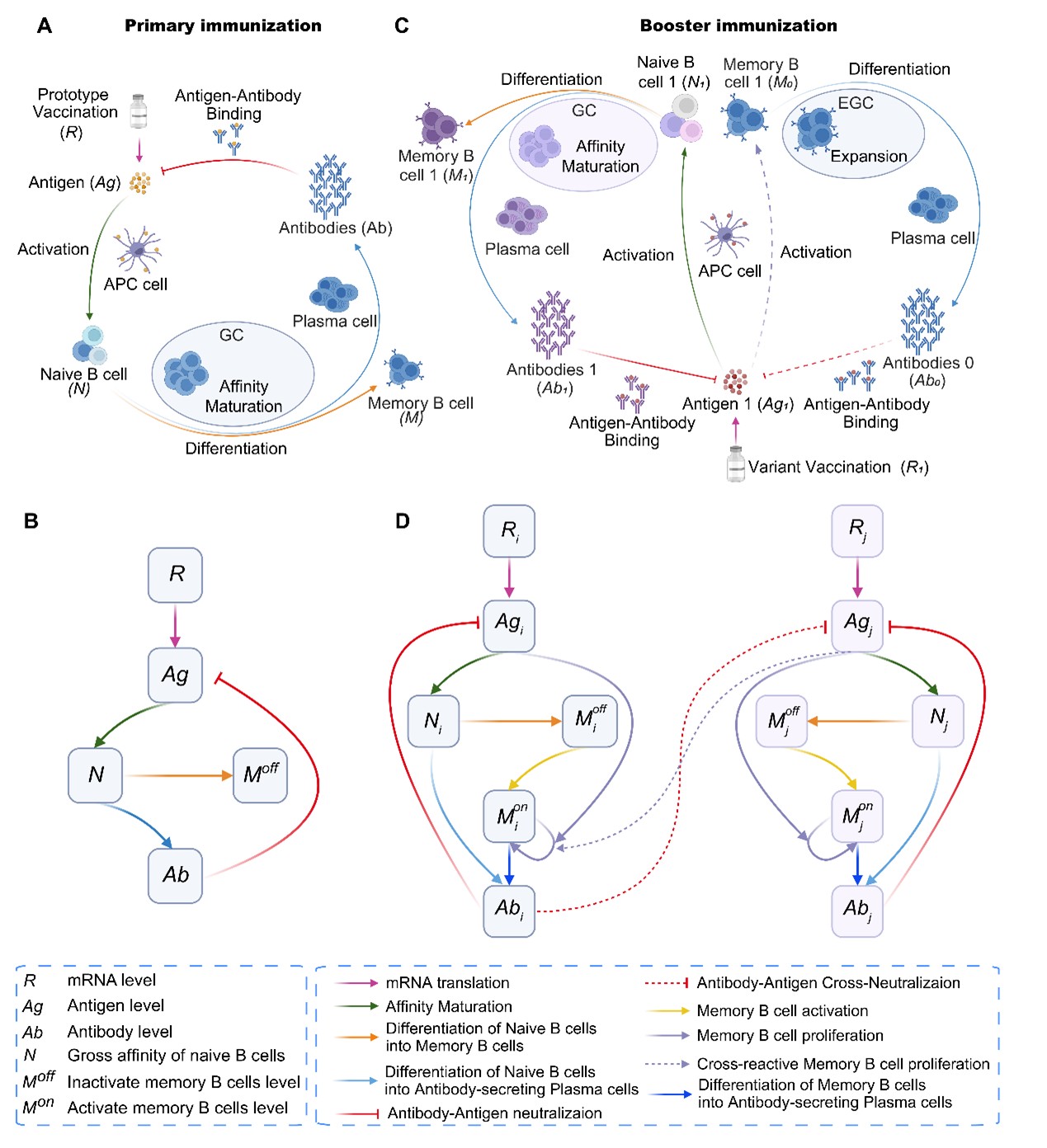
图1. DynaVac模型构建与免疫应答动力学框架
为验证模型性能,本研究设计了涵盖原始株及多个主要新冠病毒变异株的29种小鼠免疫程序,并结合已发表数据集及人体临床试验数据,对模型进行了系统参数化与交叉验证。结果显示,DynaVac能够定量预测不同接种程序下针对多种病毒变异株的中和抗体反应,在小鼠和人体临床试验数据中均表现出良好的预测准确性(图2)。这表明该模型不仅能够解释已有实验观察,更具备对不同免疫背景、疫苗平台及接种策略下抗体应答结果进行前瞻性预测的能力。
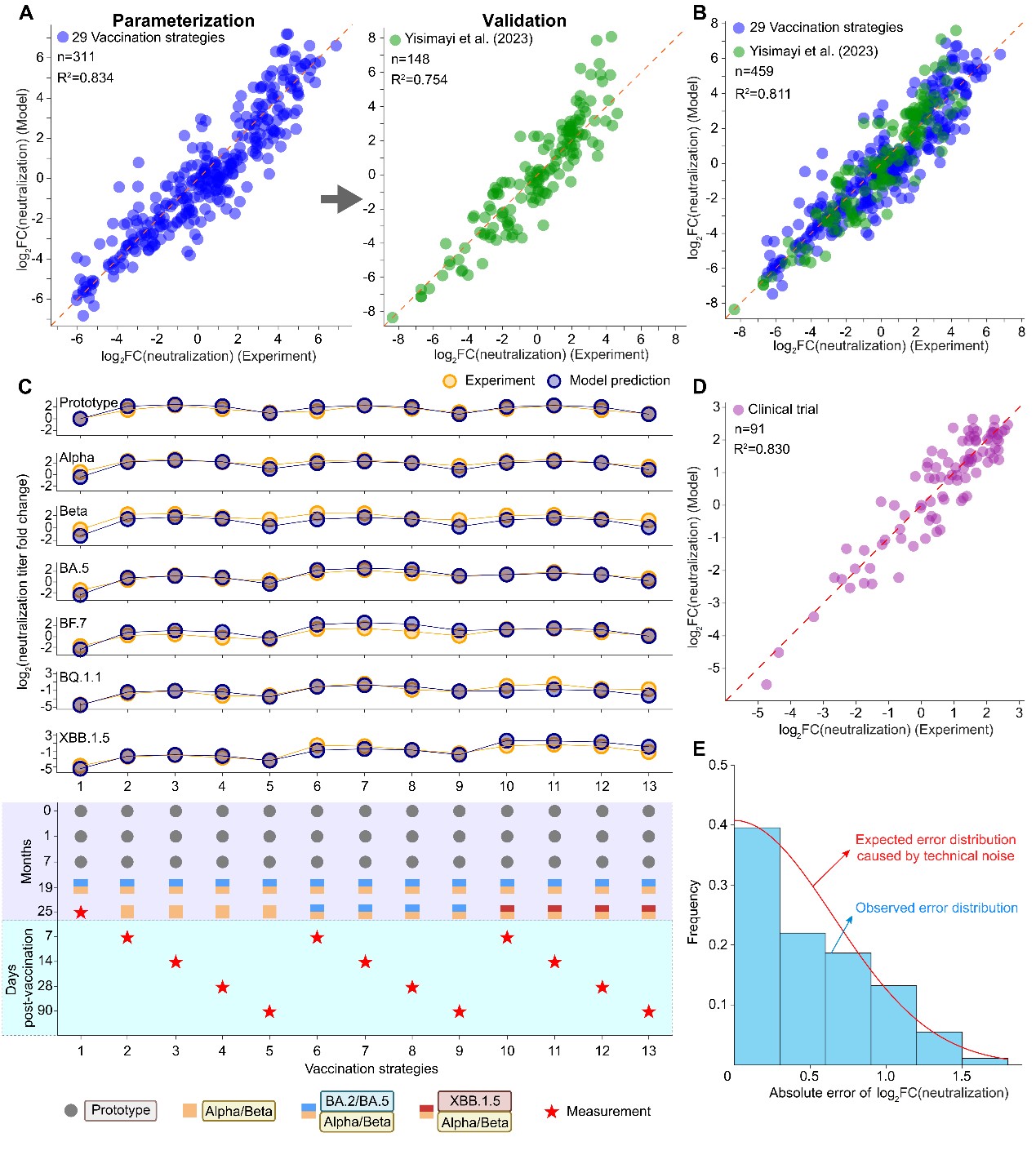
图2. DynaVac模型在小鼠和人体数据中的参数化与验证
在此基础上,研究进一步利用DynaVac对不同抗原距离下的加强免疫过程进行了模拟。结果发现,初始免疫株与加强免疫株之间的抗原距离是决定免疫印记效应走向的核心参数。当两者抗原距离较近时,原有抗体能有效交叉中和新抗原,形成“免疫印记保护区”;当抗原距离处于中间范围时,既有记忆仍足以压制新生应答但交叉中和不足,形成“免疫印记陷阱区”;当抗原距离足够远时,原有记忆对新抗原的压制明显减弱,新变异株特异性应答得以建立,进入“免疫印记突破区”。这一连续的免疫景观为理解不同加强针效果的差异提供了统一解释框架(图3)。
研究还评估了初免剂量和初免—加强间隔对免疫印记的影响。模拟结果显示,较高的初免剂量会强化原始株免疫记忆,扩大陷阱区范围;较低的初免剂量则有助于缩小陷阱区、扩大突破区。与此同时,延长初免与加强的时间间隔可使原有记忆逐渐衰减,减轻对变异株应答的压制。这表明,除抗原成分外,初始剂量与时间窗口同样是调控疫苗更新效果的关键因素(图3)。
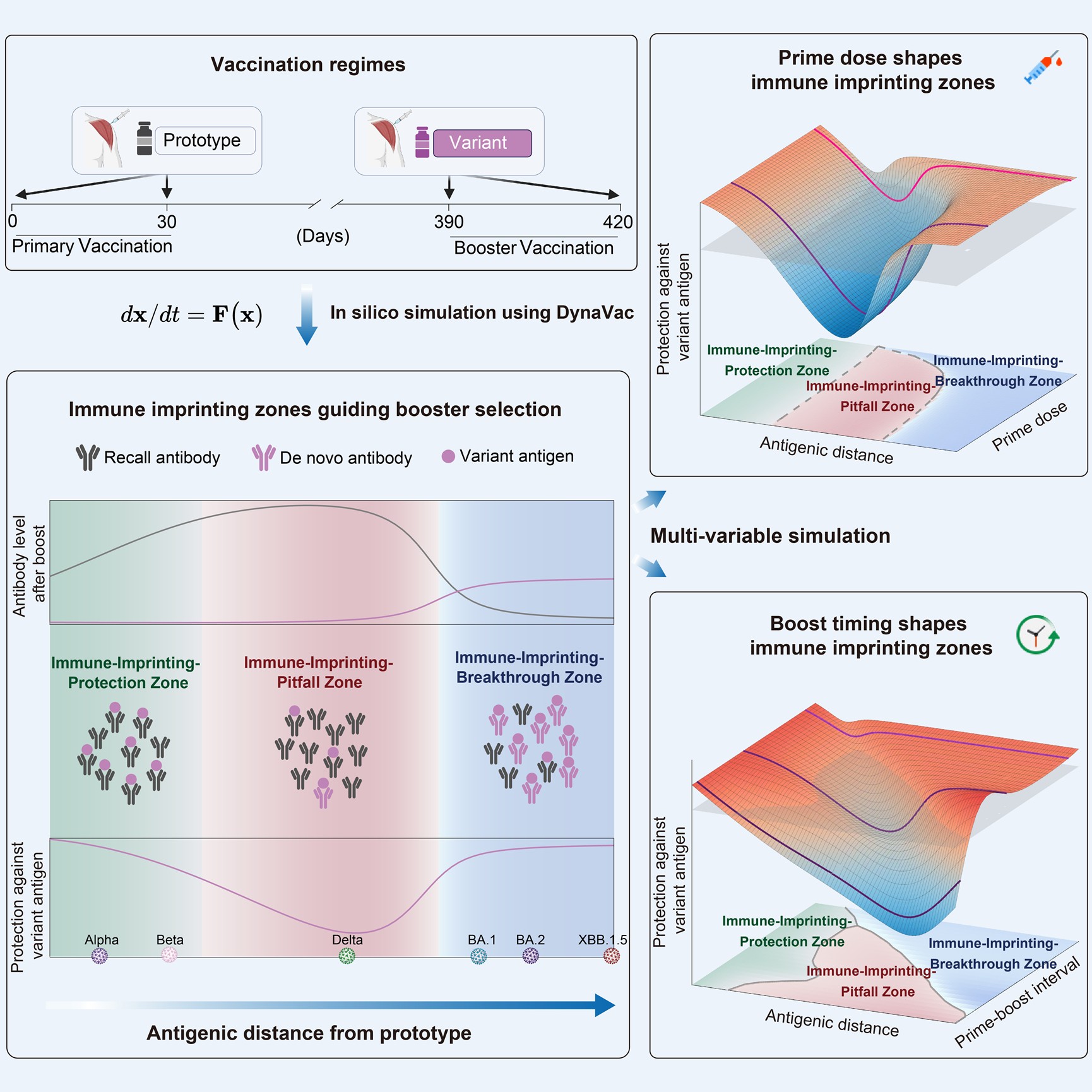
图3. 抗原距离、初免剂量和接种间隔共同塑造免疫印记的“保护区-陷阱区-突破区”
综上,该研究建立了定量预测复杂序贯接种免疫结果的动力学框架DynaVac,提出了免疫印记的“保护区-陷阱区-突破区”三分区模型,揭示了抗原距离、接种剂量和免疫时程共同塑造变异株疫苗的应答方向。该成果不仅为理解新冠病毒持续变异背景下的疫苗更新难题提供了新理论框架,也为流感、HIV等快速演化病原体的疫苗优化提供了可推广的建模思路。更重要的是,该工作推动疫苗设计从经验驱动迈向预测驱动,为在动态变化的病毒抗原景观中实现精准疫苗更新开辟了新路径。
云南大学生物交叉技术创新中心杨薇助理研究员、北京大学生命科学学院博士生靳垲淳和云南疫苗实验室mRNA BU负责人李薇为论文共同第一作者,张子杰和陆剑为共同通讯作者。该研究得到科技部国家重点研发计划、广州国家实验室专项项目、国家自然科学基金等多个项目支持,并依托北京大学高性能计算平台完成。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。














北大和云大合作?这配置有点强啊,坐等临床应用。
以前只听说免疫印记,没想到还能分三个区,涨姿势了。
这模型看着挺牛,就是不知道真打疫苗时能不能用得上?