文章导读
全球超90%的成年人都携带EB病毒,为何只有少数人会患上残酷的多发性硬化症?这项刚登顶《Cell》的研究,终于补上了这块拼图的关键缺失。问题不在病毒本身,而在于它与你基因里的一个“缺陷”发生了致命碰撞。研究发现,EB病毒感染会“重编程”你的免疫细胞,强行呈递出一种平时被隐藏的神经抗原,直接引爆自身免疫攻击。这一机制不仅解释了为何该病难以预防,更指向了一个让免疫系统“识别敌我”的关键开关——这个发现或许能改写无数患者的命运。
— 内容由好学术AI分析文章内容生成,仅供参考。
2026年1月14日,中国科学技术大学生命科学与医学部、免疫应答与免疫治疗全国重点实验室王剑教授课题组与苏黎世大学Roland Martin教授课题组合作在《Cell》期刊在线发表题为“EBV Infection and HLA-DR15 Jointly Drive Multiple Sclerosis by Myelin Peptide Presentation”的研究论文。该研究通过免疫多肽谱分析和自身反应性CD4+T细胞功能鉴定,揭示了爱泼斯坦-巴尔病毒(EBV)感染与人类白细胞抗原HLA-DR15协同作用,通过呈递髓鞘自身抗原多肽并激活自身反应性CD4+T细胞,共同驱动多发性硬化症(MS)发生的新机制。
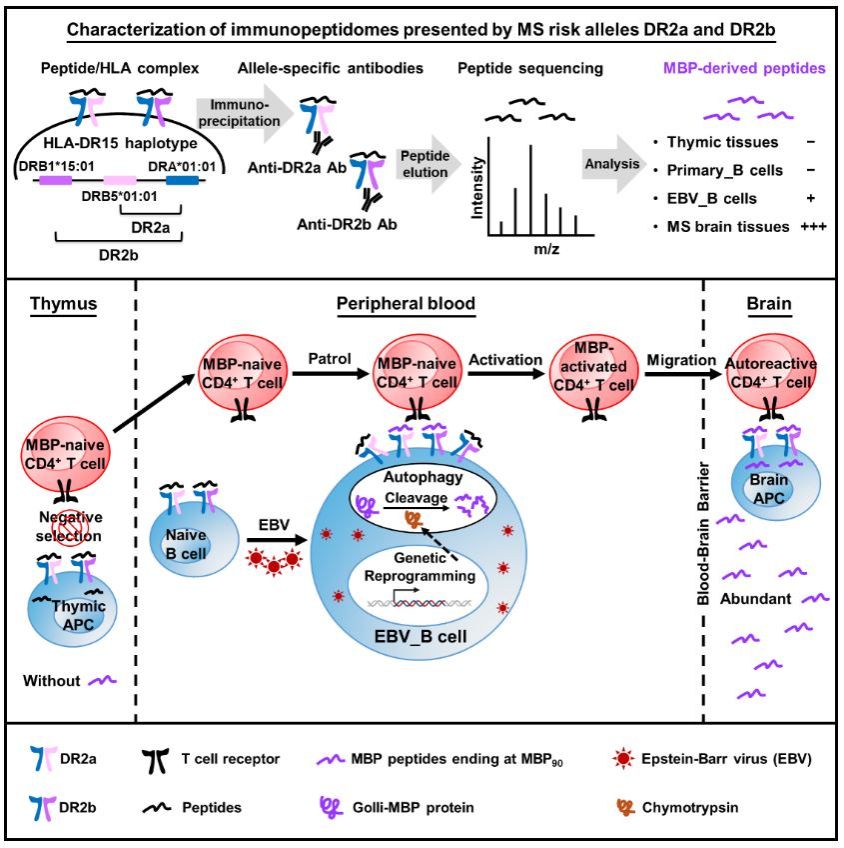
MS是一种以中枢神经系统慢性炎症性脱髓鞘为特征的自身免疫病,其发病由遗传易感性与环境因素共同介导。在环境因素中,EBV感染是诱发MS最主要的环境风险因素,全球超过90%的成年人曾感染过该病毒,而在MS患者中该比例接近100%。EBV感染后可在记忆B细胞中建立终身潜伏,既往研究表明感染导致B细胞转录谱的改变可能与MS的诱发有关,但是其具体作用机制还不清楚。在遗传因素中,HLA-DR15单体型是已知最强的MS遗传风险因子,可贡献高达60%的遗传风险。该单体型编码的两种MHC II类分子DR2a与DR2b,主要负责向CD4+T细胞呈递抗原多肽,这与MS作为CD4+T细胞介导的自身免疫病本质相契合。2020年王剑课题组的研究曾揭示,EBV抗原激活的记忆性CD4+T细胞可通过“分子模拟”交叉识别自身抗原,从而触发MS(Wang et al., 2020, Cell183, 1264–1281)。然而,这一发现并不能解释EBV感染导致的记忆B细胞转录谱的改变与MS发生之间的关系。
在本研究中,王剑课题组进一步发现,EBV感染不仅重编程B细胞,也改变了HLA-DR15分子所呈递的多肽谱。关键突破在于:在EBV感染的B细胞中,研究者检测到重要的MS自身抗原髓鞘碱性蛋白(MBP)来源的多肽MBP(78-90)和MBP(83-90)被HLA-DR15呈递,而在正常B细胞中则未检出。与此对应,在HLA-DR15阳性MS患者的脑组织中,也发现了完全相同的MBP多肽。功能实验表明,从HLA-DR15阳性MS患者外周记忆及脑脊液来源的CD4+T细胞,能对上述MBP多肽产生特异性免疫应答。更为重要的是,利用这些多肽扩增得到的CD4+T细胞克隆,可交叉识别MS脑组织中所有C端以苯丙氨酸(F90)结尾的MBP多肽。因此,本研究揭示了一条新的MS致病机制:EBV感染通过重塑B细胞的免疫多肽谱,促使关键的神经系统自身抗原被HLA-DR15分子呈递,从而激活自身反应性CD4+ T细胞。这一发现为环境因素(EBV感染)与遗传风险因素(HLA-DR15单体型)如何协同作用,共同驱动MS的发生提供了新的机制性解释。
中国科学技术大学免疫应答与免疫治疗全国重点实验室王剑教授为文章第一作者及共同通讯作者,苏黎世大学Roland Martin教授为文章共同通讯作者。免疫应答与免疫治疗全国重点实验室,合肥综合性国家科学中心大健康研究院李凤琦研究员、金林林特任副研究员和张宏霞博士后,中国科学技术大学附属第一医院神经内科徐文副主任以及安徽医科大学第一附属医院李婷婷博士共同参与了本项研究。该研究受到国自然基金委、科技部、中国科学院以及合肥综合性国家科学中心大健康研究院等项目资助。
论文链接:https://doi.org/10.1016/j.cell.2025.12.046
(生命科学与医学部、免疫应答与免疫治疗全国重点实验室、科研部)
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。

















感觉研究太专业,普通人搞不懂。
我之前也看过EBV和MS的关联,没想到有新解释。
这个机制听起来有点像科幻。
太惊讶了,EBV竟然和基因这么配合。