文章导读
你以为皮肤只是人体的一道物理城墙?当病原体入侵时,表皮细胞其实在进行一场惊心动魄的“代谢呼救”。清华大学团队发现,角质形成细胞竟能释放一种名为FPP的“警报素”,它像信使一样精准激活全身免疫开关TRPV3,让抗体产量爆发式增长。更反直觉的是,这一机制不仅能指导新型疫苗研发,其过度活化竟也是红斑狼疮等顽疾的幕后推手。同一个分子,如何在“护盾”与“杀手”之间切换?答案藏在那个你从未听说的信号轴里。
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,清华大学生命科学学院刘万里教授团队合作研究揭示了角质形成细胞(KC细胞)甲羟戊酸通路代谢中间分子(法尼基焦磷酸FPP)作为内源性警报素,在病灶局部结合并激活TRPV3,进而启动Ca2+-CaM-Calcineurin-NFAT和PYK2–RAS–ERK双信号通路,增强系统性IgG抗体应答。团队同时揭示Carvacrol和Camphor等植物来源的芳香类TRPV3激动剂也通过TRPV3-Ca2+信号轴放大IgG抗体应答;这样一内一外“内源性代谢警报素+外源性感觉芳香素”形成的相辅相成的双模TRPV3激活信号转导体,为新型疫苗佐剂的研发以及系统性红斑狼疮(SLE)等自身免疫病的防治提供潜在靶点和思路。
局部感染或刺激如何“牵一发而动全身”,触发远端淋巴器官的生发中心(GC)反应,从而建立系统性体液免疫应答,是免疫学长期关注的关键难题。体液免疫要产生高滴度、高亲和力的IgG抗体并形成免疫记忆,离不开滤泡辅助性T细胞(Tfh)的分化、B细胞在GC中的增殖、分化与亲和力成熟。皮肤作为人体最大的外周免疫器官之一,是抵御病原体入侵与环境刺激的第一道屏障。皮肤最外侧表皮的KC细胞不仅承担物理屏障作用,更能感知外界各类威胁,通过PAMPs和DAMPs分子来协调免疫防御,连接固有免疫与适应性免疫。然而,局部病灶究竟通过何种关键信号才能把信息精准传递到引流淋巴结,定向上调Tfh–GC轴介导的IgG应答强度仍然不清楚。
抗体应答强度被免疫系统设定的“阈值”予以决定。一方面,遗传变异可以把阈值调低,使机体更容易出现异常体液免疫放大。另一方面,外界刺激同样可能通过“代谢信号MAMPs”改变免疫阈值。甲羟戊酸通路是细胞必需的核心代谢途径。
此通路的代谢中间物是否会在局部感染或刺激中被“动员”为可快速远距离传播的免疫信号,从而把局部逆境高效转译为系统性体液免疫放大?一系列自身免疫病(以SLE为典型代表)通常伴随皮肤的金黄色葡萄球菌定植升高,并受到环境胁迫因素(如过度过强光照辐射等)的持续影响。这一系列的临床观察提示局部病灶可能不断向免疫系统输入异常信号,进而改变免疫应答阈值。由此,局部皮肤免疫紊乱如何逐步演变为全身性的自身抗体反应,不仅是基础免疫学的重要问题,也直接关系到SLE等疾病的发生发展及干预策略。
基于上述一系列的关键科学问题,刘万里团队联合多方合作者开展跨学科攻关,通过代谢组学、单细胞测序、分子生物学、动物模型等多种研究手段,系统鉴定FPP是KC细胞来源的内源性警报素,并解析其调控全身体液免疫的FPP-TRPV3-IL-6/CCL20-GC信号轴(图1,2);同时发现香芹酚(Carvacrol)和樟脑酮(Camphor,莰酮,常用俗名为樟脑)等芳香类TRPV3激动剂可类似地通过TRPV3-Ca2+信号轴增强抗体应答(图2)。上述工作揭示局部感染触发系统性体液免疫的全新分子机制。
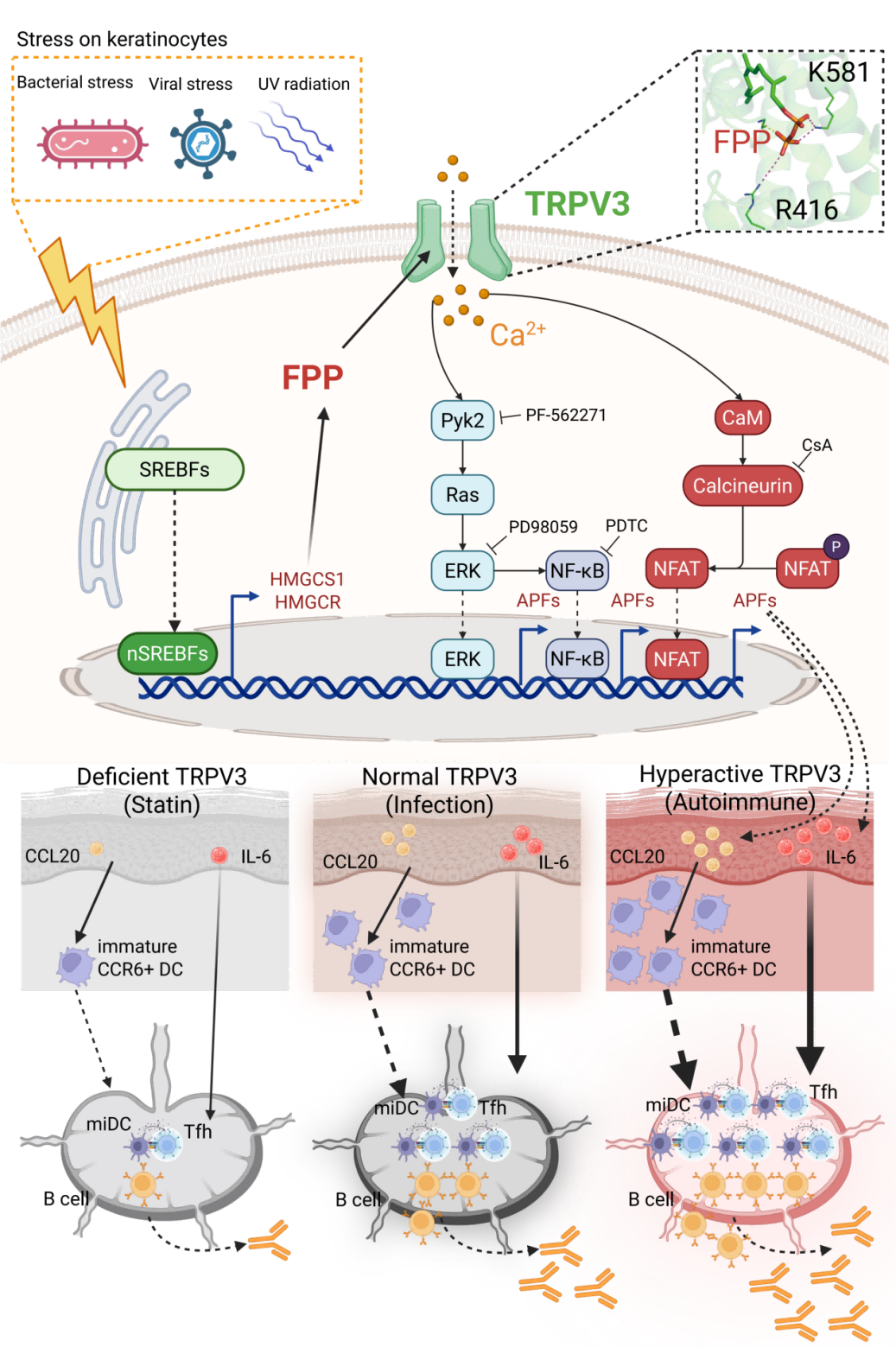
图1. UPR–SREBFs–MVA–FPP–TRPV3–IL-6/CCL20–Tfh/GCB信号轴的示意图

图2.警报素与芳香素的双模TRPV3激活介导的系统性抗体应答
具体来说,当皮肤受到病原体感染或紫外线辐照时,未折叠蛋白反应(UPR)会激活甲羟戊酸通路的固醇调节元件结合蛋白(SREBFs)转录因子,促使KC细胞在胞内快速累积FPP;累积的FPP会结合KC细胞TRPV3胞内结构域(包含关键位点R416和K581),诱导胞外钙离子进入胞浆,进而激活Ca2+-CaM-Calcineurin-NFAT和PYK2–RAS–ERK两条下游信号通路,诱导KC细胞分泌IL-6和CCL20等促进抗体应答的炎症因子和趋化因子。其中,IL-6可促进Tfh细胞分化,CCL20则能招募并促进迁移性2型常规树突状细胞向引流淋巴结迁移。在二者的协同作用下,显著增强引流淋巴结中GC反应,不仅促进了病原体特异性IgG抗体应答,同时也提升了引流淋巴结中记忆性B细胞和浆细胞的生成,为机体建立长效的体液免疫保护。
为验证该信号轴的生理功能,研究团队构建多种基因敲除的工程小鼠模型,发现FPP介导的抗体增强效应在TRPV3缺陷小鼠中被减弱:TRPV3敲除小鼠在链球菌感染后,血清中病原体特异性IgG抗体滴度显著降低,引流淋巴结中Tfh细胞和GC B细胞分化受阻,面对高剂量病原体再次攻击时,皮肤坏死病灶更大、体重损失更严重;而野生型小鼠则能通过FPP-TRPV3轴建立有效的免疫保护。
综上所述,研究发现代谢中间物FPP作为KC细胞来源的内源性警报素的全新功能,解析“病灶局部危险信号调控全身体液免疫”的分子通路;揭示FPP-TRPV3轴在SLE发生发展中的重要作用,证实该信号轴的过度活化是驱动自身免疫紊乱的重要机制。FPP的急性局部佐剂效应为新型疫苗佐剂的研发开辟了新方向,尤其在黏膜免疫和抗感染疫苗开发中展现出重要的应用前景。该研究将代谢调控与体液免疫紧密结合,为理解免疫代谢的交叉调控机制提供了全新视角,也为免疫相关疾病的转化医学研究奠定了重要的理论基础。
研究成果以“角质形成细胞的代谢警报素诱导系统性免疫应答”(A metabolic alarmin from keratinocytes potentiates systemic humoral immunity)为题,于3月4日发表于《自然》(Nature)。
清华大学冀正林博士、博士生高吉、张少存博士、本科生李嘉杰(现为清华大学博士生),湘雅二医院教授吴海竞,浙江大学博士生姚婧,清华大学马先强博士,湘雅二医院博士生忻悦,清华大学朱永杰博士以及赵萌博士为论文共同第一作者。清华大学生命学院教授刘万里、中国医学科学院皮肤病医院教授陆前进、清华大学药学院教授张永辉为论文通讯作者。
研究得到国家自然科学基金、国家重点研发计划、科技部项目、中国医学科学院医学创新基金、中国博士后科学基金,以及北京、深圳等地方科研基金和高层次卫生人才计划的支持。
论文链接:
https://doi.org/10.1038/s41586-026-10167-6
供稿:生命学院
编辑:李华山
审核:郭玲
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。


















发在Nature上的,含金量肯定没得说,就是这机制看着太复杂,脑子不够用了。
红斑狼疮患者表示一直在关注这方面的进展,希望能早点应用到临床,这病太折磨人了。
哇塞,樟脑居然还能激活免疫,老一辈爱用的那些土方子看来是有科学依据的啊。
这就跟以前说的“牵一发而动全身”一个道理,皮肤有点啥毛病全身都跟着遭罪。