生命科学与技术学院唐娟团队联合研究揭示心肌梗死后心脏不良重塑新机制与干预靶点,成果发表于《循环》
文章导读
心梗后心脏逐渐衰竭,你以为只是心肌细胞死亡那么简单?但最新的研究发现,真正的“幕后推手”可能是一群打着“衰老”标签的P16阳性细胞。它们并非无害旁观者,反而会主动分泌信号,招募免疫细胞来攻击本已脆弱的心脏组织,加剧纤维化和功能丧失。这项由同济大学与上海科技大学团队发表于《循环》的研究,首次精准绘制了这群细胞的“身份图谱”,并找到了它们煽动破坏的关键信使——CCL8。更有趣的是,通过特殊技术清除其中一类特定的P16阳性细胞,竟能有效逆转心脏损伤。这背后,是否隐藏着比传统抗炎疗法更精准、更有效的干预靶点?
— 内容由好学术AI分析文章内容生成,仅供参考。
心肌梗死后,心脏会经历由炎症、细胞死亡和纤维化瘢痕形成等驱动的不良重塑,最终导致心力衰竭。然而,驱动过程中的细胞和分子机制一直未被完全阐明。近日,同济大学生命科学与技术学院唐娟教授团队与上海科技大学生命科学与技术学院张辉教授团队联合在《循环》(Circulation)杂志上发表突破性研究,首次系统揭示P16阳性细胞在心脏不良重塑中的关键作用,并提出了靶向CCL8信号或P16阳性成纤维细胞的精准干预新策略。

研究中,团队利用先进的细胞谱系标记技术为细胞“贴标签”,首次绘制了心梗后心脏中P16阳性细胞的“身份图谱”。研究发现,在受损的心脏区域,成纤维细胞、巨噬细胞、血管内皮细胞甚至心肌细胞都会大量表达P16。通过单细胞测序等技术,团队锁定了其中两类关键细胞——P16阳性的成纤维细胞和巨噬细胞——它们并非旁观者,而是主动“煽风点火”的“肇事者”。这两种类型细胞大量分泌趋化因子CCL8,从而将细胞毒性淋巴细胞——尤其是CD8+ T细胞(杀伤性T细胞),招募至受损的心脏组织。这些被招募来的免疫细胞释放攻击性分子,直接导致心肌细胞凋亡,进一步加剧组织结构破坏和功能障碍(图1)。为了验证这一机制,研究团队在小鼠模型中开展了系列干预实验。结果表明,无论是使用抗体中和CCL8,还是利用Cre/loxP技术条件性敲除P16阳性细胞中的Ccl8基因,均可显著减少细胞毒性淋巴细胞的浸润、保护心肌细胞、缩小心梗后瘢痕面积,并有效改善心脏功能(图1)。
更值得关注的是,团队采用“双重锁定”基因技术(双重组酶介导的白喉毒素受体表达系统),实现了对P16阳性成纤维细胞或巨噬细胞的精准清除。结果显示,仅清除P16阳性成纤维细胞即可显著促进心脏修复;而清除P16阳性巨噬细胞则无明显效果,提示P16阳性成纤维细胞是驱动不良重塑的核心细胞亚群,也是未来药物干预的精准靶点。
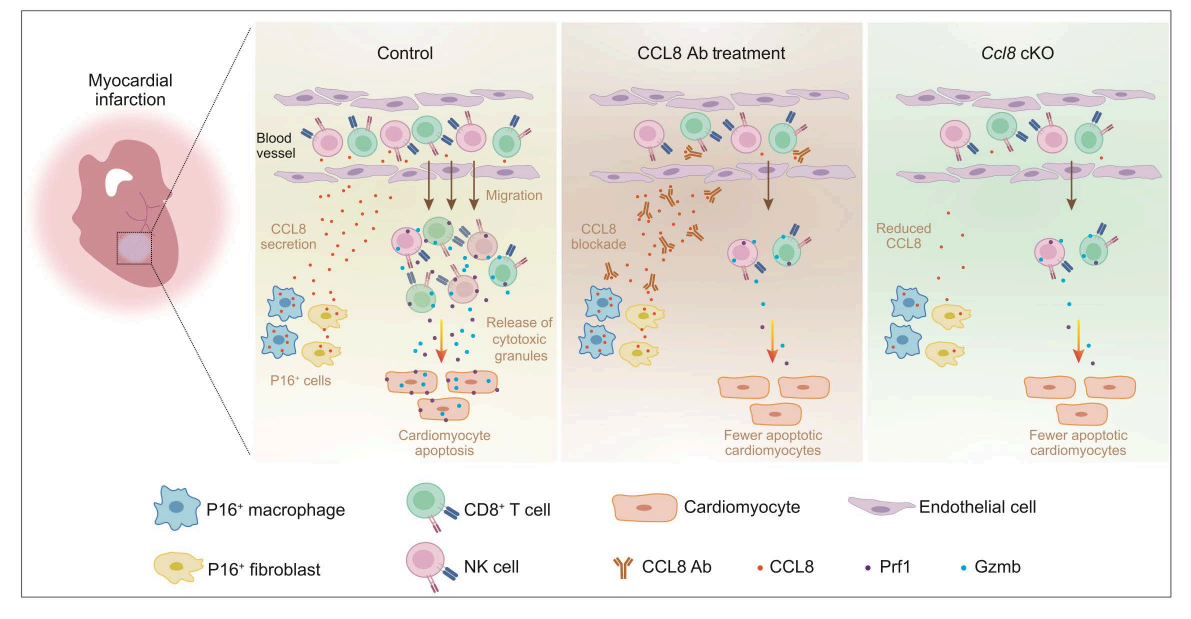
图1.研究示意图:P16阳性细胞通过分泌CCL8招募CD8+ T细胞和自然杀伤(NK)细胞,诱导心肌细胞凋亡,推动心梗后心脏不良重塑
上海科技大学生命科学与技术学院博士研究生严磊、郑嘉蕾以及同济大学生命科学与技术学院/附属东方医院博士后卢正开为论文共同第一作者。同济大学生命科学与技术学院/附属东方医院唐娟研究员和上海科技大学张辉教授为共同通讯作者。该研究得到了国家重点研发计划、国家自然科学基金等项目的资助,为开发基于免疫调节和细胞精准治疗的新型心梗药物提供了重要理论基础。
论文链接:https://doi.org/10.1161/CIRCULATIONAHA.125.077172
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。












心梗后还能精准清除特定细胞?这技术临床得等多久啊😭
清除巨噬细胞居然没效果,这和我去年做的实验结果有点出入啊
P16阳性成纤维细胞才是关键?之前看文献还以为巨噬细胞主导呢🤔