文章导读
你正在为肿瘤治疗中免疫细胞受损的问题困扰吗?传统放疗总是难以兼顾精准杀伤与免疫保护,这个医学界几十年的难题,现在有了突破性发现。北京大学团队首次在实验中验证,硼中子俘获治疗能在单细胞尺度上实现精准打击——它不仅能有效激活抗肿瘤免疫,更惊人的是能显著降低对免疫细胞的直接损伤。这种治疗方式如何重塑肿瘤免疫微环境?为什么它能在"冷""热"两种肿瘤模型中同时发挥作用?答案就藏在那5-9微米的杀伤范围里,这个微米级的差异,可能正是打开肿瘤治疗新局面的钥匙。
— 内容由好学术AI分析文章内容生成,仅供参考。
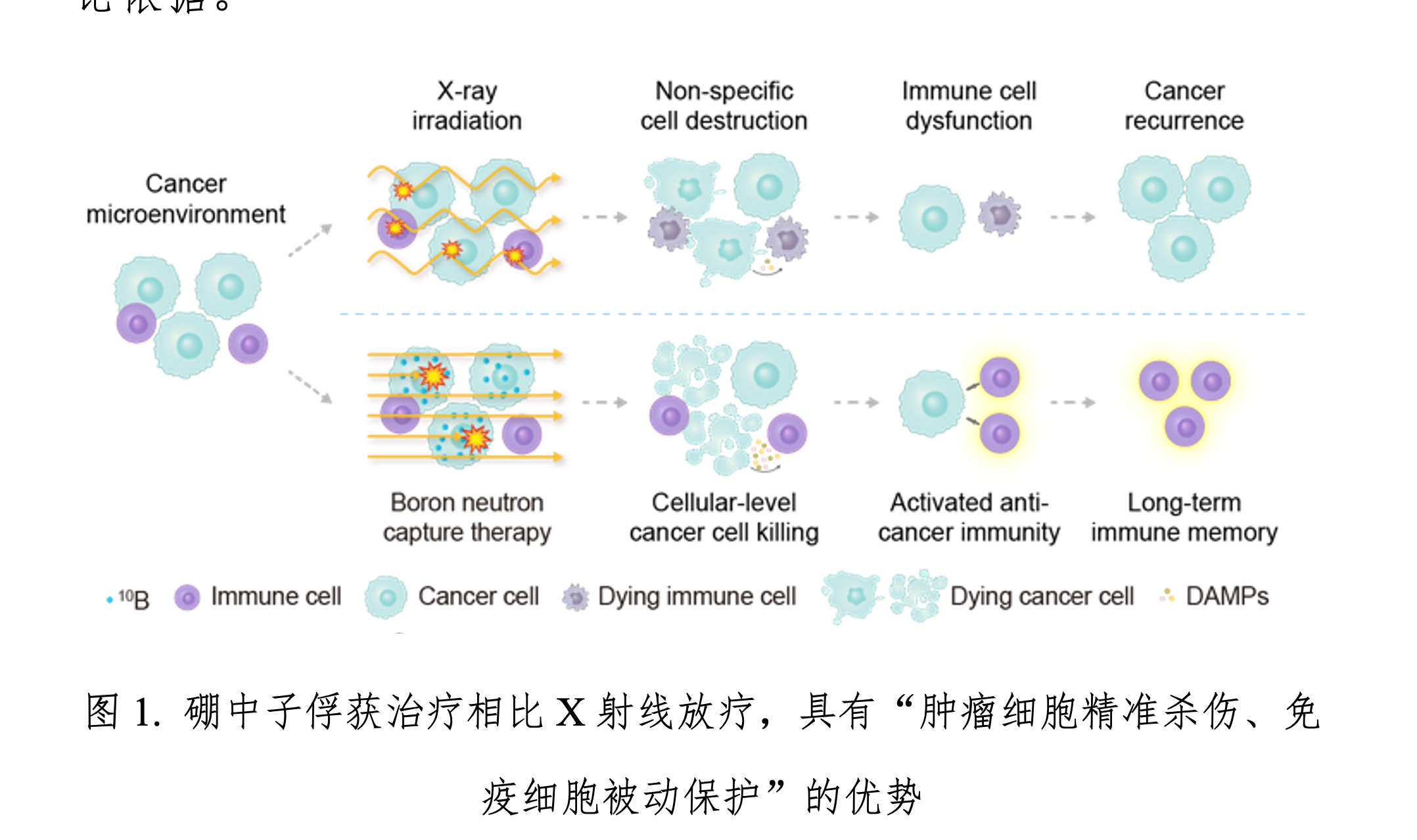
放射治疗在肿瘤治疗中发挥着重要作用,但其杀伤作用通常缺乏细胞层面的选择性,往往在清除肿瘤细胞的同时对免疫细胞造成不可避免的损伤,从而限制放疗诱导抗肿瘤免疫效应的发挥。如何在细胞尺度上实现对肿瘤细胞的精准杀伤,并最大程度保留免疫细胞功能,是放射生物学领域长期未能解决的关键问题。硼中子俘获治疗(Boron neutron capture therapy,BNCT)基于硼-10俘获热中子后释放高传能线密度粒子的物理过程,其杀伤范围为5—9微米,从理论上具备“单细胞尺度放疗”的独特优势。然而,这一精准杀伤特性是否能够在生物学和免疫学层面转化为明确的治疗获益,仍缺乏系统实验证据。
近期,化学与分子工程学院应用化学系刘志博团队与北大-清华生命科学联合中心曾泽贤团队合作,在Nature Communications上发表了题为“Boron neutron capture therapy preserves immune cells and induces robust anti-tumour immunity in preclinical mouse model”的研究文章。研究系统比较了硼中子俘获治疗与等剂量X射线放疗在免疫“冷”肿瘤和“热”肿瘤模型中的生物学与免疫学效应,发现BNCT能够在两类肿瘤模型中有效激活抗肿瘤免疫反应,并在高效杀伤肿瘤细胞的同时,显著降低对肿瘤微环境中免疫细胞的直接损伤,体现出细胞尺度上的治疗选择性。单细胞转录组分析进一步表明,BNCT可显著重塑肿瘤免疫微环境。该研究从生物学层面验证了BNCT作为“单细胞尺度放疗”的独特治疗模式,为其优异疗效提供了重要免疫学解释,也为放疗与免疫治疗的协同优化提供了新的理论依据。
刘志博和曾泽贤为论文共同通讯作者。北大-清华生命科学联合中心博士生孙琪(已毕业)、清华-北大生命科学联合中心博士生赵艳萍、昌平实验室助理研究员乔思邈博士为论文共同第一作者。该工作得到了北京大学化学与分子工程学院、北大-清华生命科学联合中心、北京大学成都前沿交叉生物技术研究院、昌平实验室、北京分子科学国家研究中心、中华人民共和国科学技术部、国家自然科学基金、北京市自然科学基金、中国博士后基金面上项目等机构和项目的资助。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。













免疫细胞保留住了是不是意味着后续治疗更顺利
想问下这个治疗现在进入临床试验阶段了吗
看不懂但感觉很厉害的样子
研究团队背景很强啊,北大清华联合
要是临床能用上就好了
之前也关注过放疗,总担心副作用太大
这个BNCT听起来挺厉害的,能精准杀肿瘤还不伤免疫细胞