研究构建出新型海胆状铜单原子纳米酶
文章导读
肿瘤治疗迎来革命性突破!当海胆状纳米酶的针刺长度成为抗癌关键,你是否好奇微观形貌如何改写治疗规则?中国科学院合肥物质科学研究院与新加坡南洋理工大学团队,依托强磁场装置首创铜单原子纳米酶UCCSE,其独特针刺结构竟能精准调控细胞内吞效率——针刺越长,肿瘤富集能力越强,杀伤效果倍增。它巧妙催化体内双酶反应,持续产生高活性自由基并阻断癌细胞防御,动物实验中安全高效抑制肿瘤生长。这项发表于ACS Nano的研究,首次揭示形貌与疗效的构效密码,为纳米酶抗癌开辟全新路径。
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,中国科学院合肥物质科学研究院与新加坡南洋理工大学合作,依托稳态强磁场实验装置电子顺磁共振谱仪,构建出新型海胆状铜单原子纳米酶,并揭示了海胆针刺长度与细胞内吞效率及相应肿瘤催化治疗效果之间的构效关系。
研究以多巴胺和氯化铜为前驱体,利用有机分子碳化—自还原策略,一步合成出海胆状铜单原子纳米酶UCCSE,并通过精细调控表面针刺长度优化其催化性能。在肿瘤微环境中,UCCSE展现出类过氧化物酶与类谷胱甘肽过氧化物酶活性:催化内源性H2O2持续产生高活性的羟基自由基,并消耗细胞内还原性谷胱甘肽,抑制•OH被清除,放大氧化应激效应,提升了化学动力学治疗效果。研究进一步结合电子顺磁共振测量、米氏动力学分析及理论计算等手段证实,UCCSE的高类芬顿催化效率源自高度分散的CuN4单原子活性位点。
研究还剖析了海胆针刺长度与细胞内吞行为之间的构效关系。研究依托活细胞成像工作站、细胞内铜含量测定等技术发现,UCCSE通过内吞途径被细胞摄取。实验显示,UCCSE在相同时间内的胞内聚集量及相应的肿瘤细胞杀伤能力,随针刺长度增加而提升,证明了针刺形貌能够增强纳米酶的内吞效率和肿瘤细胞摄取能力。该研究从微观形貌调控视角,为提升单原子纳米酶的肿瘤化学动力学治疗性能提供了新思路。
实验结果表明,UCCSE在细胞水平和动物实验中展现出优异的抗肿瘤效果。不同针刺长度的UCCSE在体内治疗表现方面存在差异:长针刺结构在血液中具有更长的循环时间和更高的肿瘤富集能力,展现出肿瘤生长抑制作用,且未对小鼠主要脏器和组织造成明显不良影响,表现出良好的生物安全性。
相关研究成果发表在ACS Nano上。研究工作得到国家重点研发计划等的支持。
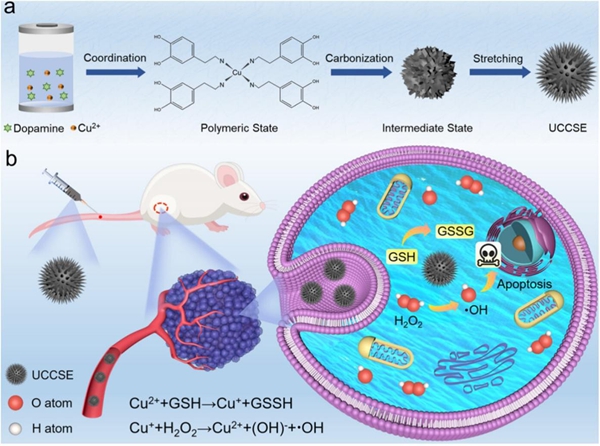
UCCSE的合成及肿瘤催化治疗示意图
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。


















作者赶紧出个视频讲解吧,示意图看不够!
生物安全性没明显影响?那临床还远吗?
说真的,这种结构能批量生产吗?成本咋样?
类芬顿反应+形貌调控,这思路简直双杀 👍
催更后续动物实验细节!小鼠数据看着太爽了
为啥是多巴胺当原料?不会让细胞“快乐”死吧
铜单原子也能做高活性位点,材料学真魔幻
UCCSE听着像某种神秘代码,其实是抗癌利器 😂
这催化效率提升得靠针刺长度?有点意思🤔
太牛了,海胆状纳米酶还能这么玩!