东南大学张宇团队在《自然通讯》上发表纳米酶催化机制调控最新研究成果
文章导读
普鲁士蓝纳米酶只能清除自由基?东南大学张宇团队重磅发现:掺入微量铯离子竟能让它“逆转基因”,从抗氧化卫士变身高效ROS生成器!这项《自然通讯》最新研究首次揭示,通过调控铁原子配位环境,使材料活性暴增百倍——在酸性条件下,它不仅能极速降解污染物,更能精准引爆癌细胞内活性氧,致死率飙升。颠覆性机制破解了纳米酶催化路径调控难题,为环境治理与肿瘤治疗开辟全新赛道。180字内读懂:如何让“老材料”释放“新杀伤力”?
— 内容由好学术AI分析文章内容生成,仅供参考。
(通讯员 王管诚)近日,《Nature Communications》(《自然通讯》)以“Steering H2O2 lysis pathway for ROS generation in Prussian blue nanozymes via alkali cation doping(碱阳离子掺杂调控普鲁士蓝纳米酶裂解过氧化氢途径生成活性氧)”为题在线发表了东南大学生物科学与医学工程学院张宇教授团队的最新研究成果。该研究首次通过配位工程实现了普鲁士蓝纳米酶(PBNPs)从“ROS清除”到“ROS生成”的性能转变,揭示了普鲁士蓝表面Fe配位环境对H2O2裂解通路的关键影响,为纳米酶催化机制及其在环境与生物医学中的应用提供了新的思路。
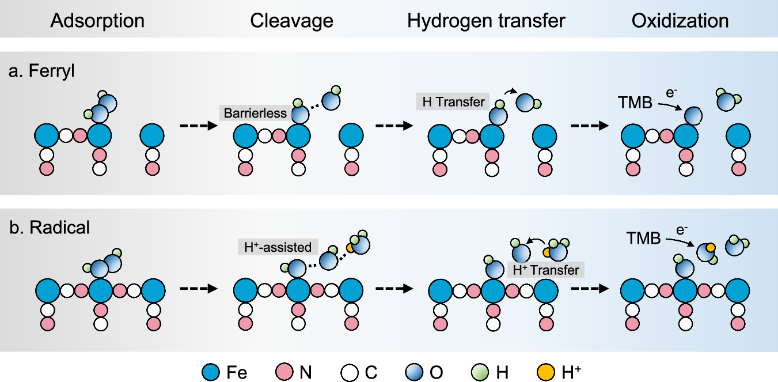
普鲁士蓝作为一类重要的铁基纳米酶,具有独特的羟基自由基(·OH)清除特性,广泛应用于抗氧化治疗。然而,这种特性与多数铁基纳米酶通过经典芬顿路径存在显著差异,其是否具备自由基生成能力仍缺乏实验证据。作者通过理论预测发现高配位的Fe中心在酸性环境下可引导H2O2发生均裂反应,生成·OH自由基,从而赋予PBNPs强氧化能力。为此,采用碱金属离子掺杂策略(以Cs+为代表)以增强晶格有序性、提升高配位Fe(FeN6)位点比例,并成功在材料结构层面诱导反应通路从非自由基到自由基的切换。
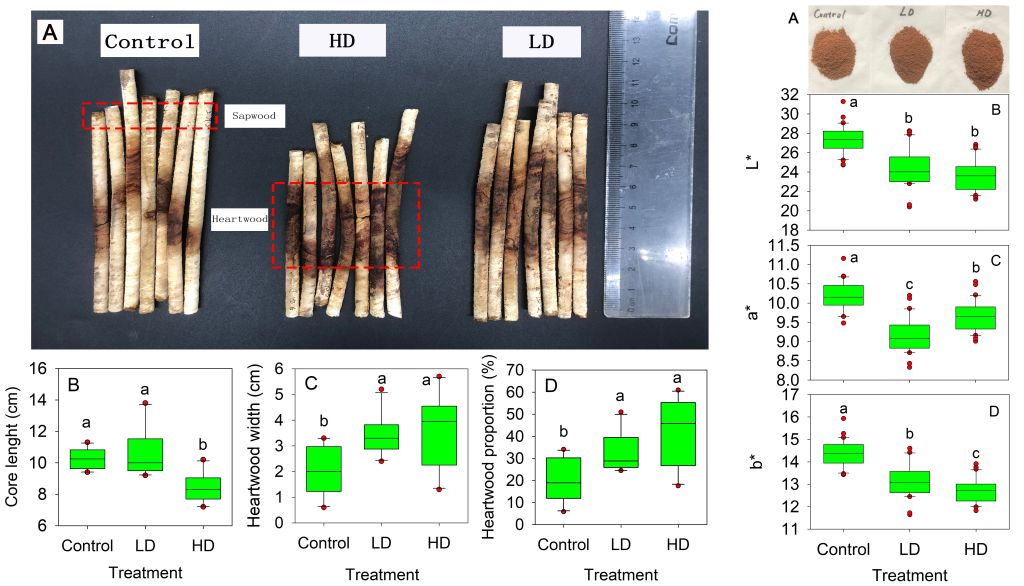
在催化性能测试中,掺Cs的普鲁士蓝纳米酶展现出显著提升的类过氧化物酶样活性,比活性较未掺杂材料提升两个数量级。在应用层面,该材料在酸性条件下实现了甲基蓝高效降解及乳腺癌细胞内诱导ROS生成、细胞存活率显著下降的效果,体现出在环境与生物医学领域的广泛潜力。该项工作为纳米酶的功能调控与机制理解提供了新的思路,也为其向高级氧化催化、肿瘤治疗等应用方向奠定了基础。
东南大学生物科学与医学工程学院博士研究生王管诚和博士后魏小丽为论文共同第一作者,武昊安教授、马明教授和张宇教授为共同通讯作者。研究得到了国家重点研发计划、国家自然科学基金等项目以及东南大学数字医学工程全国重点实验室和东南大学量子材料与信息器件教育部重点实验室的支持。
论文链接:https://doi.org/10.1038/s41467-025-64610-9
供稿:生物科学与医学工程学院
(责任编辑:嵇宏 审核:李震)
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。




















张宇团队又发顶刊了,东大生物医学果然厉害💪
好奇碱金属掺杂的具体机制,希望有更详细的科普
从抗氧化到产生活性氧,这个转变思路真是巧妙👍
这个研究成果太牛了,纳米酶应用前景广阔啊!