文章导读
你是否知道,合成具有两个相邻手性中心的非天然α-氨基酸有多难?武汉大学王春江/董秀琴教授团队给出颠覆性方案——通过Cu/Ru双金属接力催化,从惰性烯丙醇出发,一锅法高效构建δ-羟基α-氨基酸衍生物,产率高、选择性优异,过程绿色且省时。这不仅解决了传统方法依赖大量氧化还原试剂的痛点,更为生物活性分子如脯氨酸和L-吡咯赖氨酸的合成开辟了全新路径。前沿催化技术+绿色化学理念,带你看清复杂手性分子合成的未来方向。
— 内容由好学术AI分析文章内容生成,仅供参考。
(通讯员化苑)近日,《美国化学会志》(J. Am. Chem. Soc.)刊发了武汉大学化学与分子科学学院王春江/董秀琴团队关于双金属Cu/Ru接力催化合成手性δ羟基α-氨基酸衍生物的最新研究论文,题为“Asymmetric Access to δ‑Hydroxy α‑Amino Acids Bearing Two Adjacent Stereocenters from Inert Allylic Alcohols Via Cu/Ru Relay Catalysis”(通过铜/钌接力催化从惰性烯丙醇出发合成含有两个相邻手性中心的δ-羟基α-氨基酸衍生物)。武汉大学化学与分子科学学院博士研究生熊祺为论文第一作者,王春江教授和董秀琴教授为论文通讯作者,武汉大学化学与分子科学学院为第一署名单位。
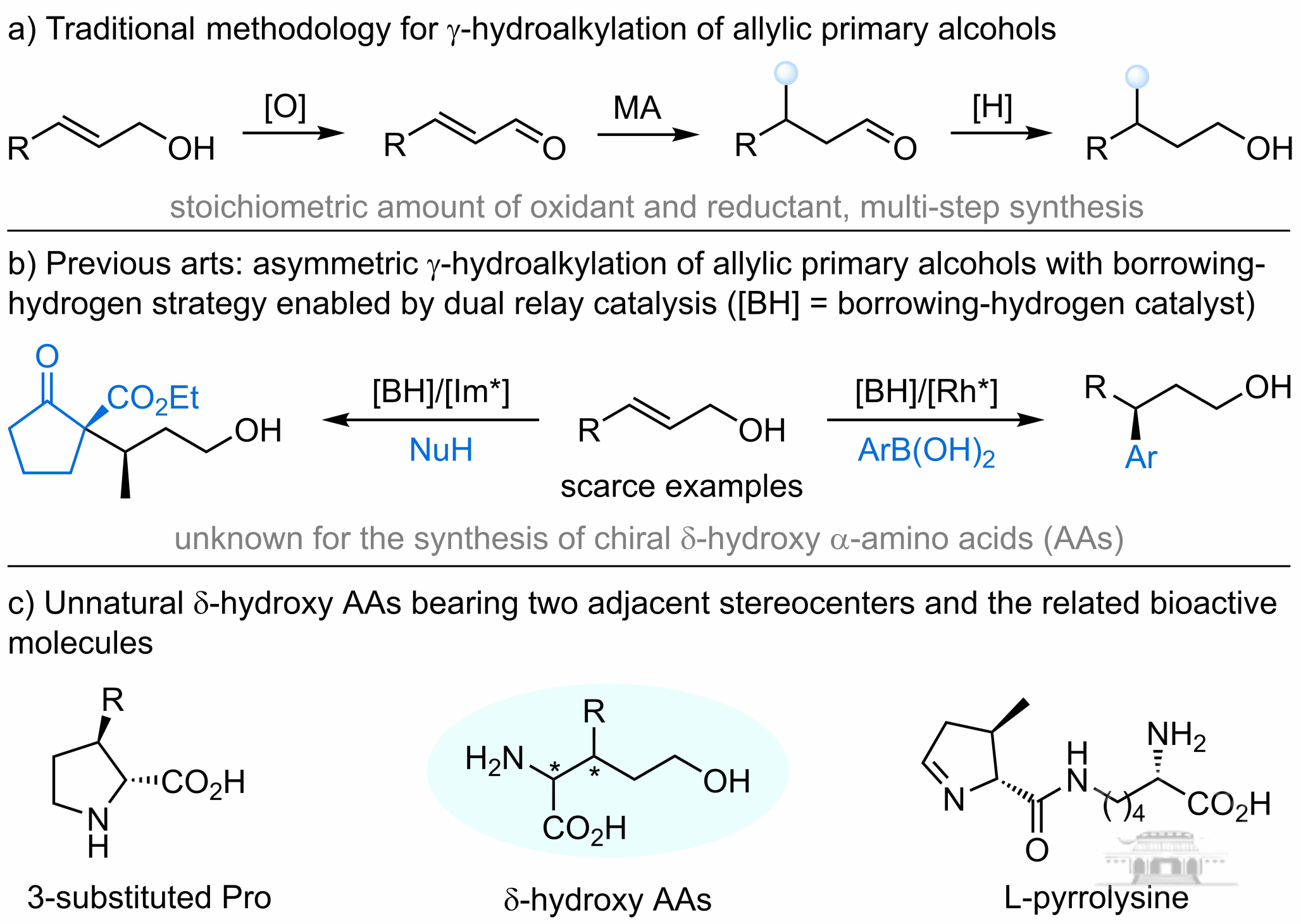
开发高效方法将简单醇转化为结构多样性手性分子,是有机合成化学的研究热点之一。其中,烯丙醇的氢官能团化是合成γ-官能团化高附加值醇的重要策略。传统分步路线所涉及的氧化、加成及还原串联合成法存在许多局限性,需使用化学计量的氧化剂和还原剂,原子经济性低,后处理复杂并产生大量的废弃物,不符合绿色化学理念。接力催化策略为复杂分子结构的快速构建提供了高效的解决方案。该策略通过将多步分离过程整合为”一锅法”串联反应,不仅避免了繁琐的中间体纯化步骤,显著提高了合成效率,同时大幅减少了有机溶剂消耗和废弃物产生,完美契合步骤经济性和绿色化学原则。
最近,借氢催化(hydrogen-borrowing catalysis)作为一种新型接力催化模式,以其优异的原子经济性和操作简便性,为从简单醇出发高效构建手性分子提供了新思路。该方法通过将烯丙醇瞬时转化为反应活性更高的α,β-不饱和醛或酮中间体,实现了惰性醇类化合物无法实现的多种不对称转化。近年来,王春江/董秀琴团队在Cu/Ru双金属接力催化领域取得了一系列代表性成果,主要聚焦于非天然α-氨基酸的构建(Angew. Chem. Int. Ed.2022,61, e202206517;Angew. Chem. Int. Ed.2024,63, e202315325;Chem. Sci.2024,15, 10135;Chem. Sci.2025,16, 1233;J. Am. Chem. Soc.2025,147, 5014)。非天然手性δ-羟基α-氨基酸(α-AAs)在有机合成中可作为关键中间体用于构建重要生理活性手性分子,该课题组设想能否通过接力催化策略从简单的烯丙基伯醇出发实现手性δ-羟基α-氨基酸的快速构建。
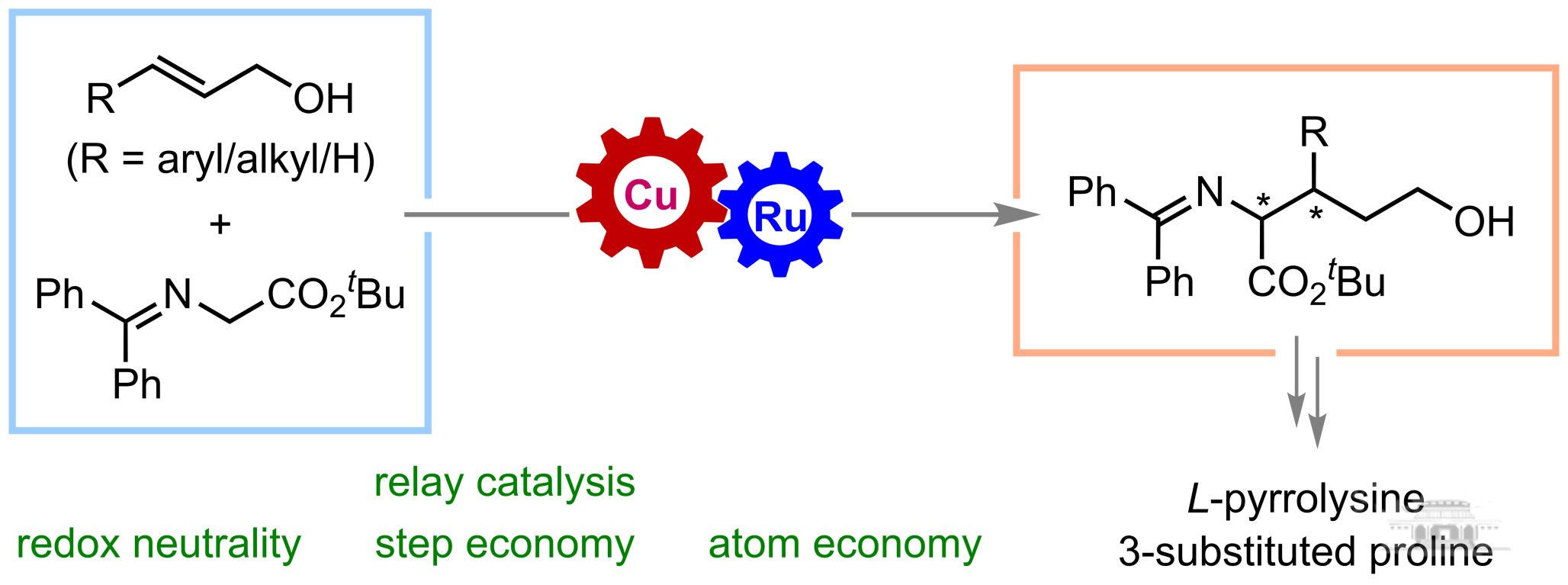
基于δ-羟基α-氨基酸衍生物的合成重要性,王春江/董秀琴团队通过高效的双金属Cu/Ru接力催化体系实现惰性烯丙醇与二苯甲酮衍生的酮亚胺酯之间的借氢/不对称迈克尔加成/氢化还原的不对称串联反应,成功实现了具有两个相邻叔碳手性中心δ-羟基α-氨基酸衍生物的高效合成,获得良好到高的产率、优异的非对映体选择性和对映体选择性。值得注意的是,该策略具有操作简单、优异的原子经济性和步骤经济性、广泛的底物耐受性和氧化还原中性等优点,同时避免了中间产物的纯化。在合成应用方面,该方法不仅成功实现了克级规模制备,还能通过简单的衍生化反应高效构建多种重要骨架结构,其中包括脯氨酸和L-吡咯赖氨酸的关键中间体,为这类重要生物分子的合成提供了更为简洁高效的途径。
该研究受到了国家重点研发计划(2023YFA1506700)、中央高校基本科研业务费专项资金(2042025kf0032)、国家自然科学基金委项目(22271226、22371216)的资助。论文其他合作者包括武汉大学化学与分子科学学院博士生陈博斌。
全文链接:https://pubs.acs.org/doi/10.1021/jacs.5c07896
(供图:化学与分子科学学院 编辑:赵冀帆)
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...