中国农业大学|动物医学院杨汉春团队揭示伪狂犬病病毒致脑损伤新机制
文章导读
伪狂犬病病毒不仅威胁养猪业,近年来新出现的变异株还能感染人引发脑炎。但病毒如何损伤大脑?此前科学界并不清楚。中国农业大学杨汉春团队最近揭开了这个谜底——损伤不是病毒直接造成的,而是触发了一种叫“铁死亡”的程序性细胞死亡方式。研究证实,PRV感染激活铁蛋白自噬,导致细胞内铁过载,进而引发脂质过氧化和神经炎症。更有意义的是,铁死亡抑制剂竟然能有效降低病毒滴度、减轻脑损伤。这意味着什么?如果你是兽医或研究者,这条“铁死亡-神经炎症”调控轴可能为PRV相关脑炎提供全新的治疗靶点;
— 内容由好学术AI分析文章内容生成,仅供参考。
4月28日,中国农业大学动物医学院、兽医公共卫生安全全国重点实验室、农业农村部动物流行病学重点实验室杨汉春教授国家级创新团队在《美国国家科学院院刊》(Proceedings of the National Academy of Sciences)在线发表研究论文《伪狂犬病毒通过铁自噬介导的铁死亡和神经炎症触发病毒性脑炎》(Pseudorabies Virus Triggers Ferritinophagy-Mediated Ferroptosis and Neuroinflammation in Viral Encephalitis)。
该研究聚焦伪狂犬病病毒感染引发的中枢神经系统损伤,揭示了铁蛋白自噬介导的铁死亡在病毒性脑炎发生发展中的关键作用,阐明了其促进神经炎症反应的分子机制,为伪狂犬病病毒相关神经系统疾病的机制研究和靶向干预提供了新的理论依据。
伪狂犬病病毒(PRV)属于α疱疹病毒亚科,主要感染猪,是危害养猪业的重要病原。近年来,新出现的PRV变异株可感染人,主要引起脑炎等严重神经系统疾病,提示其具有潜在的人兽共患风险及公共卫生意义。铁死亡是近年来发现的一种程序性细胞死亡方式,已被证实参与多种神经退行性疾病和病毒感染的发生发展过程。然而,PRV是否能够在中枢神经系统中诱导铁死亡,以及其参与病毒性脑炎发生的确切机制仍不清楚。
该研究围绕“铁蛋白自噬-铁死亡-神经炎症”调控轴,系统解析了PRV感染导致脑损伤的分子机制。研究发现,PRV感染可在N2a细胞、小鼠原代神经元以及小鼠脑组织中诱导铁死亡;PRV感染能够激活铁蛋白自噬,促进细胞内游离铁水平升高,进而诱发脂质过氧化,最终驱动铁死亡发生;通过转录组学与代谢组学联合分析证实,PRV感染诱导的铁死亡可通过PTGS2/PGE2通路促进神经炎症发生(图1)。
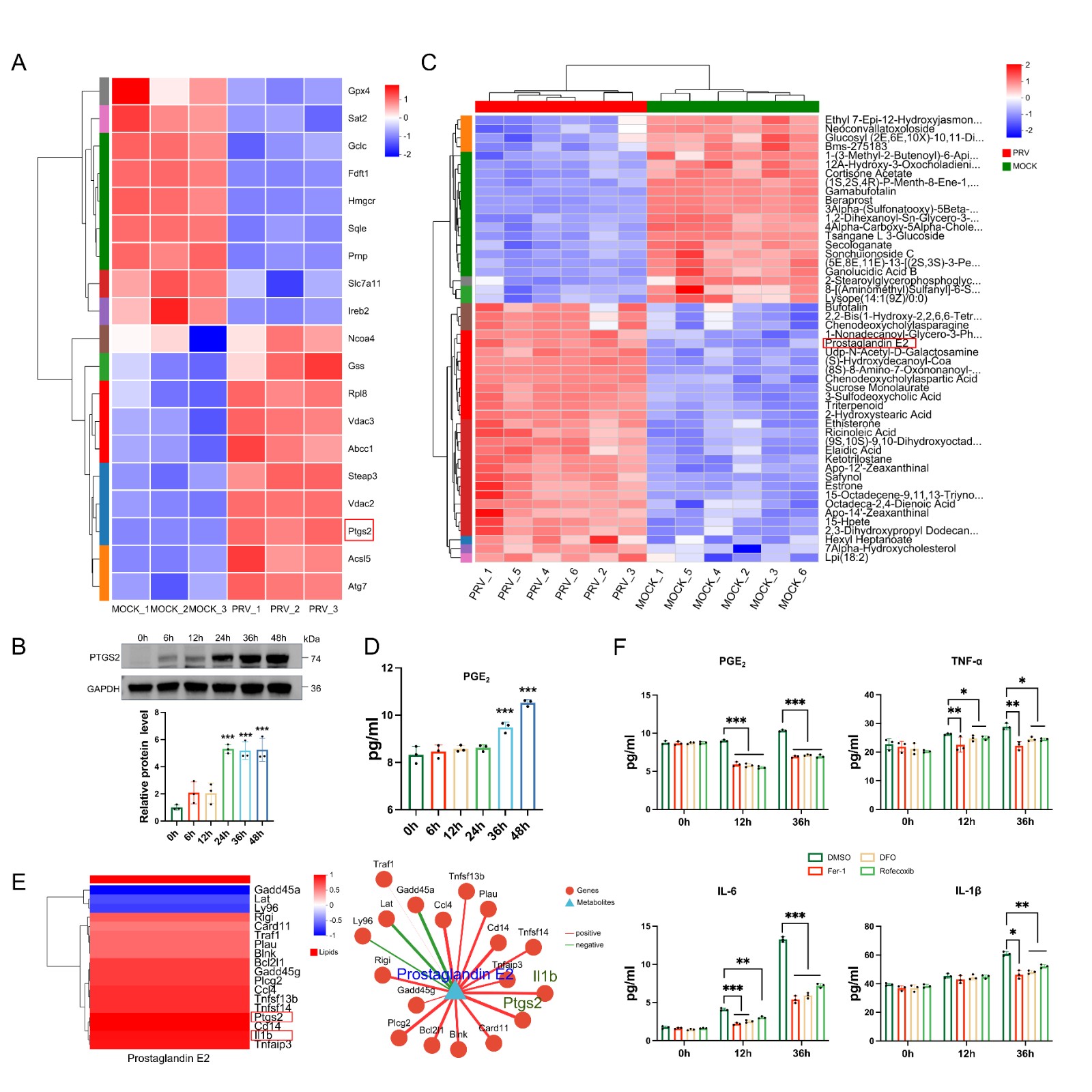
图1 铁死亡激活PTGS2/PGE2通路促进PRV诱导的神经炎症反应
PRV感染小鼠脑组织中游离铁水平和脂质过氧化程度明显升高,并伴随显著的神经炎症反应和脑组织病理损伤。铁死亡抑制剂去铁胺(DFO)可有效缓解PRV感染诱导的铁死亡,降低小鼠脑组织中的病毒滴度,并减轻病毒性脑炎相关病理损伤(图2)。
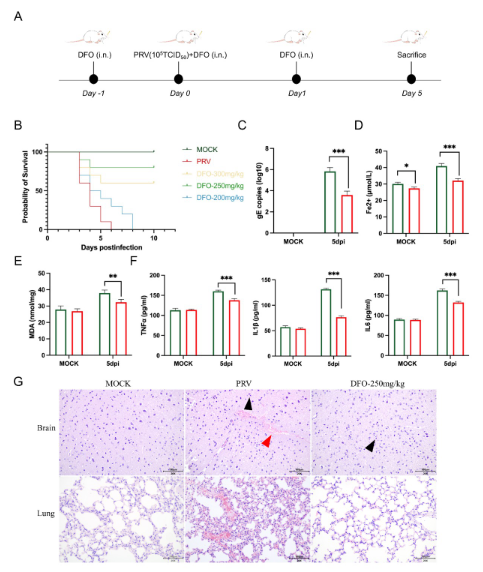
图2 铁死亡抑制剂DFO对PRV感染小鼠的治疗作用
该研究从铁代谢异常与程序性细胞死亡交叉调控的角度,揭示了PRV感染引发中枢神经系统损伤的新机制,明确了铁蛋白自噬介导的铁死亡及PTGS2/PGE2炎症通路在病毒性脑炎中的重要作用,为PRV相关神经系统疾病的防控和治疗提供了新的理论基础与潜在靶点(图3)。
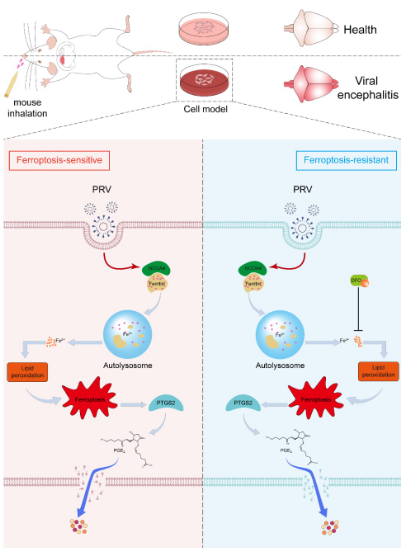
图3 铁死亡介导PRV诱导脑炎机制示意图
动物医学院在读博士研究生孙佳丽为论文第一作者,胡艳欣教授和杨汉春教授为论文通讯作者。该研究得到国家自然科学基金重点项目(32330106)、国家自然科学基金面上项目(32372966, 32172829)、国家生猪产业体系专项基金(CARS-35)和中国农业大学“2115人才培养计划”等项目的资助。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。















这机制听着挺复杂,铁死亡是啥?