文章导读
面对“女性出生后卵子不再新生”的百年定论,你是否曾以为卵巢早衰或不孕症只能被动接受?上海交大团队最新发现彻底颠覆了这一认知:一种名为 ac4C 的微小化学修饰,竟像隐形开关般精准操控着雌性生殖干细胞的命运。研究揭示,一旦缺失这个关键修饰,干细胞库将迅速枯竭,直接导致卵巢功能崩溃。这不仅是分子机制的突破,更意味着未来治疗不孕症可能无需依赖传统激素,而是通过靶向这一全新通路实现逆转。当科学界还在争论干细胞来源时,这条被忽略的"ac4C-Gm26917"调控轴,是否已经为无数家庭埋下了重获生育希望的伏笔?
— 内容由好学术AI分析文章内容生成,仅供参考。
本世纪初,吴际教授团队首次从出生后哺乳动物卵巢中分离出雌性生殖干细胞(FGSCs)并率先揭示其具有自我更新和分化潜能的雌性生殖干细胞(FGSCs)。这一发现打破了“出生后不再产生新卵母细胞”的百年传统认知,为女性不孕、卵巢早衰、多囊卵巢综合征等疾病治疗、生育力保存、动物繁殖和再生医学等开辟新途径。那么,FGSCs究竟遵循怎样的“指令”?为什么有的能保持自我更新,有的却走向分化或凋亡?解开这个谜题,不仅关乎女性生育能力的维持,更将为精准干预干细胞命运、治疗生殖相关疾病提供重要的理论基础。

2026年3月17日,上海交通大学Bio-X研究院吴际教授团队在Advanced Science在线发表题为“N4-acetylcytidine in LncRNA Gm26917 Promotes Translation in Female Germline Stem Cells by Recruiting Ribosomal Protein mRNA via EEF1A1”的研究论文。本研究首次揭示了一条调控FGSCs命运的全新分子机制:ac4C修饰增强LncRNA Gm26917的稳定性,促进其与Rpl10 mRNA的原位互作,进而增强Rpl10 mRNA的稳定性,使蛋白量增多,最终上调整体翻译效率,决定干细胞的增殖、分化与凋亡命运。研究也在小鼠体内验证了其生理意义-敲除ac4C修饰酶NAT10直接导致卵巢内FGSCs减少、卵巢发育受损。此外,研究还发现EEF1A1蛋白作为RNA结合蛋白介导了Gm26917-Rpl10互作,为这一调控轴增添了关键的分子桥梁。综上,本研究发现lncRNA上ac4C修饰调控其与mRNA的空间互作,阐明了一个新的ac4C-Gm26917-EEF1A1-Rpl10调控轴在FGSCs维持中的作用。
在该研究中,研究人员首先发现ac4C的修饰在FGSC分化过程中的动态调节,对其稳态维持至关重要。分化伴随的ac4C水平下降(通过NAT10抑制得以重现),以及ac4C对基因的双向调控效应(在下调基因中降低,在上调基因中升高),提示在FGSCs稳态维持过程中存在一个调控ac4C动态变化的复杂网络。
进一步研究发现,ac4C修饰参与RNA-RNA互作调控。其中关键互作对Gm26917-Rpl10可影响RPL10蛋白的表达量。RPL10作为细胞内蛋白质合成的“装配工人”,参与整个细胞的“翻译效率”调控。从RNA修饰到RNA稳定性,再到蛋白质合成速率,精准地调控着FGSCs的增殖、分化、凋亡等关键生命活动。
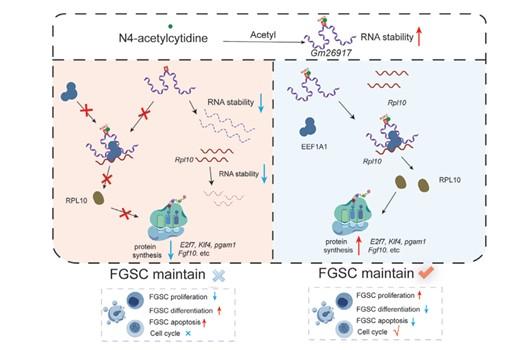
图示 ac4C对FGSC命运的转译调控
为验证这一机制在生理条件下的真实性,研究团队在小鼠模型中进行了体内验证。结果显示:敲除ac4C修饰酶NAT10后,由其调控的Gm26917-Rpl10互作减弱,小鼠卵巢内雌性生殖干细胞的数量显著减少,卵巢的正常发育遭到破坏。 这一发现直接证明了ac4C修饰在维持FGSCs细胞池和卵巢功能中的不可或缺性。深入了解互作的分子机制,发现EEF1A1蛋白扮演了“分子桥梁”的角色,确保LncRNA Gm26917与Rpl10顺利结合,从而保证这一调控通路的顺畅运行。
综上,本研究层层递进,从RNA修饰到RNA稳定性,再到RNA-RNA原位互作,最终到翻译效率,揭示了调控FGSCs发育的全新机制。研究发现的ac4C-Gm26917-EEF1A1-Rpl10调控轴,为干预卵巢功能、治疗不孕症提供了潜在的药物靶点。此外,研究还提出了一个有趣的展望:部分RNA虽自身缺乏ac4C修饰,却可能通过与携带ac4C修饰的其他RNA发生相互作用,而受到间接调控,这一观点拓展了ac4C修饰功能研究的边界。
本论文的第一作者为李新月博士研究生。通讯作者为吴际讲席教授和胡晓鹏助理研究员。该研究得到了国家重点研发计划和上海市及上海交通大学(2030计划)的科研项目资助。
论文链接:https://doi.org/10.1002/advs.202520059
作者: Bio-X研究院 供稿单位: Bio-X研究院
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。

















小鼠实验的结果能直接推及人类吗?
所以ac4C是关键开关?
希望早点出应用成果,身边有朋友卵巢早衰
有人试过类似的研究方向吗?
看不懂但感觉很厉害的样子
要是能应用到临床就太好了
这个机制还挺复杂的,得消化消化