海洋多糖构建双靶向纳米载体用于结直肠癌治疗
文章导读
你手里可能刚看到有关新免疫药物的数据,却还在为“为什么肿瘤一边对药物敏感一边又像铁墙”苦恼。大多数肿瘤递送系统只盯着癌细胞,却忽略了那片沉睡的肿瘤免疫微环境——结果药物到了肿瘤却无法发挥应有杀伤力。这项来自海洋多糖的新方案把问题放在双重靶向上:既靠P‑选择素和生物素把药物精准押送到肿瘤,又在酸性微环境触发释放,同时激活免疫细胞并抑制血管生成,能把“冷肿瘤”悄悄变成“热肿瘤”。听起来像是把多项难题一锅端,但关键机制和能否真正改写临床受益还有两道未解的门槛,你准备好去看实验数据了吗?
— 内容由好学术AI分析文章内容生成,仅供参考。
褐藻多糖硫酸酯具有天然P‑选择素靶向性与免疫调节活性,是构建肿瘤靶向递送载体的理想天然高分子材料。
近日,中国科学院海洋研究所研究团队在结直肠癌治疗方面,构建了双靶向纳米载体(CS‑Arg/Fuc‑Bio@OF),用于同步递送奥沙利铂与呋喹替尼。该载体通过P‑选择素亲和与生物素受体双重主动靶向机制,实现了药物在荷瘤小鼠肿瘤部位的精准富集与酸性微环境响应释药。
该系统协同实现免疫原性细胞死亡、肿瘤相关巨噬细胞M1极化、抗血管生成三重作用,从而高效抑制肿瘤增殖转移,且展现出优异的生物安全性。
研究突破了传统纳米载体功能局限,将海洋多糖打造为集“靶向递送、药物控释、免疫激活”于一体多功能载体,为海洋生物资源高值化利用与抗肿瘤创新药物研发提供重要实验支持。
相关研究成果发表在Carbohydrate Polymers上。研究工作得到国家自然科学基金、中国博士后科学基金等的支持。
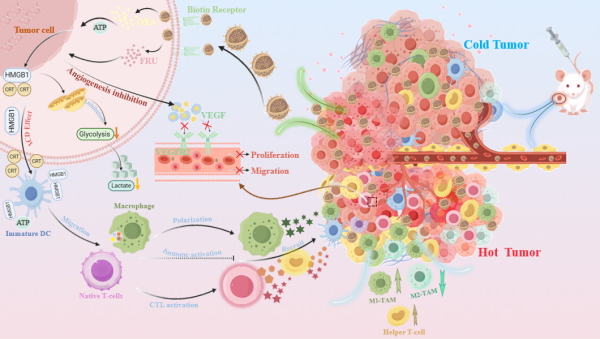
双靶向纳米递送系统CS-Arg/Fuc-Bio@OF的构建及其在结直肠癌治疗中的应用
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。




















这实验结果看着挺靠谱,就是不知道离临床还有多远。