科学家实现mRNA体内精准靶向递送
文章导读
你是否以为mRNA疫苗的瓶颈只在于序列设计?实际上,90%的研发困局藏在递送系统里——传统脂质纳米颗粒(LNP)要么效率低下,要么只能被动聚集在肝脏。我们发现,中科院团队最新突破的关键,不是改进化学成分,而是让AI学会了“看”三维结构。他们把脂质分子的动态空间构象转化为图像数据,训练出能精准预测溶酶体逃逸能力的模型,首次实现非肝靶向的高效递送。这种新LNP构建的mRNA肿瘤疫苗,在小鼠体内不仅激活了双重免疫应答,还建立起长期防护。但最令人震惊的不是疗效,而是这套AI模型正在重新定义药物递送的设计逻辑——当别人还在拼化学结构时,这场竞赛已经悄然升级到了三维空间维度,你准备好面对这场变革了吗?
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,中国科学院国家纳米科学中心成功创建了一种基于脂质空间构象的人工智能(AI)全新模型,通过精准解析可电离脂质的三维空间构象,成功攻克了脂质纳米颗粒(LNP)在mRNA药物递送中存在的转染效率低下与难以精准靶向两大难题,为下一代mRNA疗法的发展开辟了新路径。
传统LNP设计和AI模型构建多聚焦于可电离脂质的二维化学结构,团队首次将可电离脂质的空间构象引入AI模型,通过构建可电离脂质分子文库,并利用分子动力学模拟等技术勾勒分子动态3D构象,将数据转化为二维密度图像用于AI模型构建。优选后的AI模型成功筛选出转染效率更高、且具有器官靶向功能的新LNP。
在应用验证层面,团队利用优选的LNP构建的mRNA肿瘤疫苗在黑色素瘤小鼠模型中展现出显著治疗效果。试验结果表明,该mRNA疫苗成功激活了强效T细胞免疫应答,并诱导高水平特异性抗体产生,实现体液免疫与细胞免疫的双重激活,有效抑制肿瘤生长,并为小鼠提供了长期免疫保护。
研究首次将可电离脂质的设计逻辑从“二维化学结构”的经验摸索,拓展至“三维空间构象”的AI精准解析及预测。研究不仅解析了可电离脂质在mRNA递送过程中实现溶酶体逃逸的核心分子机制,也成功突破mRNA药物的肝外器官靶向递送难题,为基因编辑、蛋白替代疗法、体内CAR-T治疗等前沿领域提供了兼具高效性与安全性的递送解决方案。
相关研究成果发表在《自然-生物医学工程》(Nature Biomedical Engineering)上。研究工作得到国家重点研发计划、国家自然科学基金、北京市自然科学基金、京津冀基础研究合作专项项目等的支持。
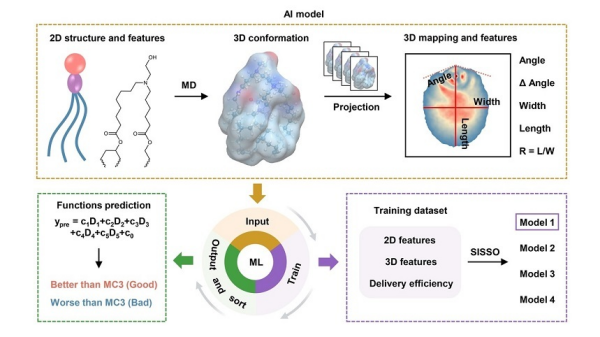
可电离脂质AI预测模型构建
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。



















又是高大上的科研,普通人听着头大。
我之前做过LNP改造,感觉空间构象真的影响大。
这个模型对黑色素瘤的免疫提升到底有多强?
这个新LNP听起来真牛,期待看看实际效果。