西北农林科技大学(816)动科学院肌肉生物学与生猪遗传改良创新团队揭示肠道菌群代谢物3-PPA通过肠道-免疫-脂肪祖细胞互作驱动米色脂肪生成和能量消耗的分子机制
文章导读
你是否以为猪的脂肪沉积只和饲料营养有关,却忽略了肠道里那个看不见的“开关”?当所有人都在死磕配方时,西北农林科技大学的最新发现却颠覆了认知:一种由普雷沃氏菌产生的代谢物3-PPA,竟能直接激活免疫细胞,指挥脂肪祖细胞转化为产热的米色脂肪。这意味着,冷适应的关键不在保暖,而在菌群调控。但这套复杂的“肠道 - 免疫 - 脂肪”轴究竟如何精准运作?如果把它变成饲料添加剂,能否让生猪在低温下依然保持高效生长而不长肥膘?答案就藏在这篇《Cell Metabolism》论文里。
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,动科学院肌肉生物学与生猪遗传改良创新团队袁业现教授课题组在国际知名期刊《Cell Metabolism》在线发表题为“Microbial-derived 3-phenylpropionic acid orchestrates immune–progenitor cell crosstalk to promote beige adipogenesis and energy expenditure”的研究论文。西北农林科技大学袁业现教授、吴江维教授和美国伊利诺伊大学芝加哥分校Yuwei Jiang教授为共同通讯作者。动科学院在读博士生李德富、青年教授夏博、伊利诺伊大学芝加哥分校Ruoci Hu为共同第一作者。
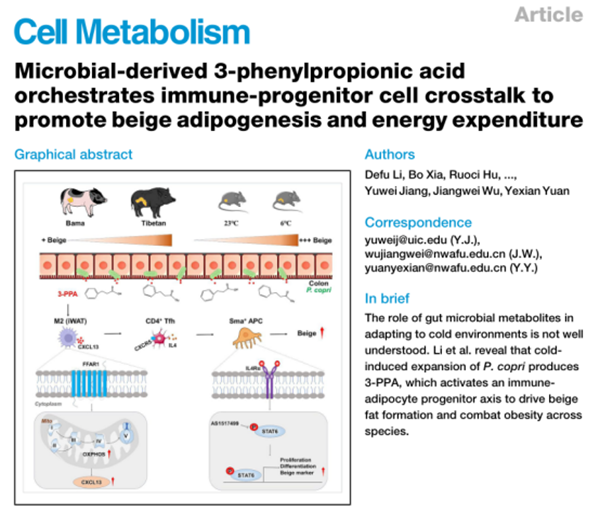
该研究鉴定出一种在冷暴露条件下显著富集的肠道微生物代谢物—3-苯基丙酸(3-PPA),其主要由肠道普雷沃氏菌(Prevotella copri)产生。为了验证3-PPA在猪冷适应中的关键作用,研究比较了耐寒藏猪与寒冷敏感巴马猪在冷暴露前后的3-PPA代谢变化。结果显示,冷暴露前藏猪血清和结肠组织中的3-PPA水平显著高于巴马猪,随着冷暴露时间增加(3d),藏猪和巴马猪结肠与血清中3-PPA水平显著升高,且藏猪3-PPA水平仍显著高于巴马猪。此外,3-PPA处理猪原代脂肪细胞发现,其能够上调产热相关基因(UCP3, CIDEA, DIO2)的转录和产热关键蛋白UCP3的表达,表明3-PPA具有调控猪脂肪代谢作用。
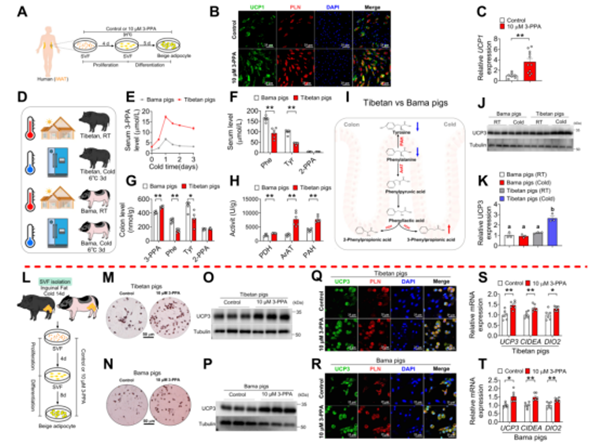
机制上,3-PPA通过作用于米色脂肪组织内M2样巨噬细胞膜上的游离脂肪酸受体1(FFAR1),刺激其分泌C-X-C基序趋化因子13(CXCL13)。CXCL13进而招募T滤泡辅助细胞(Tfh),并通过Tfh细胞表面的C-X-C 趋化因子受体5(CXCR5)信号,促进白细胞介素-4(IL-4)的分泌,最终调控米色脂肪细胞的生成。通过谱系追踪分析,进一步证实3-PPA诱导产生的米色脂肪细胞主要来源于平滑肌肌动蛋白阳性(SMA+)的脂肪祖细胞。
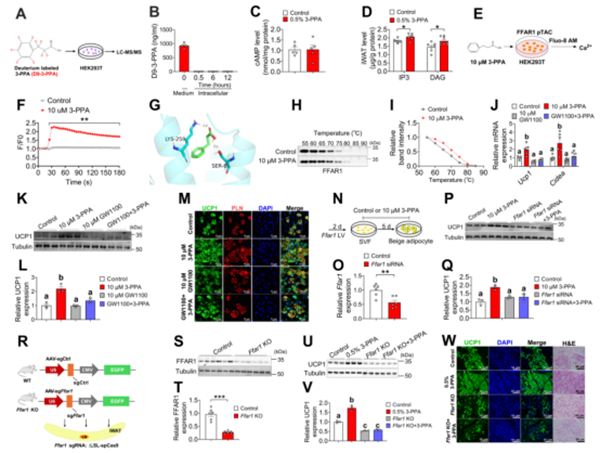
综上,该研究揭示了一条由肠道微生物代谢物3-PPA驱动,经免疫细胞(巨噬细胞-Tfh)介导,最终调控脂肪组织代谢的肠道-免疫-脂肪轴。研究结果不仅有效解析肠道菌群调控脂肪沉积的分子机制,也为研发新型调控脂肪沉积的饲料添加剂提供研究参考。
该研究得到国家自然科学基金(32302827)、国家生猪产业技术体系(CARS-35-PIG)等项目资助。
论文链接:https://www.sciencedirect.com/science/article/pii/S1550413126000197
编辑:张晴
终审:刘玉峰
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
















猪的脂肪细胞和人的一样吗
肠道-免疫-脂肪轴这个概念挺新的
能不能用在人体减肥上啊
研究团队挺厉害的,发在Cell Metabolism上
之前养过猪,确实品种不同耐寒性差很多
这个发现对养猪业应该有帮助
脂肪代谢好复杂,看晕了😵
有人试过补充这种代谢物吗
藏猪比巴马猪耐寒是因为3-PPA水平高啊
这研究挺有意思的,肠道菌群还能影响脂肪代谢🤔