研究发现H5N1病毒在牛群中获得增强哺乳动物致病性的关键突变
文章导读
H5N1禽流感病毒为何突然在牛群中暴发?科学家最新发现,病毒在跨种传播过程中,其PB2蛋白出现了关键突变M631L,能显著增强在哺乳动物细胞中的复制能力与致病性。研究证实,该突变可导致小鼠严重肺部感染甚至高死亡率,致病力堪比经典的E627K突变,且两者协同作用时危害更甚。中国科学院微生物研究所团队还发现多个新型适应性突变,揭示了病毒借助ANP32A/B宿主因子高效感染哺乳动物的分子机制。这一突破为评估H5N1大流行风险提供了关键依据,警示我们对牛群感染的监测或成防控新重点。
— 内容由好学术AI分析文章内容生成,仅供参考。
高致病性禽流感H5N1病毒在跨宿主传播过程中,其聚合酶蛋白适应性突变是影响病毒复制的关键因素,但学界对牛源H5N1病毒聚合酶发生哪些宿主适应性突变及其生物学功能尚不明晰。
近期,中国科学院微生物研究所研究团队,系统鉴定了H5N1病毒从禽向牛跨种传播过程中,其聚合酶PB2蛋白发生的哺乳动物适应性关键突变,揭示了突变通过增强病毒聚合酶对哺乳动物宿主因子ANP32A的利用效率,来提升病毒在哺乳动物中的复制水平与致病力。
研究发现,PB2蛋白是决定牛源病毒在哺乳细胞高效复制的关键因素,其中PB2 M631L突变可显著增强聚合酶活性。小鼠感染实验证实,携带PB2 M631L的病毒可引起严重肺部感染并导致高死亡率,其致病力与经典哺乳动物适应性突变PB2 E627K相当;当两者共存时,病毒致病力呈现协同增强效应。
研究进一步发现,H5N1病毒在持续传播过程中,除出现E627K、Q591R、D701N等已知突变外,还出现了I647V、G685R、K736R等多个新型适应性突变,这些突变均能增强病毒聚合酶在哺乳细胞中的活性。结构分析表明,这些突变通过增强对牛和人源ANP32A/B的利用效率,来提高病毒在哺乳动物体内的复制能力与致病性。
该研究为学界理解H5N1病毒在哺乳动物中的快速适应与进化提供了关键分子证据,揭示了PB2 M631L这一适应性突变位点的重要性,对科学评估H5N1病毒大流行风险及制定预警与防控策略具有重要参考价值。
相关研究成果发表在《自然-通讯》(Nature Communications)上。研究工作得到国家自然科学基金委员会、科学技术部、北京市科学技术委员会等的支持。
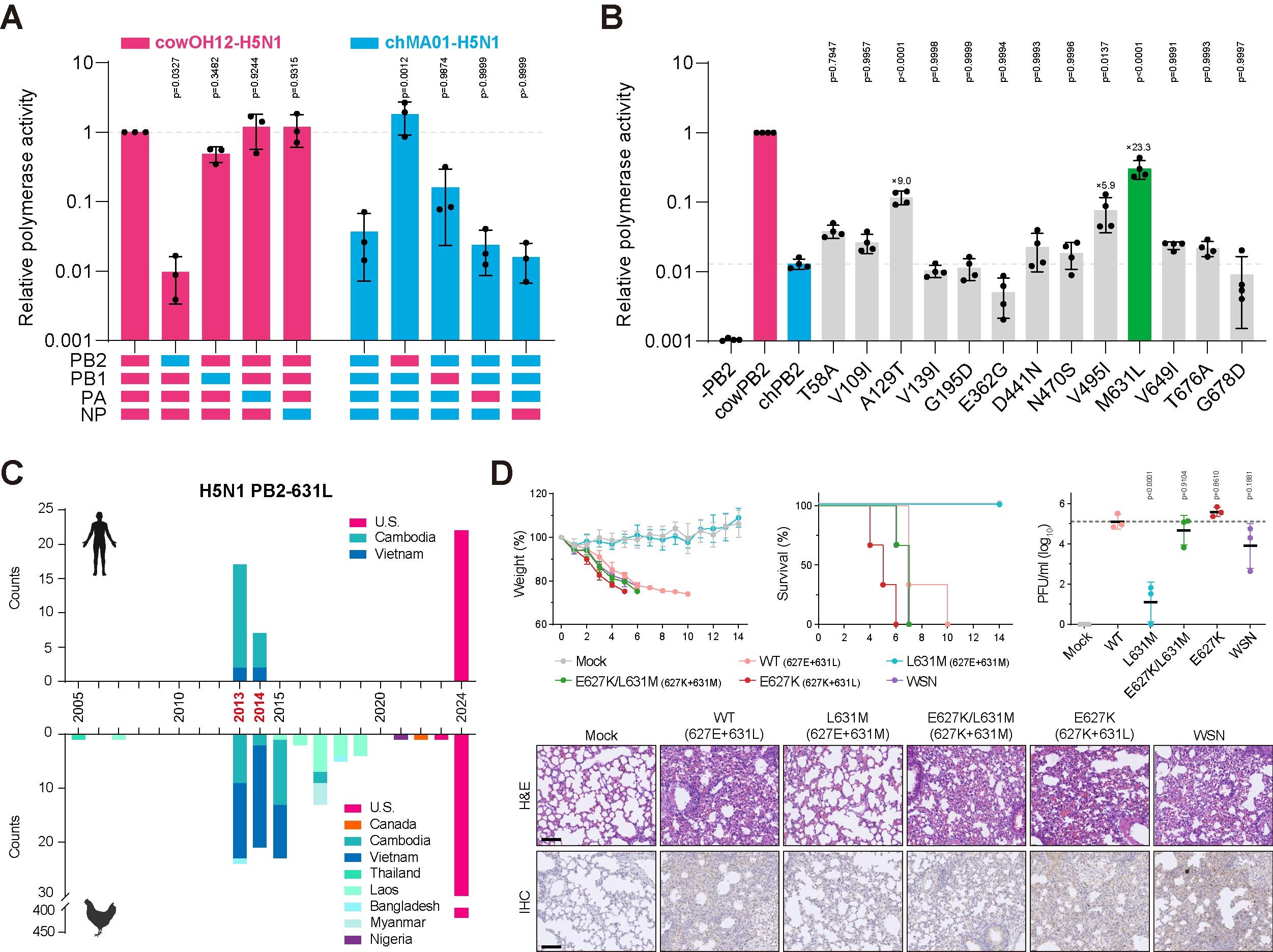
H5N1关键氨基酸突变PB2 M631L增强病毒复制能力和致病性
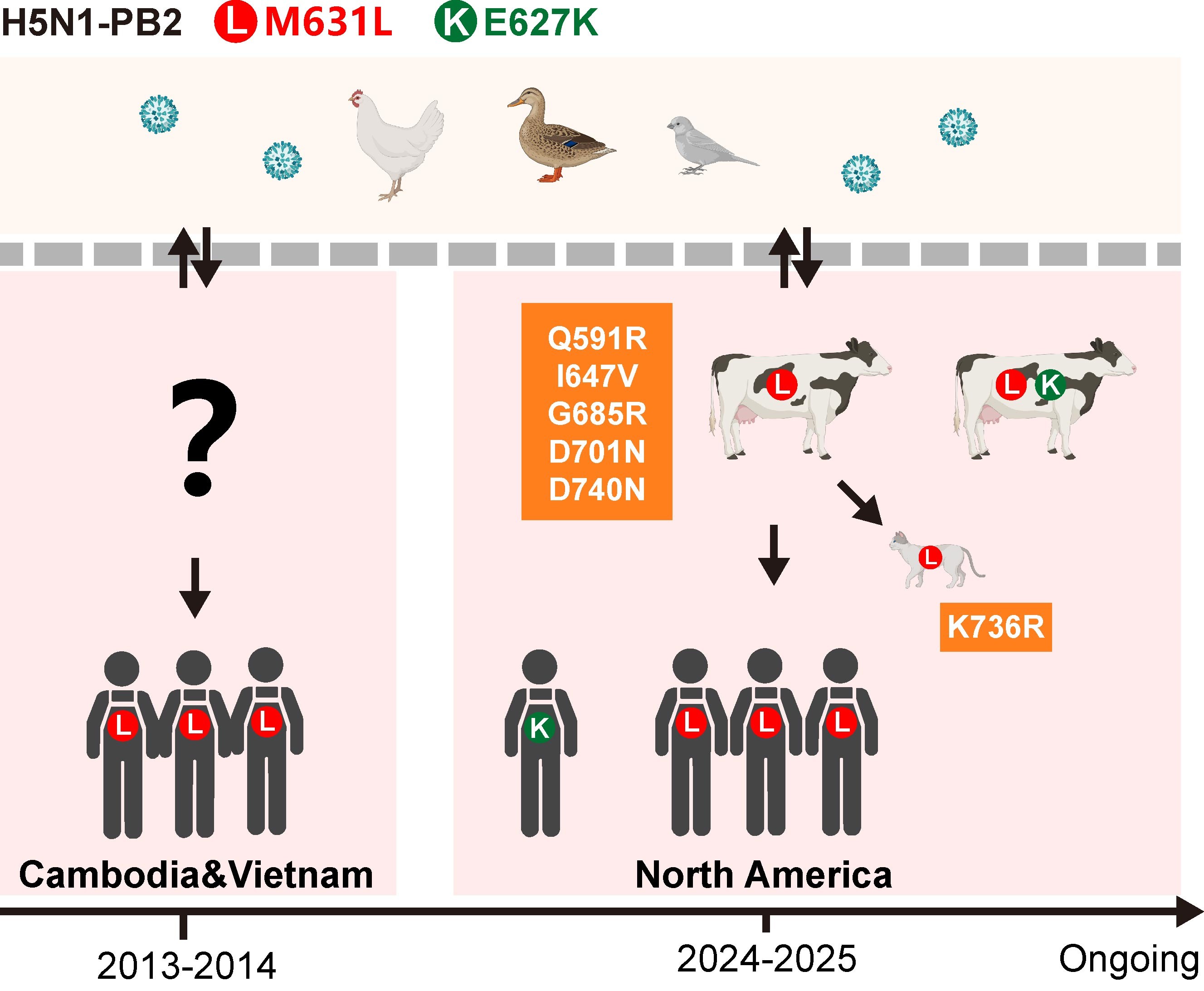
H5N1病毒聚合酶PB2蛋白关键突变参与病毒跨种传播
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。



















又是E627K又是M631L的,现在病毒进化速度是不是比我们研究还快?hhhhh
小鼠实验死亡率那么高,那要是传到人这边咋办?后续还会出现更强的变异吗?
前几天看新闻说奶牛也中招了,原来是因为这个ANP32A被利用了,难怪能跨种传播
这PB2 M631L突变听着挺关键啊,感觉危险性不小🤔