文章导读
腹主动脉瘤破裂致死率高达90%,却至今无药可防?南京大学魏辉教授团队带来颠覆性突破:一种超小型纳米酶OZn,不仅能精准靶向病灶、抑制动脉瘤扩张,更可通过尿液检测实现无创疗效监测。它“边治疗边反馈”,构建“诊断-治疗-监测”闭环系统,让不可预测的致命疾病变得可追踪、可干预。这项发表于《Science Advances》的研究,或将改写AAA临床管理格局,开启心血管疾病精准诊疗新纪元。
— 内容由好学术AI分析文章内容生成,仅供参考。
腹主动脉瘤(AAA)是老年常见致死性疾病,直径≥5.5cm无症状、症状性或破裂性AAA需手术,但外科修复创伤大、并发症多,且20%~30%血管内修复患者5年内需二次干预,增加风险。小型或解剖受限患者多采用保守监测,但AAA进展非线性、破裂风险高,管理困难。AAA破裂前常无症状,破裂后致死率高达85%~90%,患者长期面临心理压力与突发破裂风险,亟需延缓进展、降低破裂的药物方案。然而目前无有效药物抑制AAA进展或延迟破裂。AAA发病机制复杂,涉及炎症、血管壁扩张、氧化损伤等,其中氧化应激及过量ROS是早期进展关键因素,ROS调控成潜力靶点。降低ROS可缓解炎症、保护平滑肌细胞、维持细胞外基质完整性。天然抗氧化酶(如SOD、CAT)虽有效,但免疫原性强、成本高,限制临床应用,开发新型酶模拟物成新策略。
针对上述挑战,南京大学魏辉教授团队选择具有类酶诊疗特性的纳米酶作为早期干预AAA并进行无创疗效监测的新型策略。如图1所示,基于AAA特征性病理生理微环境,作者设计了一种ROS响应型靶向纳米诊疗体系。具体而言,超小尺寸的普鲁士蓝类似物(SPBZn)被包载于氧化敏感型聚合物中,构建诊疗了一体化OZn纳米酶。该纳米酶可被动靶向聚集于动脉瘤部位,并在炎症微环境刺激下释放出SPBZn纳米酶,通过其抗氧化效应有效抑制AAA进展。更重要的是,超小尺寸SPBZn可经肾脏代谢,并通过尿液分析实现无创诊断监测。这一特性使得OZn既可用于治疗AAA,又能通过尿液检测实时观察纳米酶的疗效,提供疾病状态的动态调控与实时反馈。该研究通过诊疗功能的协同整合,为AAA的临床管理提供了创新性解决方案,为非侵入性、可持续监测的精准治疗策略奠定了基础。
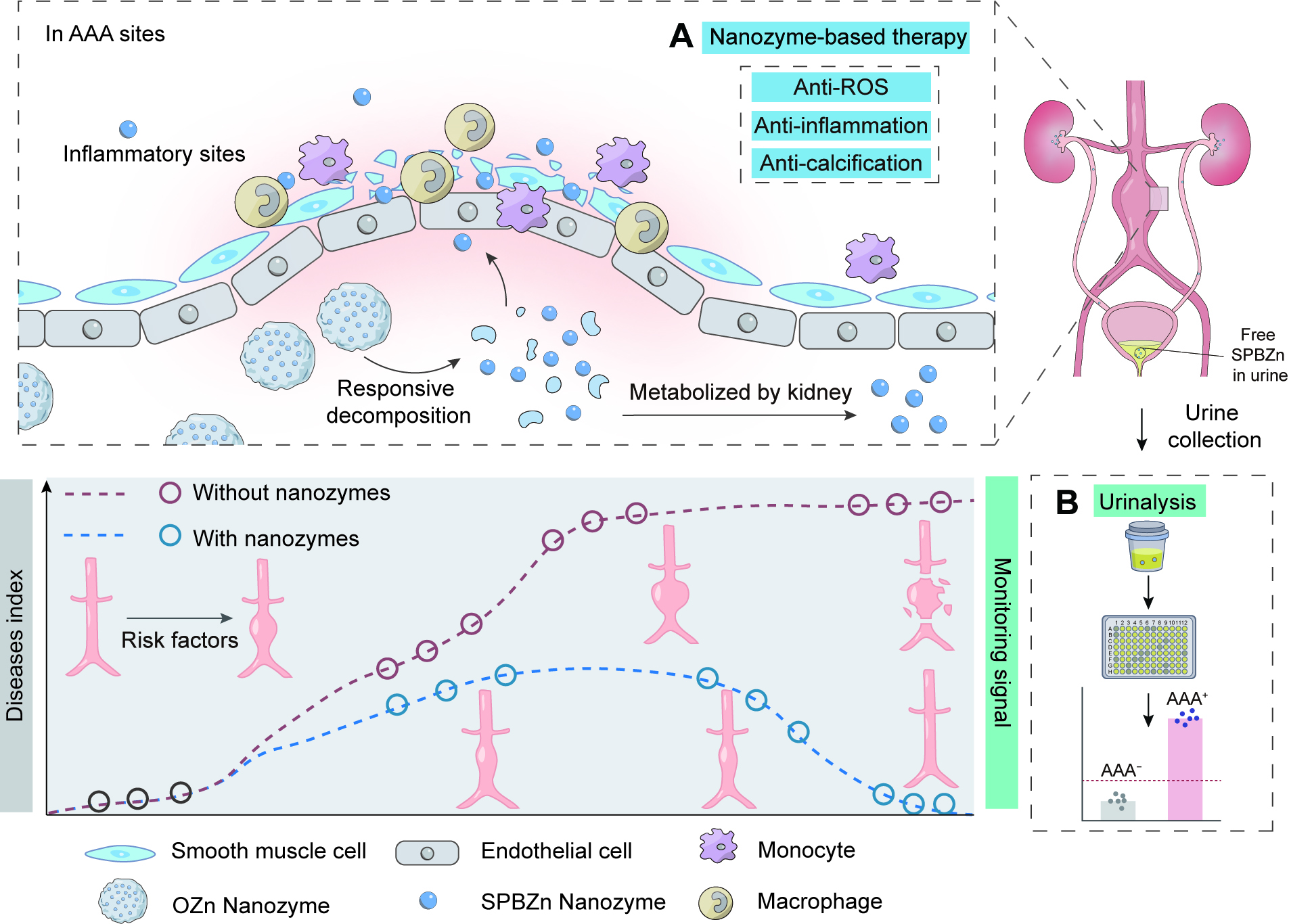
图1. 诊疗一体化纳米酶OZn用于腹主动脉瘤综合防治及疗效监测的作用机制示意图
为了制备可经肾脏代谢的超小纳米酶,作者选用了具有良好生物安全性的PB纳米酶作为核心材料,不仅因其优异的抗氧化活性,还因其独特的晶体结构使其具有尺寸可调性。基于此,作者合成了超小尺寸普鲁士蓝纳米酶和掺杂Zn2+的超小的PB类似物(SPBZn)。验证了SPBZn具有优异的抗氧化性能后,作者进一步设计了ROS响应型纳米酶体系SPBZn@Oxi-DEX(OZn)。OZn纳米酶具有ROS响应释放特性,在ROS的存在下,更快速地释放出具有抗氧化活性的SPBZn。这种特性使得OZn纳米酶在AAA的诊疗中具有潜在的优势,因为它能够根据病理环境ROS的水平调节其活性成分SPBZn的释放。
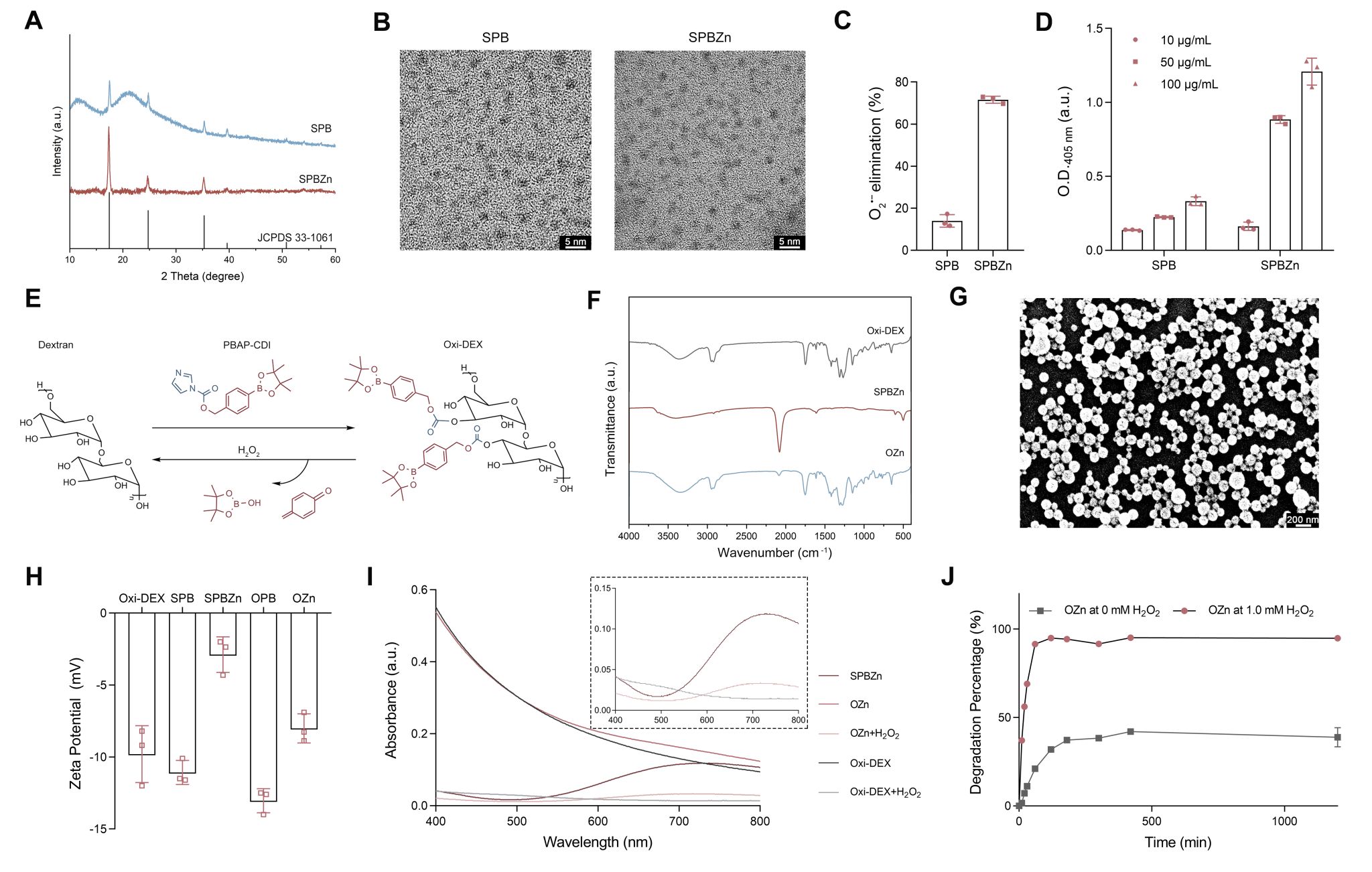
图2. 超小型诊疗一体纳米酶的设计、合成和表征
相关细胞实验结果表明OZn纳米酶能有效清除平滑肌细胞(VSMC)内的ROS,减少VSMC的钙化和凋亡,同时在单核细胞和巨噬细胞中也表现出良好的ROS清除能力,抑制炎症细胞的激活。这些结果充分说明具有抗氧化活性的OZn纳米酶在AAA的防治方面具有巨大潜力。
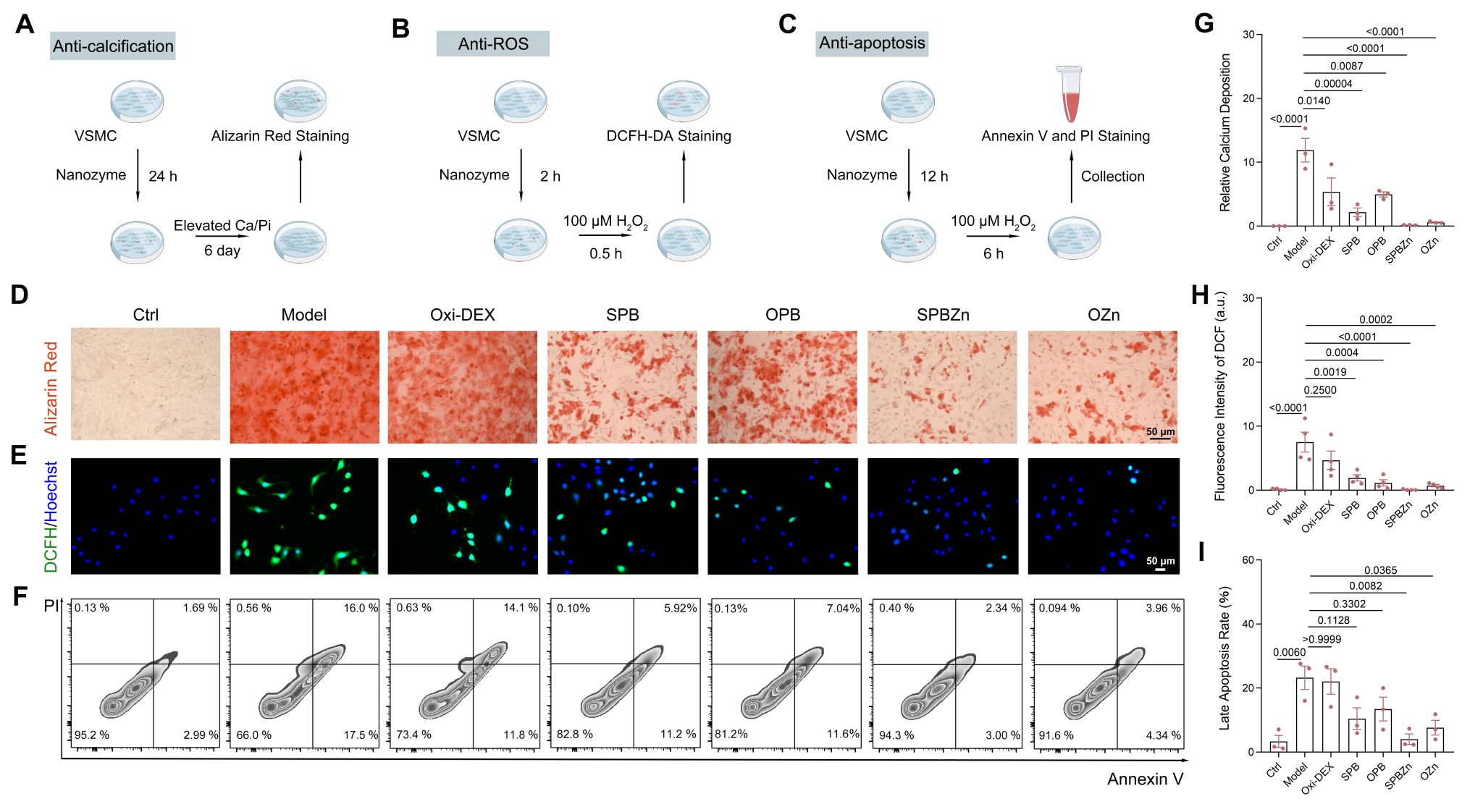
图3. 纳米酶的体外生物活性
接下来,作者验证了纳米酶的体内靶向能力(图4A)。在CaCl2诱导的AAA大鼠模型中,用FITC荧光标记的OZn验证ROS响应的OZn纳米酶对腹主动脉瘤的靶向能力。静脉注射8h后,在从AAA+大鼠中分离的腹主动脉损伤部位观察到显著更高的荧光信号(图4E)。染色显示,FITC荧光在冷冻切片的F4/80+巨噬细胞(图4C)和α-SMA+ VSMCs(图4D)细胞中定位。并且FITC-OZn在动脉瘤病变中积累并留存至少24h(图4F)。这些结果共同表明,OZn纳米酶有效地靶向动脉瘤,并长时间留存在病变部位。
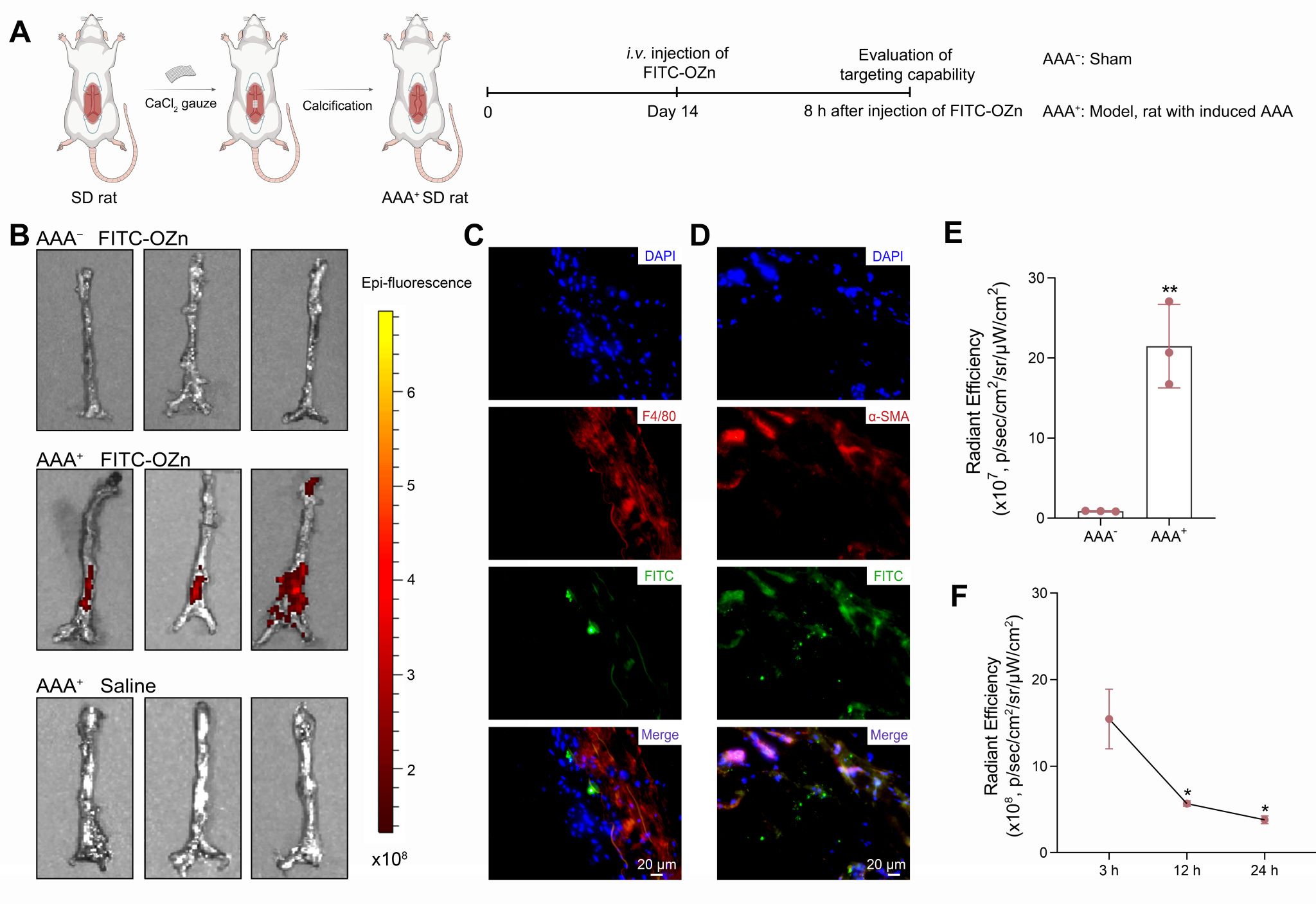
图4. 通过静脉内给药在AAA大鼠模型中体内靶向
随后,通过分析尿液中的FITC荧光和电感耦合等离子体-发射光谱法(ICP-OES)测量尿液中Fe、Zn含量,证明其对AAA的诊断潜力(如图5)。结果显示,SPBZn在AAA模型大鼠中特异性地从OZn中释放并最终从尿液排出,建立了一种通过尿液分析对AAA进行非侵入性诊断的方法。
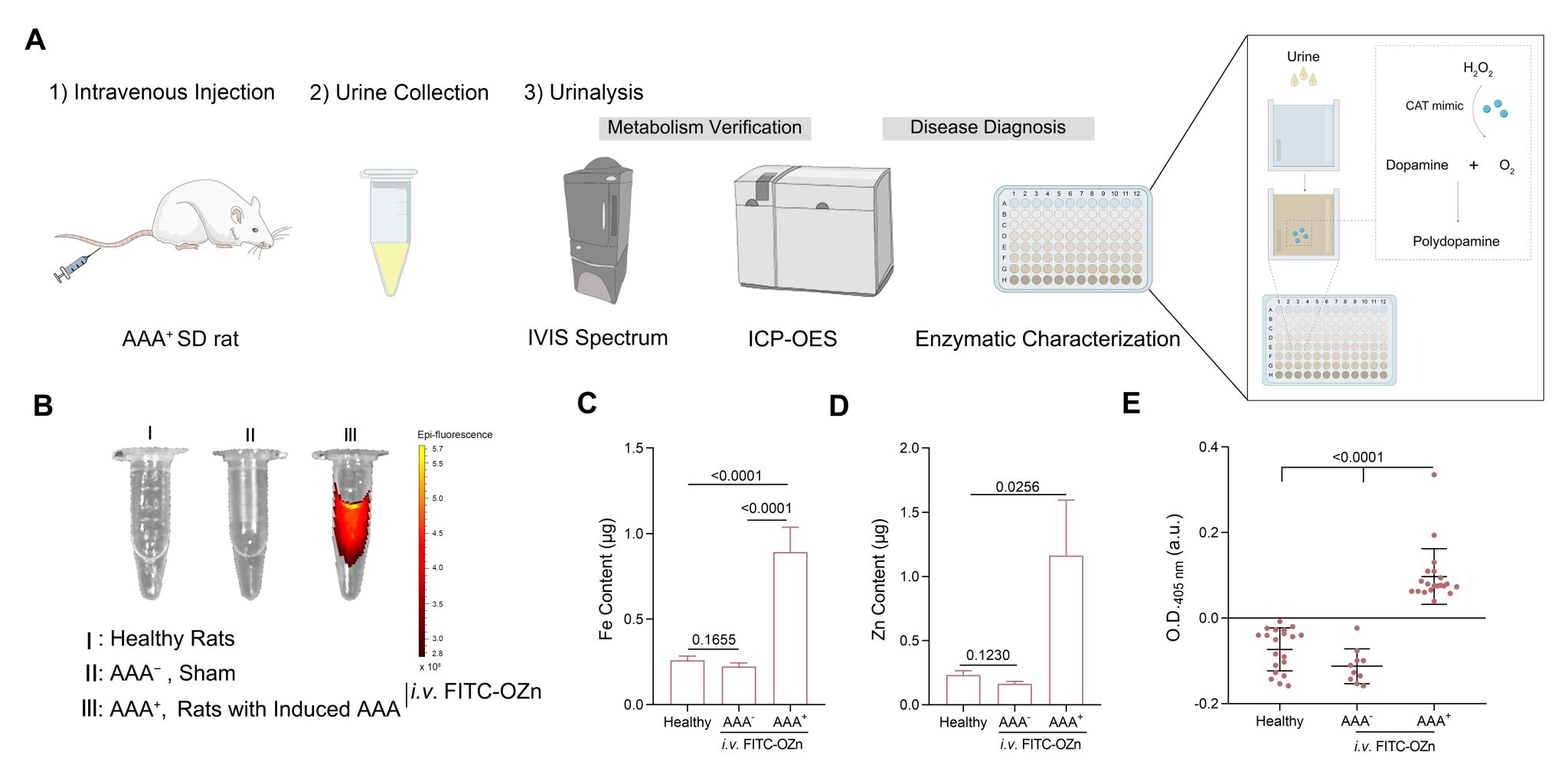
图5. 通过尿液对AAA进行诊断
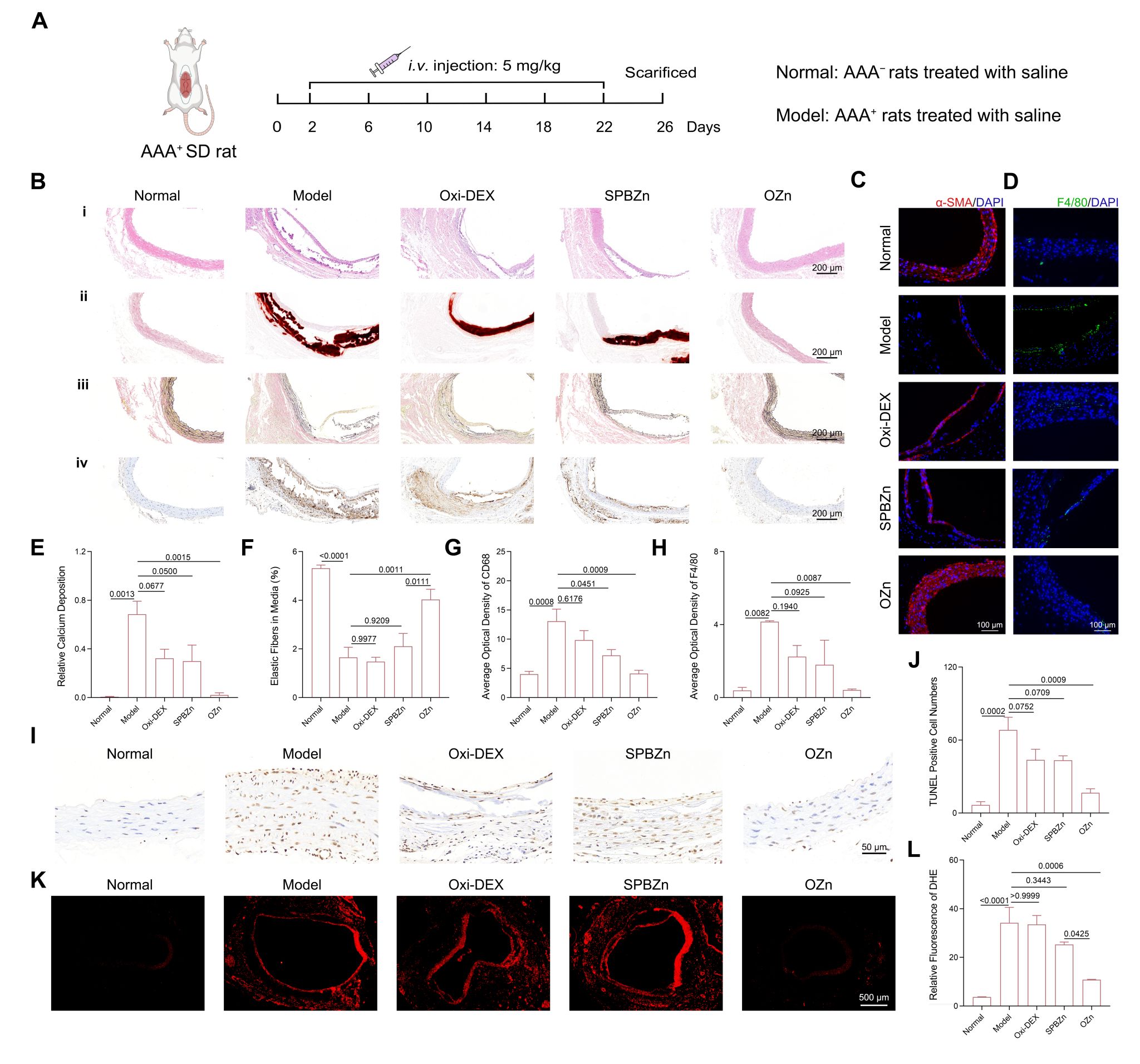
图6. 不同纳米酶在AAA大鼠体内的治疗效果
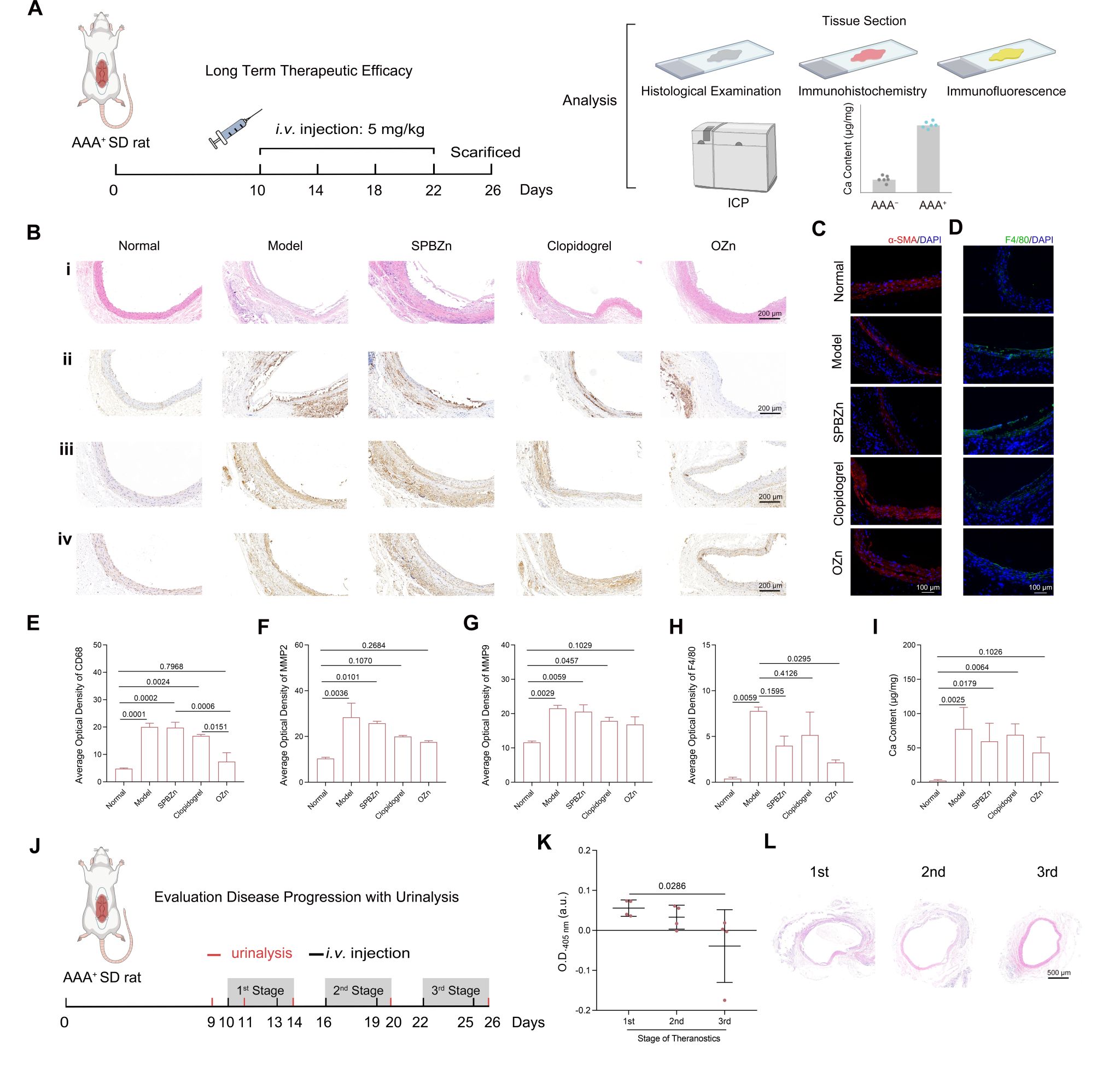
图7. OZn在长期接受CaCl2诱导腹主动脉损伤的AAA大鼠中的疗效评估以及尿液检测与疾病发展过程关系评估
在长期CaCl2诱导损伤的AAA大鼠中进一步评估了OZn的体内疗效,氯吡格雷小分子药物作为治疗的阳性对照。结果显示,OZn能有效减少钙化,减弱炎症细胞的浸润和激活,疗效上优于氯吡格雷。在疗效监测方面,我们证明,治疗后阴性结果意味着显著的治疗效果,而阳性的尿液分析意味着病理上治疗效果不显著。
随着治疗的推进,大鼠尿液中类CAT酶的信号水平持续下降。病理分析进一步证实,延长的OZn治疗显著抑制了主动脉扩张,展现了其治疗效果。尿液分析结果与治疗结果的一致性表明,这一策略具有动态调控诊断反馈和治疗效果的潜力。与传统需要分别进行诊断成像和治疗干预的方法不同,这种纳米酶能够直接调控病理微环境,同时生成SPBZn作为诊断信号。这种“边治疗边监测”的策略显著提高了临床效率,减少了额外侵入性检查的需求。
南京大学魏辉教授团队开发了一种融合早期干预与疗效监测的突破性腹主动脉瘤管理策略,构建了治疗与诊断双向联动的闭环反馈系统。所构建的多功能纳米酶凭借其多元酶活性及肾脏可清除特性,在通过尿液分析实现无创诊断监测的同时,可有效抑制动脉瘤扩张、延缓疾病进展。这项工作不仅说明了纳米酶的可修饰性,即通过精准调控其类酶催化活性与多功能特性以满足复杂生物医学需求,更推动了诊疗一体化纳米酶在心血管疾病中应用的实质性进展。该工作创新性地提出腹主动脉瘤综合管理的整合方案,展现出显著的临床转化潜力。
该研究工作以题目“An Ultrasmall Theranostic Nanozyme for Abdominal Aortic Aneurysms Management and Therapeutic Efficacy Monitoring”发表在期刊Science Advances上。
原文链接:
https://www.science.org/doi/10.1126/sciadv.adz3713
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。















要是能早点用到临床,能救不少人的命。
快点推进人体试验吧,家里老人就有这问题,等不起啊。
吃瓜群众表示看不懂原理,但感觉好厉害的样子。🤔
魏辉教授团队牛哇,又发Science子刊!
这纳米酶能经肾代谢,安全性应该不错吧?
虽然机制看起来挺复杂,但能解决AAA这种难题就是重大突破。
赞!希望早点看到临床实验。👍
通过尿液检测来无创监控疗效,这想法真绝了!
这个研究方向太有创意了,能治疗还能监测,临床转化价值很大。