中国海洋大学在蛋白质温度适应和趋同进化研究中取得新进展
文章导读
海洋鱼类如何在冰点与沸点间自由切换生存?中国海洋大学董云伟团队揭秘蛋白质温度适应的终极密码!他们通过277种鱼类乳酸脱氢酶A的深度解析,首次锁定18个关键氨基酸位点(TRSS),并用AI深度学习模型精准预测生物温度耐受能力。实验证实其中5个位点突变直接决定酶功能稳定性,颠覆传统认知——趋同进化竟是温度适应的核心机制。这项PNAS重磅研究不仅揭示物种分布背后的温度逻辑,更将海洋生物学带入智能预测新时代。15秒读懂:气候变化下,你的餐桌海鲜未来或许由这串“分子代码”掌控!
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,中国海洋大学水产学院、海水养殖教育部重点实验室、山东省海水绿色养殖与智慧渔业重点实验室、未来海洋学院董云伟教授团队构建了“分子动力学模拟–酶促动力学–蛋白表达验证–人工智能深度学习”的研究框架,将深度学习技术方法带入到海洋动物蛋白质结构研究中,系统分析了海洋鱼类蛋白质结构稳定性对温度的适应模式,揭示了其趋同进化特征。研究成果以“Temperature adaptation in structure and function in lactate dehydrogenase-A reflects convergent evolution in a few key protein regions”(乳酸脱氢酶A结构与功能的温度适应揭示蛋白质关键区域的趋同进化)为题,发表在国际知名学术期刊Proceedings of the National Academy of Sciences of the United States of America(《美国科学院院报》)。
酶结构和功能的温度稳定性差异决定着所有生物的最适和极端生存温度,理解酶结构和功能的温度适应机制有助于深入探究蛋白质结构-功能关系的演化,并从机理上揭示温度变化对物种分布的影响。随着计算机技术和人工智能的发展,大规模深入探究蛋白质结构功能的趋同进化机制成为可能。
研究团队以277种海洋鱼类的乳酸脱氢酶A为研究对象,构建了“分子动力学模拟–酶促动力学–蛋白表达验证–人工智能深度学习”的研究框架,探究了氨基酸替换对酶温度适应性的潜在影响。首先,基于Gromacs分子动力学模拟发现,酶结构稳定性随环境温度升高而增强,并确定了变异位点的位置;进而结合ColabFold蛋白质结构预测,发现18个与温度显著相关的氨基酸位点(TRSS),明确了蛋白质结构与酶适应温度的关系。并在模式生物斑马鱼上对7个TRSS进行定点突变实验和酶促动力学测定,发现5个TRSS的突变会显著影响酶功能特征(即KmPYR和热残留活性),这进一步证明了趋同进化是酶结构和功能进化的主要机制。最后,团队构建了结合图神经网络(GNN)与XGBoost算法的深度学习预测模型,从酶的结构和功能特征成功预测了生物的温度耐受能力。本研究成功将海洋动物温度功能适应研究推动到了人工智能阶段。
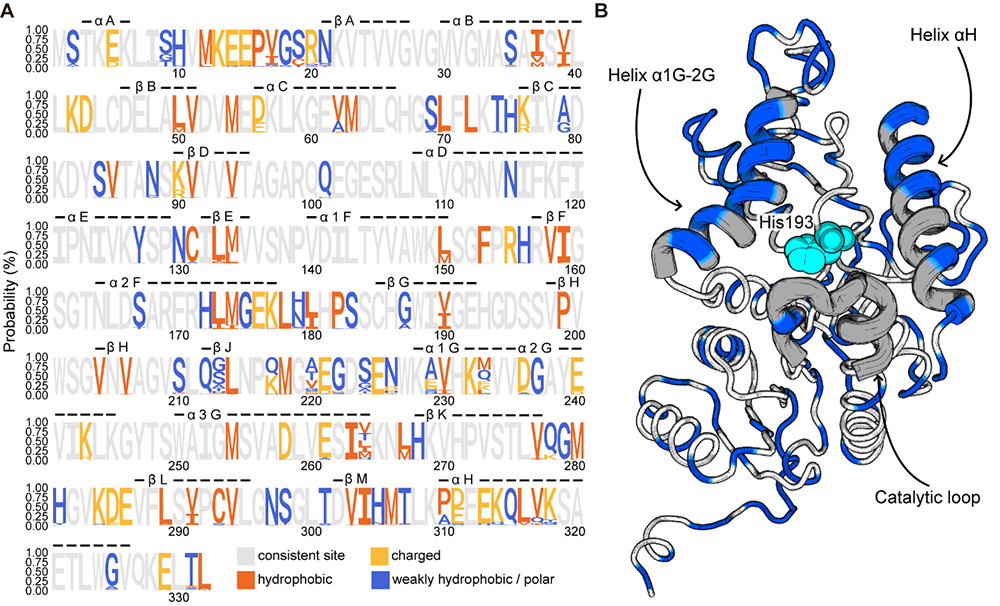
图1 海洋鱼类LDH-A同源物的序列比对和模型模拟结果

团队合影
中国海洋大学水产学院董云伟教授为文章通讯作者,中国海洋大学水产学院/未来海洋学院博士生朱晓露为第一作者。研究工作获得国家自然科学基金杰青项目、国家自然科学基金面上项目和中国海洋大学优青培育计划等项目的支持。董云伟教授团队主要从事海洋生物环境适应和分布变化相关研究,近年来在海洋动物蛋白质结构和功能适应领域以第一作者和通讯作者连续4次发表在《美国科学院院报》(PNAS)上,推动了相关领域发展。
文:朱晓露 董云伟
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...