文章导读
当巨噬细胞的极化方向决定生死,你能否想象一个钙离子通道竟掌握着炎症风暴的开关?西安交大耿晶团队在《尖端科学》发表的突破性研究揭示:Calhm6通道通过核外颗粒递送系统激活Chp1-Camk4-Creb1信号轴,精准调控巨噬细胞向M2型转化。这一机制如同免疫系统的精密调谐器——激活时可显著缓解脓毒症、急性肺损伤及肝肠炎症并促进组织修复;而缺失时则导致巨噬细胞失控极化为促炎M1型,大幅提升致死率!研究更首次解析Irf1/Stat6转录因子对Calhm6的双向调控网络,为炎症风暴相关危重症治疗开辟全新靶向策略。
— 内容由好学术AI分析文章内容生成,仅供参考。
炎症反应是机体应对感染和损伤的重要防御机制,但过度的炎症反应会导致严重的组织损伤和器官功能障碍,是败血症等疾病的主要致死原因。而巨噬细胞作为机体免疫系统的重要组成部分,因其强大的可塑性在感染、炎症及组织修复等过程中发挥着关键作用,因此如何精准调控巨噬细胞可塑性对于维持免疫稳态、促进炎症消退及组织修复具有重要意义。然而如何精确调控巨噬细胞可塑性的机制尚不完全清楚。
近日,西安交通大学第二附属医院生物诊断治疗国家地方联合工程研究中心、西安市细胞应激与疾病诊疗国际合作基地、西安交通大学精准医学研究院、生命科学与技术学院等合作研究,在国际高水平期刊《尖端科学》(Advanced Science)在线发表题为《Calhm6通过Chp1-Camk4-Creb1轴及核外颗粒递送途径调控巨噬细胞极化并参与炎症反应》(Calhm6 governs macrophage polarization through Chp1-Camk4-Creb1 axis and ectosomal delivery in inflammatory responses)的合作研究成果,揭示了钙离子通道Calhm6通过核外颗粒调控巨噬细胞参与的急性炎症和组织修复中的保护作用。
西安交通大学精准医学研究院辛彦龙博士、熊晓蕃博士为该论文的共同第一作者,耿晶教授为唯一通讯作者。论文的第一作者单位及通讯作者单位均为西安交通大学第二附属医院。

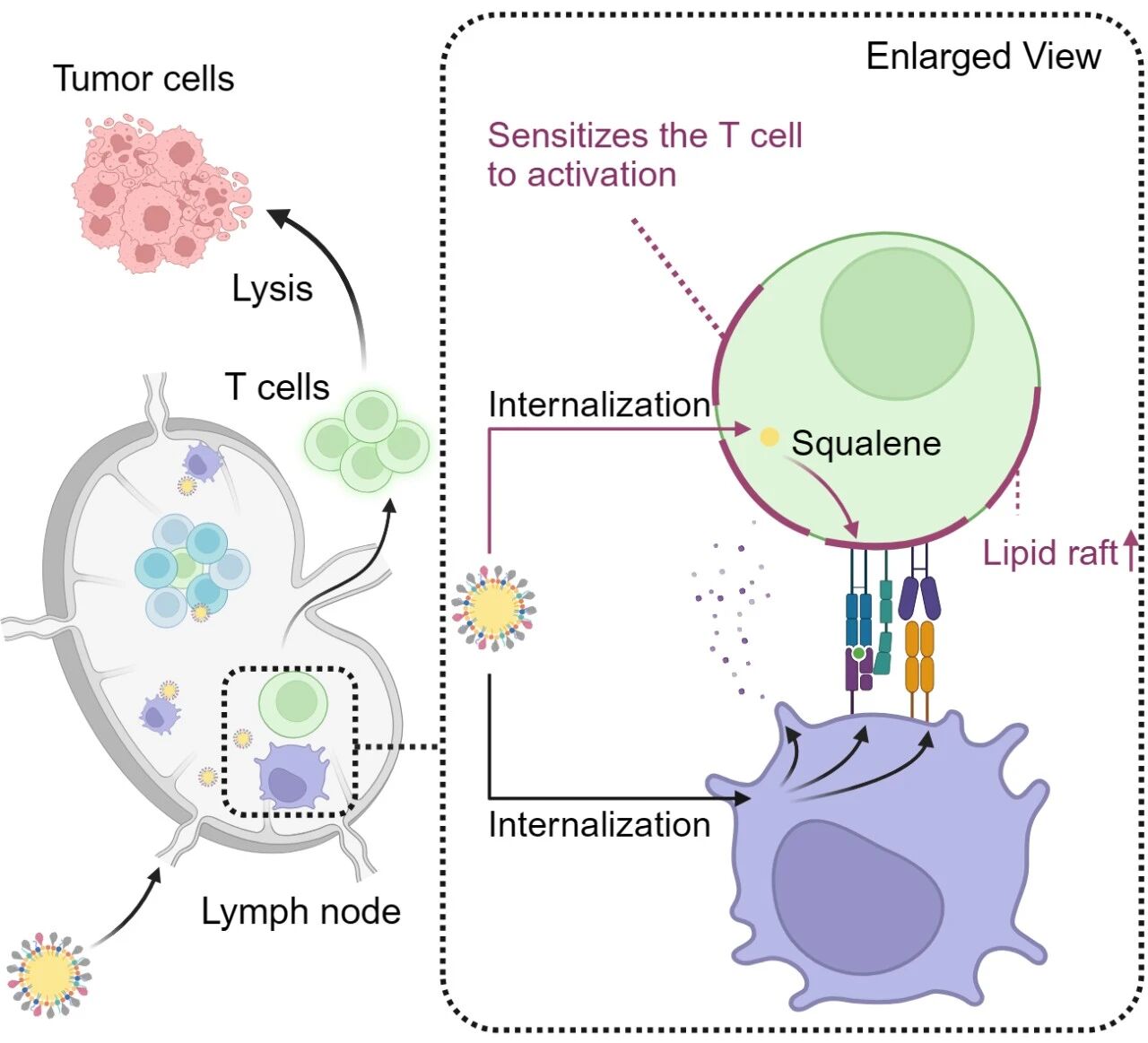
西安交大生物诊断治疗国家地方联合工程研究中心耿晶团队长期致力于研究天然免疫细胞在感染及炎症相关疾病中的病理机制。该研究发现Calhm6作为一种大孔径钙离子通道,能够介导钙离子内流,在炎症刺激下可由巨噬细胞分泌并包裹于核外颗粒(Ectosomes)中,被环境巨噬细胞内化后,通过激活Chp1-CaMK4-Creb1信号轴,推动周围巨噬细胞向M2-like极化,从而显著缓解全身性炎症、急性肺损伤、结肠炎和药物性肝损伤并促进组织修复。相反,Calhm6缺失则导致Creb1失活,使巨噬细胞倾向于M1-like极化,虽可一定程度增强杀菌效率,但显著增强小鼠在脓毒症模型中的组织损伤和致死率。
此外,耿晶团队还深入解析了Calhm6表达的转录调控机制,发现LPS/IFNγ刺激下,转录因子Irf1能够结合Calhm6启动子,促进其表达;而IL-4则通过激活Stat6,竞争性抑制Irf1的结合,从而下调Calhm6表达。这种精细的转录调控机制确保了巨噬细胞在不同免疫环境下能够精准调节Calhm6的表达水平,避免巨噬细胞可塑性失控从而维持免疫稳态。该研究不仅揭示了Calhm6在巨噬细胞极化及炎症调控中的全新功能,还为炎症相关疾病的精准治疗提供了新的潜在靶点。
耿晶团队始终以临床问题为导向,紧扣国际前沿、国家重大需求,坚持炎症与免疫调节研究。本研究得到了国家自然科学基金、国家重点研发计划、陕西省自然科学基础研究计划、陕西省基础科学研究院基础研究计划、西安市科技计划项目及西安交通大学“青年拔尖人才支持计划”等多项科研项目的资助。
论文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202502395
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...