北京师范大学北师大李辉教授团队揭示多细胞组织力学新机制:细胞间流体输运起主导作用
文章导读
颠覆传统认知!北师大李辉教授团队联合MIT郭明、中国医学科学院刘率男,在《自然·物理》重磅揭示:多细胞组织在秒至分钟尺度下,力学响应竟由细胞间流体输运主导,而非学界长期认定的粘弹性。实验直击核心——组织松弛时间随尺寸平方增长,药物干预更证实流体流动是关键机制。这一突破为破解糖尿病胰岛硬化、肿瘤发展等病理谜题提供全新物理视角,让组织工程与再生医学迎来革命性转机。速读,掌握生命力学的隐藏密码!
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,北京师范大学系统科学学院教授李辉、美国麻省理工学院教授郭明,中国医学科学院药物研究研究员所刘率男的联合研究团队在生物组织力学研究领域取得重要进展。研究团队发现,在秒至分钟的短时间尺度上,多细胞组织的力学响应主要由其内部细胞间流体输运所主导,表现出“多孔弹性”(poroelasticity)的力学特性,而非传统认识中的“粘弹性”(viscoelasticity),为理解组织发育、疾病进展以及组织工程等领域提供了全新的物理学视角。该研究成果以“Intercellular flow dominates the poroelasticity of multicellular tissues”为题,发表于《自然·物理》(Nature Physics)期刊2025年8月第21卷(DOI: 10.1038/s41567-025-02947-0)。
水是构成生命系统的基本物质,细胞功能的正常运行与其内部的含水量及动态变化密切相关。李辉团队围绕“水”在细胞及组织中扮演关键物理角色,开展了一系列研究。在单细胞尺度上,通过发展生物多尺度动力学定量实验技术,揭示了细胞含水量调控内部的分子拥挤与扩散动力学 [Angew. Chem. Int. Ed. 64, e202500998 (2025)],进而深刻影响细胞凋亡 [PNAS. 15,12118 (2018)]、迁移 [Nat. Commun. 14, 5166 (2023)]、胞内相分离 [Adv. Sci. 11, 2308338 (2024)] 等关键的生命活动;团队还实验证实了水分子通过水通道蛋白的跨膜运输受到离子液体的调控 [J. Am. Chem. Soc. 146, 13588 (2024)]。在多细胞组织尺度上,通过发展流体注入膨胀技术,精确测量了包裹在组织外侧基底膜的非线性力学特性及其对流体的渗透性,揭示了其作为物理屏障的关键力学原理 [PNAS. 118, e2022422118 (2021)]。
尽管上述研究分别阐明了细胞内部和组织边界的流体力学过程与相关生物物理响应,但在多细胞组织内部,其细胞间隙充满了间质流体(interstitial fluid),即存在于细胞之间的流体。这种间质流体的集体动力学行为如何影响组织的宏观力学特性,仍是一个尚未解决的关键科学问题。尤其是在心跳、肌肉收缩或运动损伤等快速形变过程中,其内在机制尚不明确。长期以来,学界普遍将生物组织简化为粘弹性材料模型,但这很大程度上忽略了组织内部的流体流动。
为了精准探究这一问题,研究团队自主设计并搭建了一套高精度的微尺度生物力测量平台(专利申请号:202410313368.7),其能够对三维生物组织施加精确的力学压缩,并实时测量其力学响应。
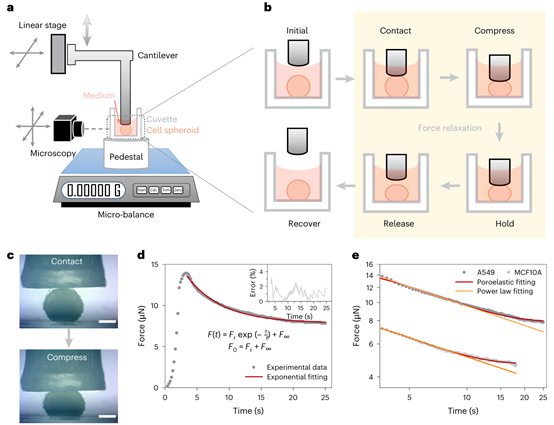
图1. 团队自主研发的微尺度力学测量平台及其工作原理示意
研究团队首先通过力学实验和有限元模拟,明确了区分多孔弹性和粘弹性两种行为的关键物理判据。这两种力学模型的关键区别在于:力学松弛时间是否依赖样品尺寸。粘弹性材料的松弛时间依赖于材料本身的粘滞系数和弹性模量等内禀属性,与样品大小无关;而多孔弹性材料的松弛则源于内部流体的流动,因此松弛时间会随样品尺寸的增大而变长。实验结果清晰地表明,无论是人工培养的细胞球,还是直接从动物体内分离的胰岛组织,其力学松弛时间均与样品尺寸的平方(L²)呈现出显著的线性关系。该结果证实,在秒至分钟的时间尺度上,这些多细胞组织均表现为典型的多孔弹性力学特征。
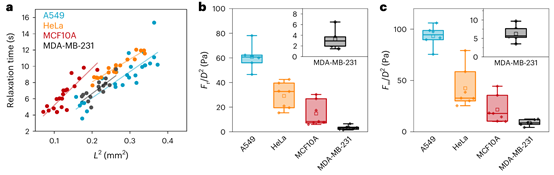
图2. 细胞球展现出典型的多孔弹性力学行为
为了进一步验证间质流体输运是这一现象的核心机制,研究团队通过药物抑制细胞间隙连接(gap junction),人为增大了细胞间隙。结果显示,细胞间隙的增大使得组织内部的流体更易于流动和重新分布,从而显著加快了力学松弛的速度。这一结果直接证明了细胞间流体输运是主导组织多孔弹性的关键物理机制。
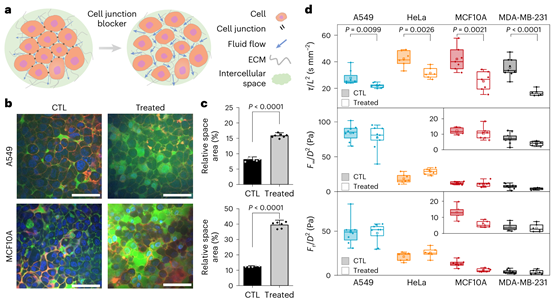
图3. 细胞间质流体输运是主导组织多孔弹性的关键物理机制
该研究不仅揭示了多细胞组织在短时间尺度下力学行为的内在物理规律,也为理解相关疾病的病理生理过程提供了新的思路。例如,研究发现糖尿病小鼠的胰岛组织比健康胰岛更“硬”,在受压时能产生更强的内部流体驱动力,从而导致其力学松弛时间反而更短,这种力学特性的改变可能与其功能异常有关。该成果将为肿瘤、发育以及再生医学等领域的发展提供重要理论支持,并为设计具有特定力学性能的工程化生物组织提供新的策略。
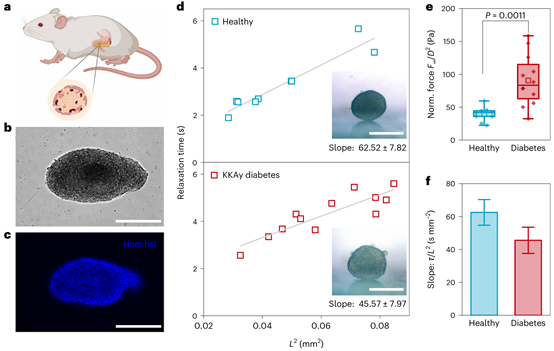
图4. 天然胰岛组织的多孔弹性力学特性及其在糖尿病中的变化
该研究得到了国家自然科学基金(12122402)和中央高校基本科研业务费专项资金的支持。
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...