文章导读
你正为新生儿胆道闭锁的致死率和缺乏明确致病机制而焦虑吗?多数研究只停留在临床症状,忽视了背后遗传通路的根源。最新的多组学大样本解析首次将细胞黏附通路异常锁定为核心驱动因素,并通过斑马鱼实验验证其致病链条。若能把握这条通路,未来的基因咨询和靶向治疗或将改写预后。到底是哪几个基因在悄悄破坏胆管极性,让疾病一步步失控?这背后隐藏的分子钥匙,你准备好揭开吗?
— 内容由好学术AI分析文章内容生成,仅供参考。
胆道闭锁(Biliary Atresia, BA)是新生儿期致死性的肝胆系统疾病,病情进展可致终末期肝病,是儿童肝移植的首要病因。尽管临床诊疗不断进步,胆道闭锁的核心发病机制至今仍未完全阐明。家族聚集性发病与同地域不同种族发病率差异等证据提示,遗传因素在胆道闭锁病因中扮演关键角色。因此,从全基因组层面系统解析其致病基因与分子通路,已成为揭示疾病本质的重要突破口。

近日,上海交通大学Bio-X研究院秦胜营团队与复旦大学附属儿科医院郑珊、董瑞教授团队合作,在期刊 Science China Life Sciences 发表题为 Multi-omics analysis provides genetic evidence for the involvement of cell adhesion pathway in the pathogenesis of biliary atresia 的研究论文。该研究不仅构建了目前国际上最大规模的胆道闭锁家系多组学图谱,更从遗传变异、转录失调、功能缺陷等角度层层递进,首次系统揭示了细胞黏附通路(Cell Adhesion Pathway)异常是胆道闭锁发生发展的重要机制,为这一疾病的遗传咨询与未来靶向干预提供了科学依据。
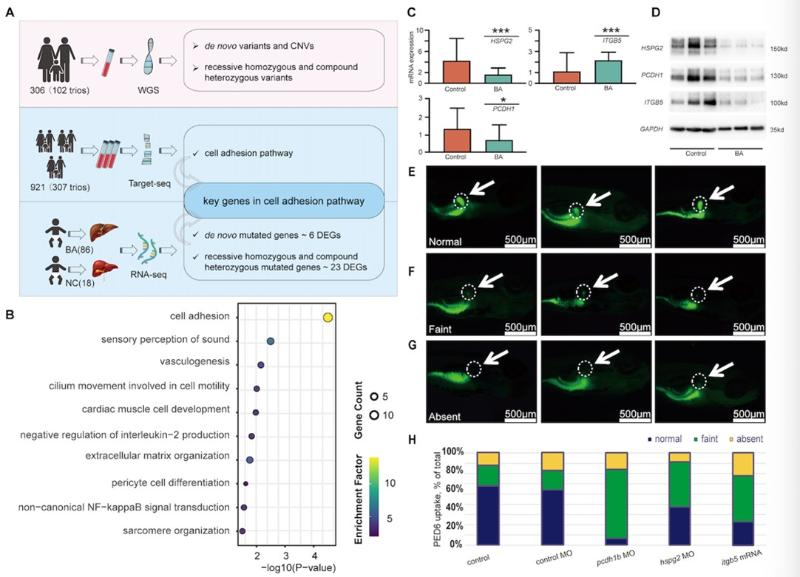
研究团队基于 409 个家系(共 1227 例样本)的大规模队列相继开展了全基因组测序及靶向基因组测序,筛选出 125 个罕见功能性变异;同时结合肝组织转录组测序数据,识别出 5532 个差异表达基因。通过跨组学联合分析,进一步挖掘出 HSPG2、LAMA5、ITGB5 及 PCDH 家族等关键候选基因,基因组变异及转录组失调的相互验证。
在机制解析方面,信号通路富集分析显示,上述候选基因显著汇聚于细胞黏附通路。为验证其致病机理,团队选取3个核心基因开展斑马鱼功能实验。结果显示,干扰这些基因表达后,斑马鱼幼鱼出现胆囊发育畸形、荧光摄取障碍等胆道闭锁样表型。进一步的细胞生物学研究表明,这些关键分子的缺陷直接破坏了胆管上皮细胞的极性建立与细胞间连接组装,导致组织结构完整性丧失。这一发现从分子到表型的完整链条上,首次明确了细胞黏功能障碍是驱动胆道闭锁发生的关键病理环节。
此项研究明确了胆道闭锁的多基因遗传特征及其关键候选基因与信号通路,为临床遗传咨询提供了直接的分子依据。团队同时指出,研究仍需在多种族人群与更大规模健康对照队列中进一步验证,从而推动基础研究成果向临床转化。
复旦大学附属儿科医院董瑞教授、上海交通大学朱金行博士、复旦大学附属中山医院叶纯静博士、神州医疗科技股份有限公司孙丰龙博士是本论文的共同第一作者。复旦大学附属儿科医院郑珊教授、上海交通大学 Bio-X 研究院秦胜营教授为本论文的共同通讯作者。
论文链接:https://doi.org/10.1007/s11427-025-3288-x
作者: Bio-X研究院 供稿单位: Bio-X研究院
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
















研究团队里有交大也有复旦,这种合作挺好的
这种遗传病是不是产前能筛查出来?
409个家系啊,这数据量确实够大
斑马鱼实验那段没太看懂,有人能解释下吗?
为啥我家孩子没这个病,看这些研究还是心里发慌
细胞黏附通路?听着挺复杂的,但找到病因就好办了