电子科技大学医学院石毅教授团队在Nature Communications上发表医工结合新成果
文章导读
膀胱癌灌注治疗为何总陷“进不去、走不远”困局?Nature Communications最新重磅研究揭晓:电子科技大学石毅团队巧妙将膀胱压力转化为“隐形发电站”!他们首创自驱动电触发系统,利用BTO压电材料捕捉天然膀胱压,自发触发化疗药物定量释放,同时激活肿瘤细胞间的隧穿纳米管“高速通道”,让药物穿透上皮屏障直达深部。更突破性的是,压力还能生成ROS增强杀伤——从细胞到猪模型实验证明,仅靠身体自身力量即可提升药效。这一医工结合里程碑,或将终结膀胱癌药物递送难题,临床转化曙光已现!
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,由电子科技大学石毅团队、电子科技大学医学院缪养宝研究员、台湾大学林宗宏教授共同开展的医工结合相关研究成果以“Self-driven electrical triggering system activates tunneling nanotube highways to enhance drug delivery in bladder cancer therapy”发表在《Nature Communications》上。

他们共同研究的自驱动电触发系统激活隧穿纳米管通路以增强膀胱癌治疗中的药物递送,聚焦一个长期困扰临床的核心难题——膀胱内灌注化疗中药物渗透差、释放不可控。作者提出的解决思路颇具原创性,同时具备扎实的科学逻辑:利用膀胱天然“膀胱压”作为内源能源,驱动铁电/压电材料(BTO)在体内自发发电,进而触发药物定量释放、诱导隧穿纳米管(TNTs)大量生成,并显著提高化疗药物在肿瘤细胞间的快速传递效率。构建的BTO-CPT/FA 纳米系统兼具三重功能:①压电驱动自发电,实现CPT的定量、可控释放;②激活TNT“高速传输通道”,促进跨细胞的快速药物递送;③压力触发ROS生成,进一步增强肿瘤杀伤效应。整体设计充分体现了材料科学、力电转换、生物屏障突破及肿瘤微环境调控的深度交叉。思路严谨、体系完整,尤其是从小鼠到兔再到猪的多物种膀胱模型中验证“压力驱动深度渗透”的实验,凸显出非常强的临床转化潜力。
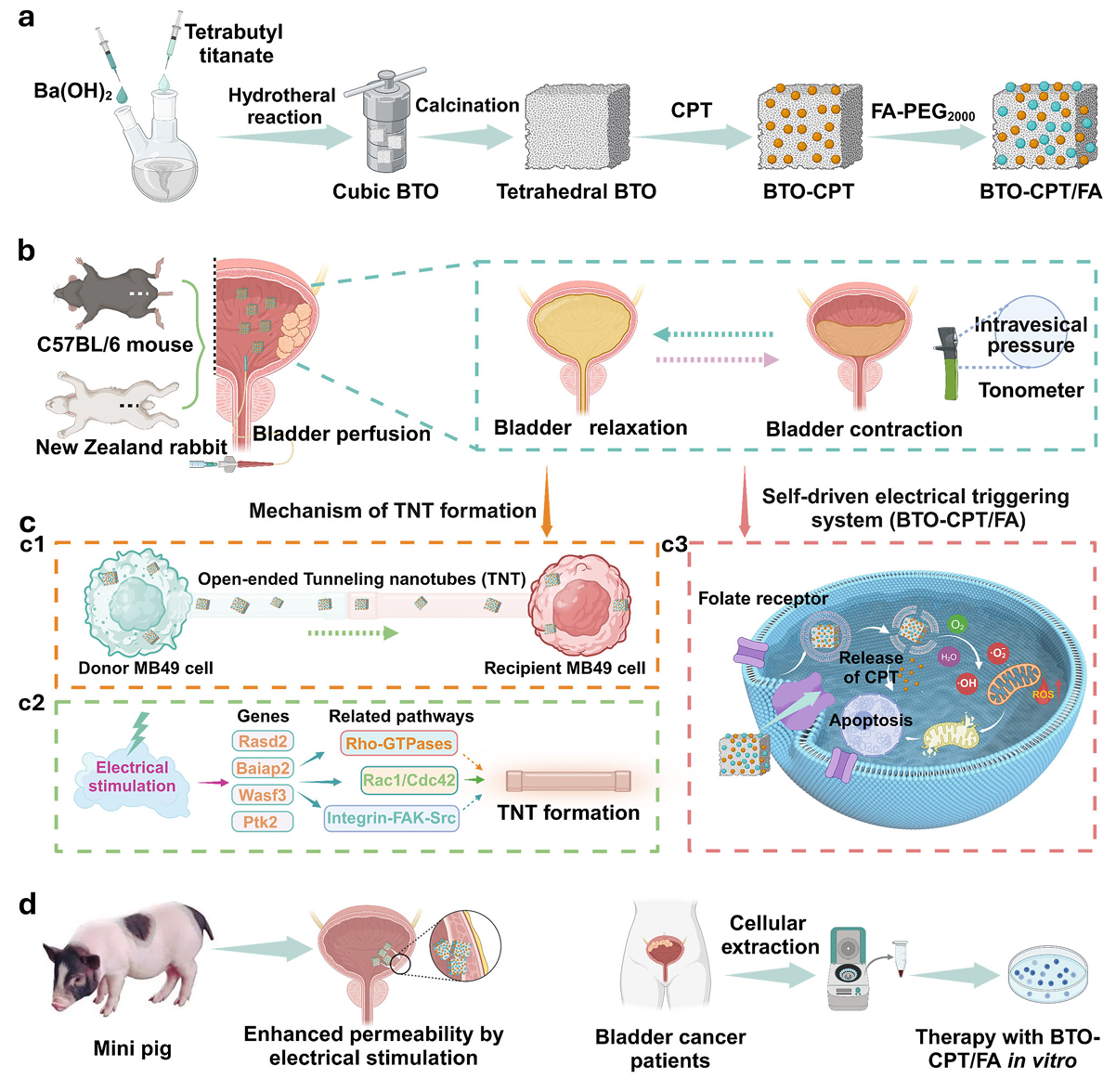
图1:自驱动电触发系统的构建与工作机制
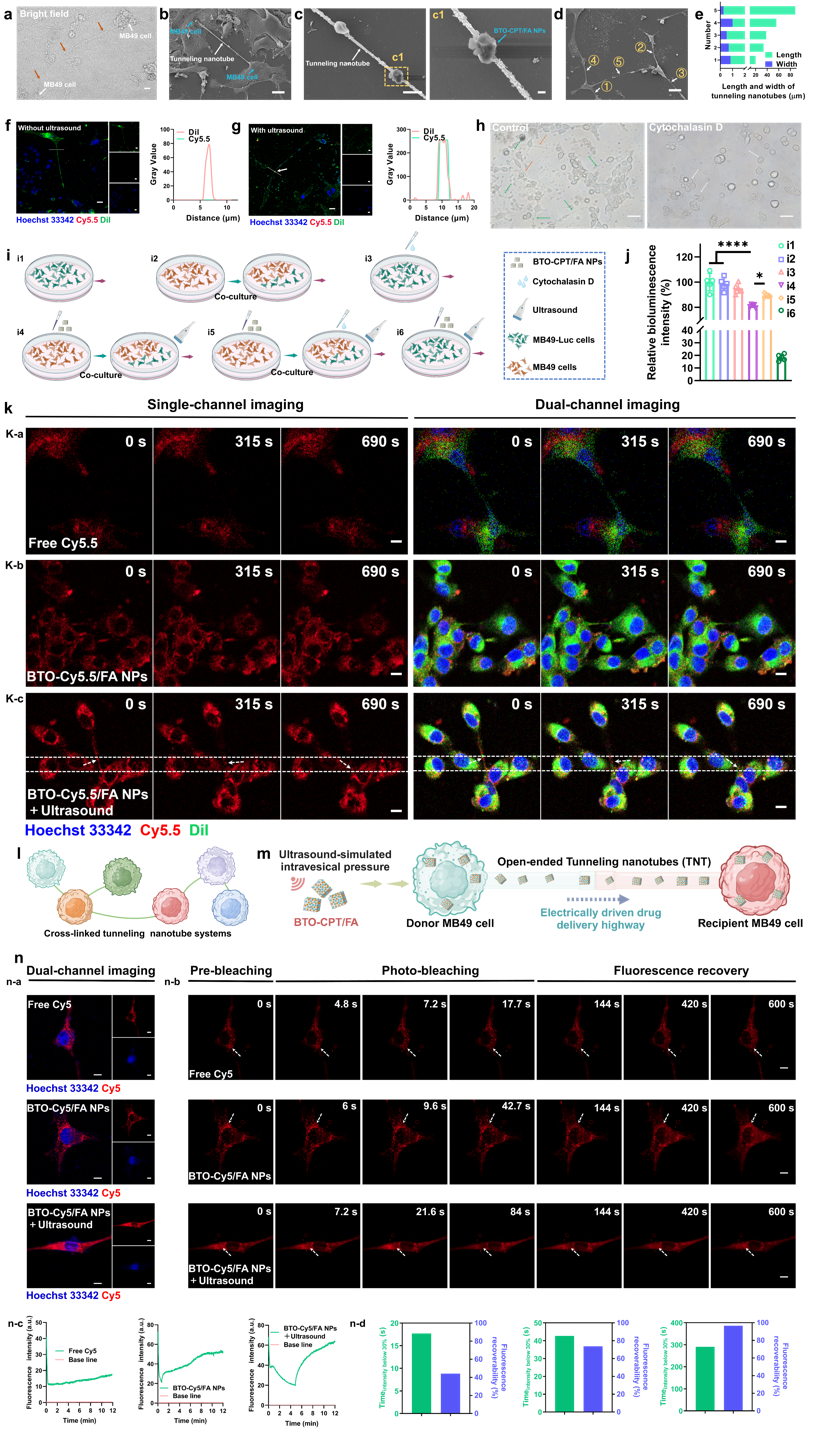
图2:通过隧穿纳米管的高速递送
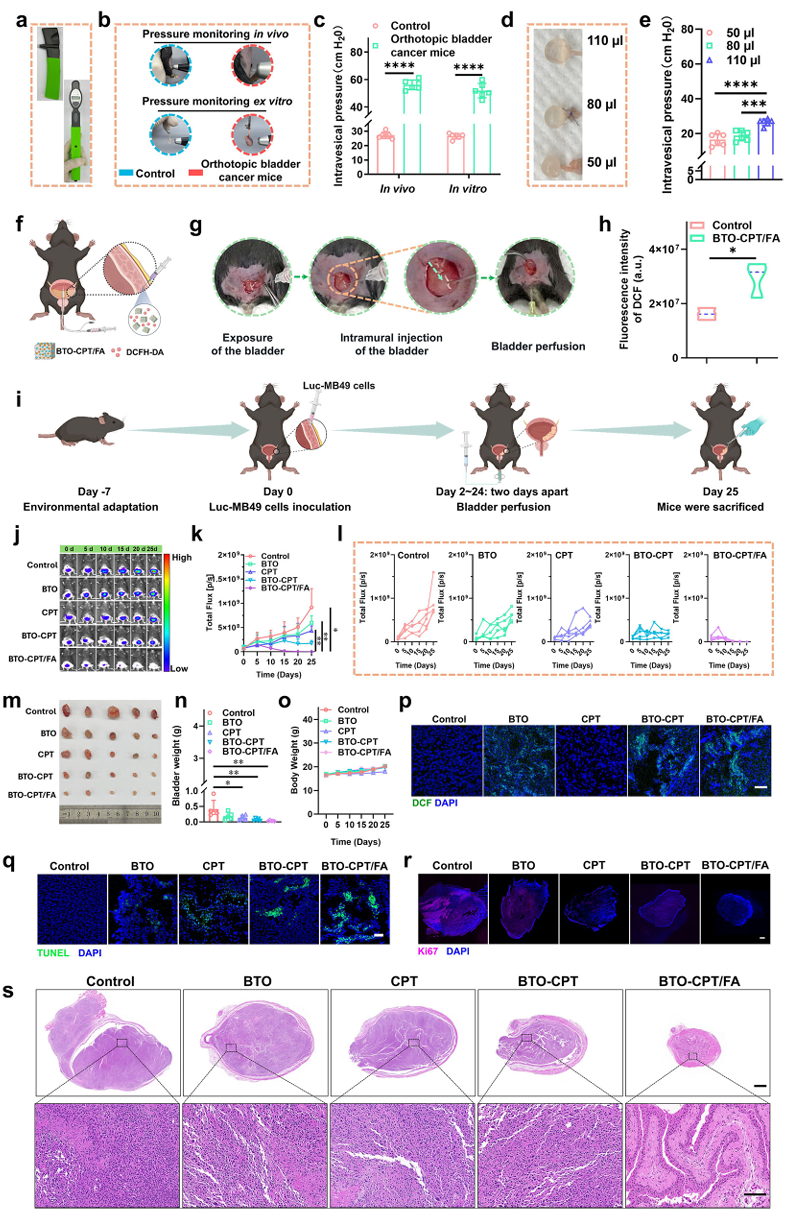
图3:在体抗肿瘤疗效评估(小鼠)
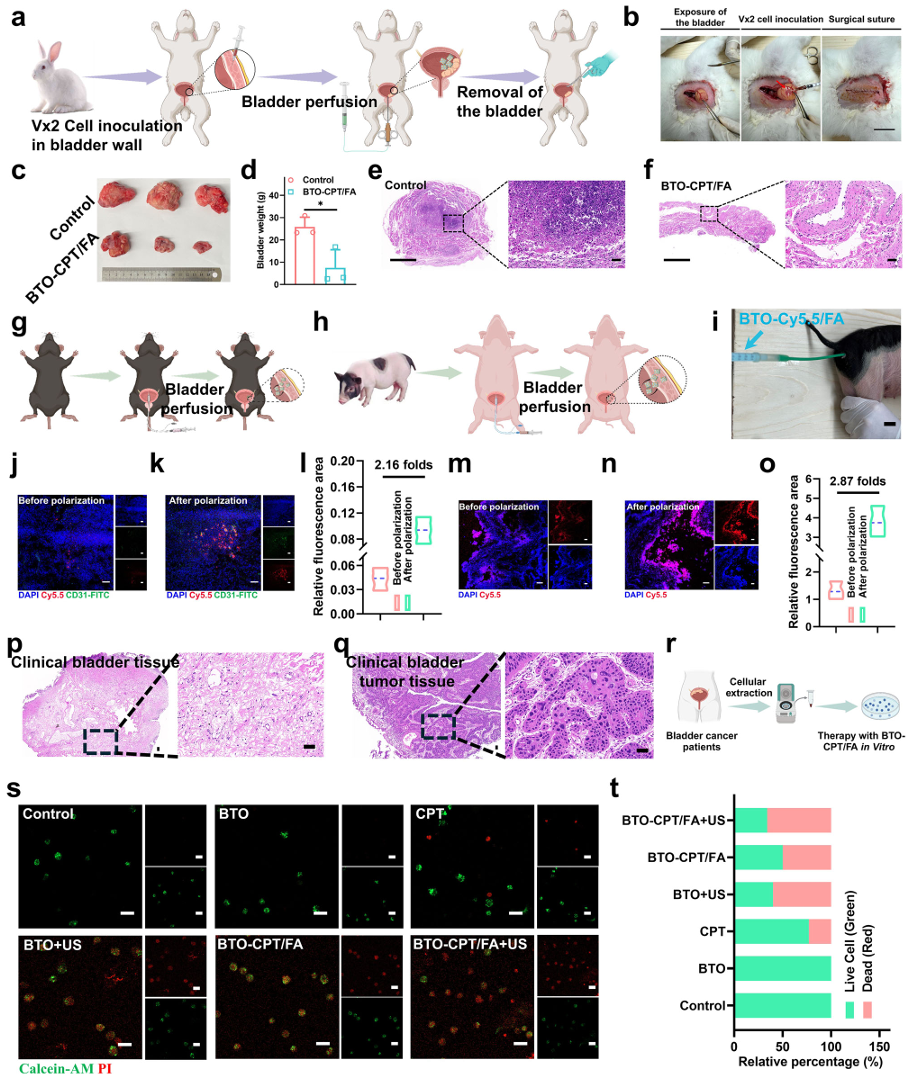
图4:大动物与临床细胞验证及膀胱通透性评估
本研究亮点:(1)膀胱癌灌注治疗最大的障碍不是药物本身,而是“进不去、走不远、留不住”,这篇 Nature Communications 最新研究提出了一个非常聪明的方案:把膀胱压力变成能源,让药物自己“发电”、自己“冲刺”。(2)在自发电材料的驱动下,化疗药沿着隧穿纳米管高速运输,直接突破膀胱上皮这一关键屏障,实现深部递送与强效杀伤。(3)从细胞,到小鼠、兔,再到小型猪膀胱模型,作者完整地证明了:只靠膀胱自身的压力,就能激活药物释放与ROS生成,大幅提升治疗效果。
原文链接:https://www.nature.com/articles/s41467-025-65017-2
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。


















化疗药自己“冲刺”?这设计简直科幻照进现实!
自发电+纳米管递送,医工交叉的天花板了吧!
吃瓜群众表示:看完只想问一句,啥时候能用上?🤔
这研究太硬核了!膀胱压力变能源,脑洞大开又实用👍