中国海洋大学在手性生物电子等排体合成领域取得新进展
文章导读
如何突破药物分子立体化学优化的瓶颈?中国海洋大学王洪玉教授联合中科院上海有机所赵刚研究员,开发出镍催化烯醛不对称交叉偶联新方法,高效构建α-羟基酮类手性生物电子等排体。该反应兼容多种官能团,产率高达94%,对映选择性达99.8:0.2,可规模化制备并实现多样化衍生。这一突破为多肽类药物等复杂分子的立体结构精准调控提供了全新工具,有望推动三维药物分子设计的创新发展。
— 内容由好学术AI分析文章内容生成,仅供参考。
近日,中国海洋大学医药学院、海洋药物教育部重点实验室王洪玉教授联合中国科学院上海有机化学研究所赵刚研究员,在不对称催化烯醛交叉偶联反应构建手性生物电子等排体方面取得新进展。相关研究成果以“Nickel-Catalyzed Regioselective and Enantioselective Olefin-Aldehyde Cross-Couplings toward Acyloin Isosteres”(镍催化区域和对映选择性烯醛交叉偶联反应构建α-羟基酮生物电子等排体)为题,发表在国际知名学术期刊Angewandte Chemie International Edition(《德国应用化学》)上。
生物电子等排取代已成为现代药物研发中的关键策略,尤其适用于将二维官能团替换为三维结构,以改善如溶解度、代谢稳定性和靶点选择性等类药特性。近年来,该领域研究主要集中于三维脂肪族生物电子等排体的多样化设计,这类结构具有调节分子构象等优势而受到广泛关注。然而,生物活性分子中普遍存在手性特征,且立体化学单元常与平面药效团相邻,导致许多药物靶点需要精确的立体化学匹配才能实现最佳结合,这也极大限制了生物电子等排取代的结构保真度。因此,在三维生物电子等排体附近构建手性中心的不对称合成方法,仍是极具挑战的研究方向,这也制约了对临床验证骨架进行立体化学优化的药物类似物研发。
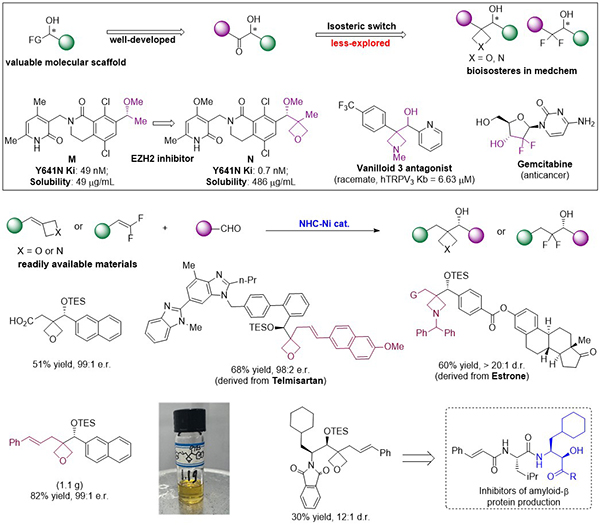
图1 不对称烯醛交叉偶联反应构建α-羟基酮生物电子等排体砌块
针对以上问题,研究团队发展了一种镍催化的醛与四元杂环烯烃的不对称还原交叉偶联反应,可高效、高选择性地构建α-羟基酮生物电子等排体。在N-杂环卡宾(NHC)配体的调控下,该反应具有广泛的官能团兼容性,能够以高达94%的产率和99.8:0.2的对映体比例(e.r.)生成富含对映异构体的产物。该方案也适用于合成富含对映异构体的α-羟基二氟亚甲基烷烃。机理研究揭示了张力驱动的反应活性与配体调控如何共同主导化学选择性、区域选择性和立体选择性。通过克级规模制备及多样化的衍生化实验,验证了该方法的合成实用性,为高效获取以往难以制备如多肽类药物分子的特定立体结构生物电子等排体,提供了多功能的结构优化平台。

团队合影(前排中为王洪玉教授)
中国海洋大学为该论文的第一通讯单位,中国海洋大学医药学院王洪玉教授与上海有机化学研究所赵刚研究员为共同通讯作者,医药学院博士研究生张明帅为第一作者。研究工作得到了国家自然科学基金、泰山学者青年专家、中国海洋大学青年英才启动经费等项目资助。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202510690
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...